23/12/2011
La Reacción en Cadena de la Polimerasa (PCR) en tiempo real, o qPCR, ha revolucionado la forma en que estudiamos el medio ambiente. Desde la detección de ADN ambiental (eDNA) para rastrear especies raras en un río, hasta la cuantificación de microorganismos que indican contaminación en el suelo, esta técnica es una herramienta indispensable para el ecologista moderno. Sin embargo, su alta sensibilidad también la hace susceptible a errores que pueden comprometer la validez de un estudio completo. Un resultado fallido no solo significa una pérdida de tiempo y recursos, sino que puede llevar a conclusiones ecológicas erróneas, como declarar falsamente la ausencia de una especie en peligro o la presencia de un patógeno inexistente. En este artículo, abordaremos los problemas más comunes que enfrentan los investigadores en sus experimentos de qPCR y cómo solucionarlos para asegurar la integridad de nuestros datos ambientales.
El Experimento Silencioso: ¿Por Qué Mi qPCR No Muestra Señal?
Uno de los resultados más frustrantes en un experimento de qPCR es la ausencia total de señal de amplificación en las curvas. Observar una línea plana cuando esperabas una curva sigmoidea puede generar una gran incertidumbre. ¿Significa que el ADN de la especie objetivo no está en la muestra, o es un fallo técnico? Antes de sacar conclusiones biológicas, es crucial descartar los problemas técnicos. A continuación, se detallan las causas más comunes.
1. Ausencia del Molde de ADN (Template)
Parece trivial, pero es la primera comprobación obligatoria. En la vorágine del trabajo de laboratorio, con múltiples muestras y reacciones, es sorprendentemente fácil olvidar añadir la muestra de ADN a la mezcla de PCR. Antes de embarcarte en una compleja odisea de resolución de problemas, revisa tus notas de laboratorio y, si es posible, tu protocolo de pipeteo. Un simple descuido puede ser la causa, y verificarlo te ahorrará horas de trabajo.
2. La Presencia de Inhibidores en la Muestra
Las muestras ambientales son notoriamente "sucias". El suelo, el agua de sedimentos, los tejidos vegetales o los fluidos corporales de animales contienen una gran cantidad de sustancias que pueden inhibir la reacción de PCR. Compuestos como los ácidos húmicos y fúlvicos del suelo, fenoles de plantas, sales, o metales pesados pueden bloquear la actividad de la polimerasa. Si sospechas que este es el problema, tienes varias soluciones:
- Dilución de la muestra: Diluir tu muestra de ADN puede reducir la concentración de inhibidores a un nivel que ya no afecte a la reacción, aunque también reducirá la concentración de tu ADN diana.
- Aditivos para PCR: La adición de ciertos reactivos a la mezcla maestra puede contrarrestar el efecto de los inhibidores. Los más comunes son la Albúmina de Suero Bovino (BSA), el dimetilsulfóxido (DMSO) o la betaína.
- Uso de Controles Internos Positivos (IPC): Esta es una de las soluciones más elegantes. Un IPC consiste en añadir una secuencia de ADN sintético y su correspondiente par de cebadores/sonda a la reacción. Si tu muestra amplifica el IPC pero no tu gen diana, la PCR funciona y tu diana probablemente no está presente. Si ni el IPC ni tu diana amplifican, entonces tienes una inhibición clara.
3. Problemas con la Sonda o los Cebadores (Oligonucleótidos)
La calidad y el diseño de tus sondas y cebadores son fundamentales. Un problema aquí puede ser la causa directa de la falta de señal:
- Degradación: Los oligonucleótidos son sensibles a ciclos repetidos de congelación y descongelación. Almacenarlos incorrectamente o usarlos después de demasiados ciclos puede degradarlos, impidiendo que se unan eficazmente a su secuencia diana.
- Diseño incorrecto: Un diseño de sonda o cebador que no sea óptimo puede resultar en una unión ineficiente o nula al producto amplificado, especialmente si las condiciones de la PCR (como la temperatura de anillamiento) no son las adecuadas.
4. Perfil Térmico No Optimizado
La qPCR es un baile molecular preciso que depende de temperaturas y tiempos exactos. Asegúrate de que tu perfil térmico es el adecuado para tus cebadores y la longitud de tu amplicón. Un tiempo de desnaturalización insuficiente, una temperatura de anillamiento demasiado alta o un tiempo de extensión demasiado corto pueden impedir una amplificación eficiente.
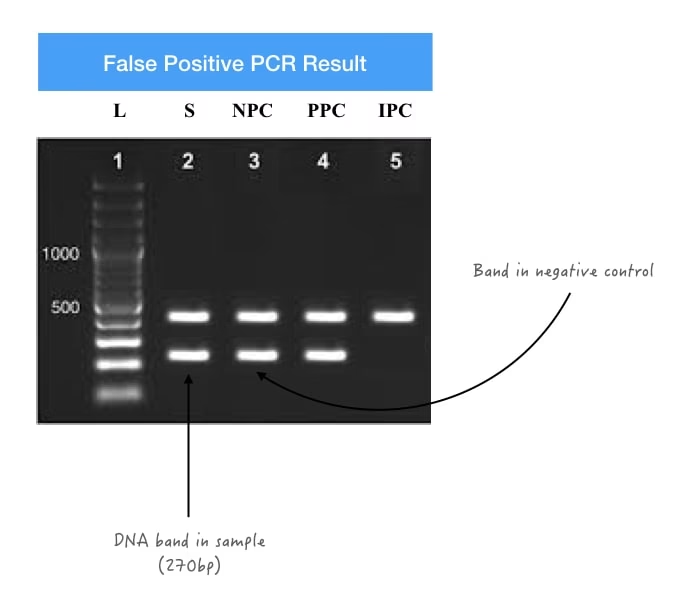
El Fantasma en la Máquina: Señal en el Control Negativo
Quizás más alarmante que la ausencia de señal es la aparición de una señal en tu control negativo (NTC, No Template Control). Este resultado invalida potencialmente toda la corrida experimental, ya que sugiere que hay contaminación o artefactos en la reacción. En un contexto ambiental, un falso positivo podría llevar a reportar erróneamente la presencia de una especie invasora, provocando costosas e innecesarias medidas de gestión.
1. Contaminación con el Molde de ADN
La causa más directa de una señal en el NTC es la contaminación cruzada. Una minúscula cantidad de ADN de una muestra positiva o del producto de una PCR anterior puede haber contaminado tus reactivos, tus puntas de pipeta o tu espacio de trabajo. La PCR es tan sensible que puede amplificar incluso unas pocas moléculas de ADN contaminante. Para evitarlo, es fundamental seguir buenas prácticas de laboratorio: usar puntas con filtro, trabajar en cabinas de PCR separadas para la preparación de la mezcla y la adición de la muestra, y limpiar regularmente las superficies y el equipo con soluciones descontaminantes (como lejía diluida o soluciones específicas).
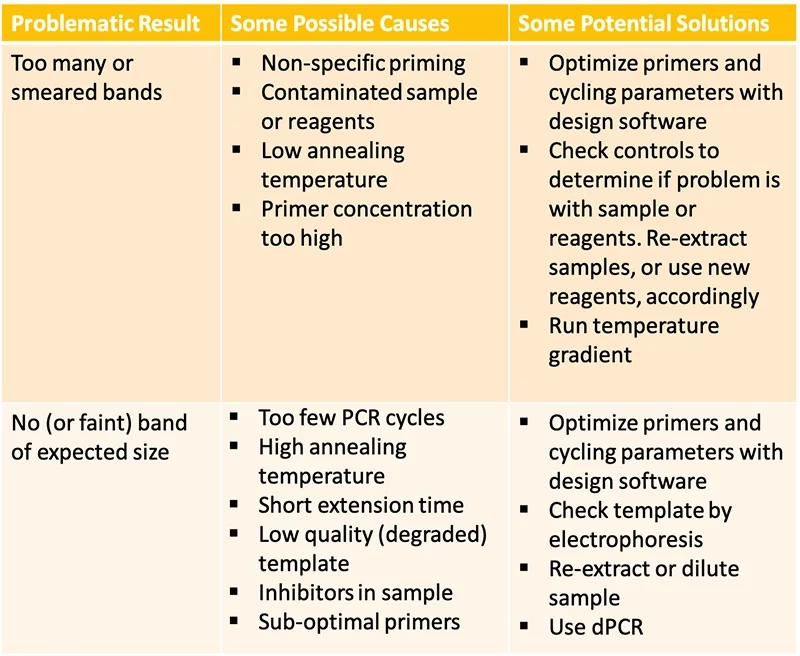
2. Formación de Dímeros de Cebadores
A veces, la señal positiva no proviene de una contaminación real, sino de un artefacto de la reacción. Los dímeros de cebadores (o primer-dimers) se forman cuando las moléculas de los cebadores se unen entre sí en lugar de unirse al molde de ADN. Esta estructura puede ser extendida por la polimerasa, generando un producto corto que, si estás usando un agente intercalante como SYBR Green, producirá una señal fluorescente. Para diagnosticar este problema, puedes realizar un análisis de curva de fusión (melting curve) al final de la corrida. Los dímeros de cebadores suelen tener una temperatura de fusión más baja y aparecerán como un pico distinto al de tu producto específico.
Tabla Comparativa de Problemas y Soluciones en qPCR
| Problema Detectado | Causa Común | Solución Clave | Impacto Ambiental del Error |
|---|---|---|---|
| Ausencia de señal en todas las muestras | Olvido de añadir el ADN; inhibidores potentes; degradación de la sonda. | Revisar protocolo; usar controles internos (IPC); alicuotar y almacenar correctamente los oligos. | Falso negativo: concluir erróneamente la ausencia de una especie o patógeno. |
| Señal en el control negativo (NTC) | Contaminación cruzada; formación de dímeros de cebadores. | Mejorar las prácticas asépticas; realizar análisis de curva de fusión; rediseñar cebadores. | Falso positivo: reportar la presencia de una especie o contaminante que no está ahí. |
| Baja eficiencia de la PCR | Concentración subóptima de reactivos; perfil térmico inadecuado. | Optimizar la concentración de MgCl2 y cebadores; realizar un gradiente de temperatura. | Cuantificación inexacta de la carga de ADN, afectando estudios poblacionales o de contaminación. |
Preguntas Frecuentes (FAQ)
¿Qué es exactamente un control interno positivo (IPC) y por qué es tan crucial en muestras ambientales?
Un IPC es una secuencia de ADN no relacionada con tu objetivo que se añade en una cantidad conocida a cada reacción, junto con sus propios cebadores y sonda. Sirve como un control de calidad para la propia reacción de PCR. Si el IPC amplifica correctamente en una muestra donde tu gen diana no lo hace, puedes estar seguro de que la reacción no fue inhibida y que la ausencia de señal se debe a la ausencia real del ADN diana. Es vital para muestras ambientales porque la probabilidad de inhibición es muy alta.
¿Cómo puedo saber si mi muestra tiene inhibidores antes de hacer la qPCR?
Una forma sencilla es realizar una PCR de prueba. Prepara dos reacciones para la misma muestra: una con tu ADN ambiental y otra con tu ADN ambiental más una cantidad conocida de ADN control positivo. Si la reacción con el control positivo añadido muestra una amplificación tardía o nula en comparación con el control positivo solo, es una clara señal de que tu muestra contiene inhibidores.
¿Qué son los dímeros de cebadores y cómo los evito?
Son artefactos formados por la unión de los cebadores entre sí. Para evitarlos, es fundamental un buen diseño bioinformático de los cebadores, asegurándose de que no tengan complementariedad entre ellos, especialmente en sus extremos 3'. Además, usar una polimerasa "Hot Start" que solo se activa a alta temperatura puede reducir significativamente su formación, ya que evita la actividad enzimática durante la preparación de la reacción a temperatura ambiente.
En conclusión, la qPCR es una técnica poderosa pero exigente. La fiabilidad de nuestros estudios ecológicos, desde la conservación de la biodiversidad hasta la vigilancia de la salud de los ecosistemas, depende de nuestra capacidad para generar datos precisos y reproducibles. Prestar atención a los detalles, entender las posibles fuentes de error y utilizar los controles adecuados no es solo una buena práctica de laboratorio; es una responsabilidad científica para asegurar que nuestras conclusiones contribuyan positivamente a la protección de nuestro planeta.
Si quieres conocer otros artículos parecidos a PCR en Tiempo Real: Guía para Ecologistas puedes visitar la categoría Ecología.