06/03/2019
La extracción de ARN es una técnica fundamental en el campo de la biología molecular, que permite el aislamiento del ácido ribonucleico a partir de muestras biológicas. Este proceso es indispensable para estudiar la expresión génica, comprender los procesos celulares y diagnosticar enfermedades. Dentro de las múltiples metodologías existentes, el uso del reactivo TRIzol se ha consolidado como uno de los métodos más fiables y eficientes para obtener ARN de alta calidad, esencial para análisis moleculares posteriores como la RT-qPCR, la secuenciación de ARN (RNA-seq) o los microarrays.
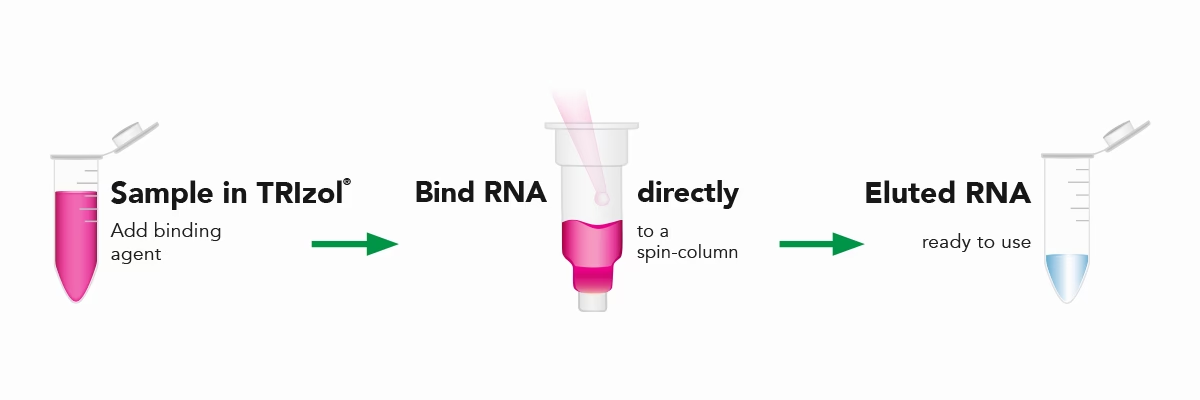
¿Qué es el Reactivo TRIzol y Cómo Funciona?
El TRIzol es una solución monofásica lista para usar, diseñada para el aislamiento simultáneo de ARN, ADN y proteínas a partir de una amplia variedad de materiales biológicos, como tejidos animales y vegetales, células en cultivo y bacterias. Sus componentes principales son el isotiocianato de guanidinio y el fenol, que actúan en conjunto para lograr una separación eficaz y proteger la integridad del ARN.
El isotiocianato de guanidinio es un potente agente caotrópico que cumple una doble función crucial: primero, lisa las células al desorganizar las membranas lipídicas y, segundo, desnaturaliza las proteínas, incluidas las potentes ribonucleasas (RNasas), que de otro modo degradarían rápidamente el ARN liberado. Esta desnaturalización inmediata es clave para preservar la molécula de ARN. Por otro lado, el fenol es un solvente orgánico que, en combinación con el cloroformo que se añade posteriormente, facilita la separación de los ácidos nucleicos de las proteínas y otros componentes celulares. El pH ácido del TRIzol (aproximadamente 5) es fundamental, ya que asegura que el ARN permanezca en la fase acuosa superior, mientras que el ADN se particiona en la interfase o en la fase orgánica inferior.
El Proceso de Extracción Paso a Paso
El protocolo de extracción con TRIzol es un procedimiento meticuloso que requiere precisión en cada etapa para garantizar un alto rendimiento y pureza. A continuación, se detalla el proceso estándar.
1. Homogeneización
El primer paso consiste en lisar completamente la muestra biológica dentro del reactivo TRIzol para liberar el contenido celular. La forma de proceder varía según el tipo de muestra:
- Tejidos: Se requiere una disrupción mecánica. Generalmente, se utilizan homogeneizadores mecánicos (tipo rotor-estator) para descomponer a fondo la estructura tisular. La proporción recomendada es de 1 mL de TRIzol por cada 50-100 mg de tejido.
- Células en suspensión o monocapas: Las células se pueden lisar directamente en la solución de TRIzol mediante pipeteo repetitivo. Se utiliza 1 mL de TRIzol por cada 5-10 x 10⁶ células.
Es vital que el volumen de la muestra no exceda el 10% del volumen de TRIzol utilizado. Una vez mezclado, el lisado debe reposar a temperatura ambiente durante 5 minutos para asegurar la disociación completa de los complejos nucleoproteicos.
2. Separación de Fases
Tras la homogeneización, se añade cloroformo para separar la mezcla en distintas fases. Se agrega 0.2 mL de cloroformo por cada 1 mL de TRIzol utilizado. La mezcla se agita vigorosamente durante 15 segundos hasta que adquiere una apariencia lechosa y homogénea. Luego, se deja reposar a temperatura ambiente entre 2 y 15 minutos. Posteriormente, se centrifuga a 12,000 x g durante 15 minutos a 4°C. Esta centrifugación separa el lisado en tres capas bien definidas:
- Fase acuosa superior: Incolora, contiene el ARN.
- Interfase: Una capa blanquecina donde se acumula el ADN.
- Fase orgánica inferior: De color rojo (debido al fenol), contiene proteínas y lípidos.
Con extremo cuidado, se debe transferir la fase acuosa superior a un nuevo tubo libre de RNasas, evitando aspirar cualquier parte de la interfase o la fase orgánica, ya que esto contaminaría la muestra de ARN.
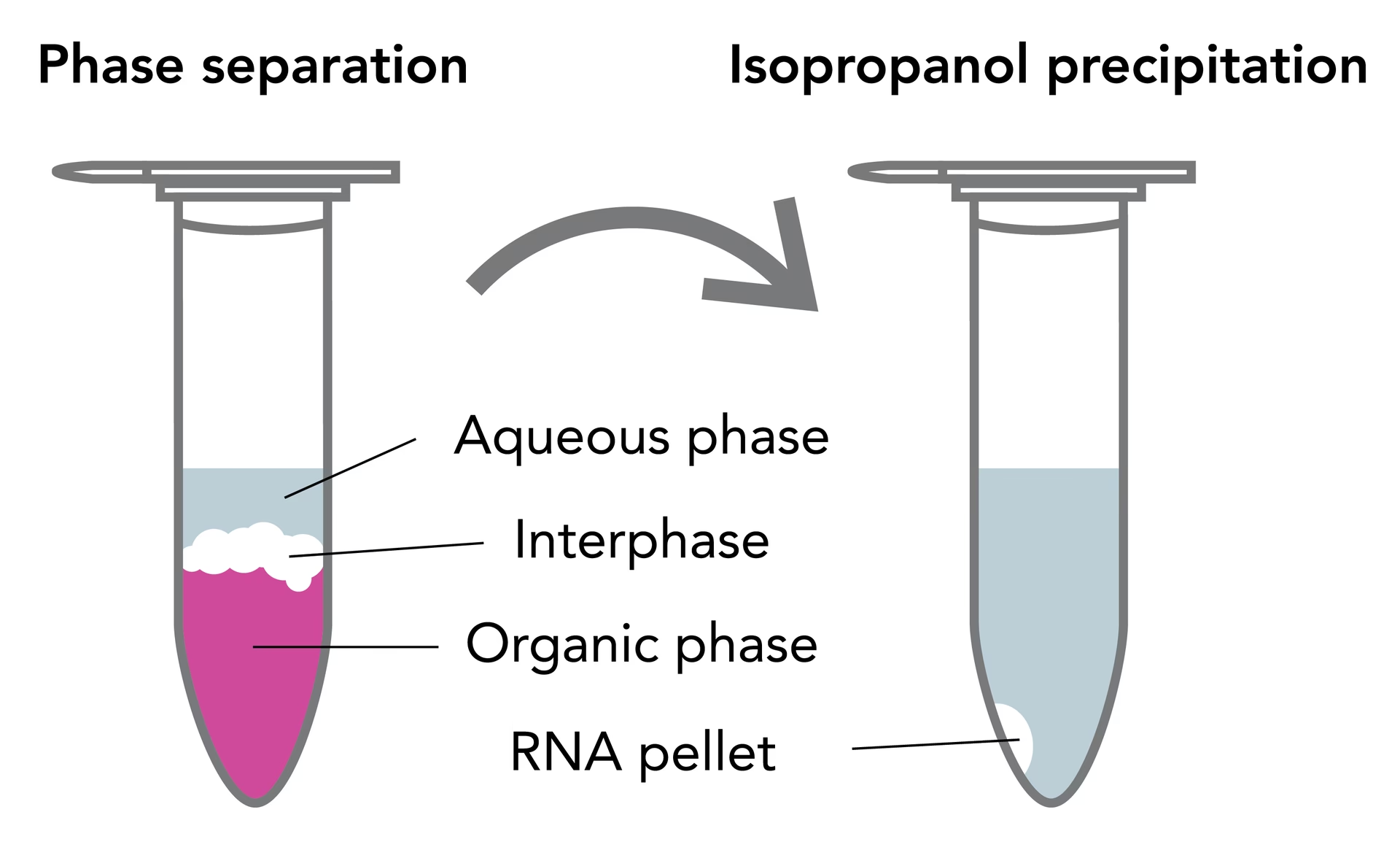
3. Precipitación del ARN
El ARN se precipita de la fase acuosa mediante la adición de isopropanol. Se añade 0.5 mL de isopropanol por cada 1 mL de TRIzol utilizado inicialmente. Se invierte suavemente el tubo varias veces para mezclar y se incuba a temperatura ambiente durante 5-10 minutos. Esta incubación permite que el ARN forme un precipitado. A continuación, se centrifuga a 12,000 x g durante 10 minutos a 4°C. El ARN formará un pellet gelatinoso y translúcido en el fondo del tubo.
4. Lavado del ARN
El pellet de ARN se lava con etanol al 75% para eliminar sales y otras impurezas residuales. Se añade 1 mL de etanol al 75% (por cada 1 mL de TRIzol inicial) y se resuspende suavemente el pellet. Es importante no usar un vórtex de forma vigorosa, ya que podría dispersar el pellet. Se centrifuga de nuevo a 12,000 x g durante 5 minutos a 4°C para volver a sedimentar el ARN. Este paso de lavado puede repetirse para asegurar una máxima pureza.
5. Resuspensión
Se retira con cuidado el sobrenadante de etanol y se deja secar el pellet al aire durante 5-10 minutos. Es crucial no secar en exceso el pellet, ya que esto puede dificultar enormemente su posterior disolución. Finalmente, el pellet de ARN seco se disuelve en 30-60 µL de agua libre de RNasas o en una solución de SDS al 0.5%. Un pipeteo suave y una incubación a 55-60°C durante 10 minutos ayudarán a la solubilización completa del ARN.
Evaluación de la Pureza y el Rendimiento del ARN
Una vez completada la extracción, es imprescindible evaluar la calidad y cantidad del ARN obtenido para asegurar su idoneidad en aplicaciones posteriores. Los métodos más comunes son la espectrofotometría UV y la electroforesis en gel.
Espectrofotometría UV
Se utiliza un espectrofotómetro (como un NanoDrop) para medir la absorbancia de la muestra de ARN a diferentes longitudes de onda.
- Ratio A260/A280: Evalúa la contaminación por proteínas. Los ácidos nucleicos absorben luz a 260 nm, mientras que las proteínas lo hacen a 280 nm. Un ratio ideal para ARN puro se sitúa entre 1.9 y 2.1. Un valor inferior sugiere contaminación residual con proteínas o fenol.
- Ratio A260/A230: Indica contaminación por compuestos orgánicos como sales de guanidinio, fenol o carbohidratos. Para un ARN puro, este ratio debe estar en el rango de 2.0-2.2. Un valor significativamente más bajo apunta a la presencia de estos contaminantes.
| Parámetro | Rango Óptimo | Posible Causa de Desviación |
|---|---|---|
| Ratio A260/A280 | 1.9 - 2.1 | Valores bajos indican contaminación por proteínas o fenol. |
| Ratio A260/A230 | 2.0 - 2.2 | Valores bajos sugieren contaminación por sales de guanidinio u otros solventes. |
Electroforesis en Gel de Agarosa
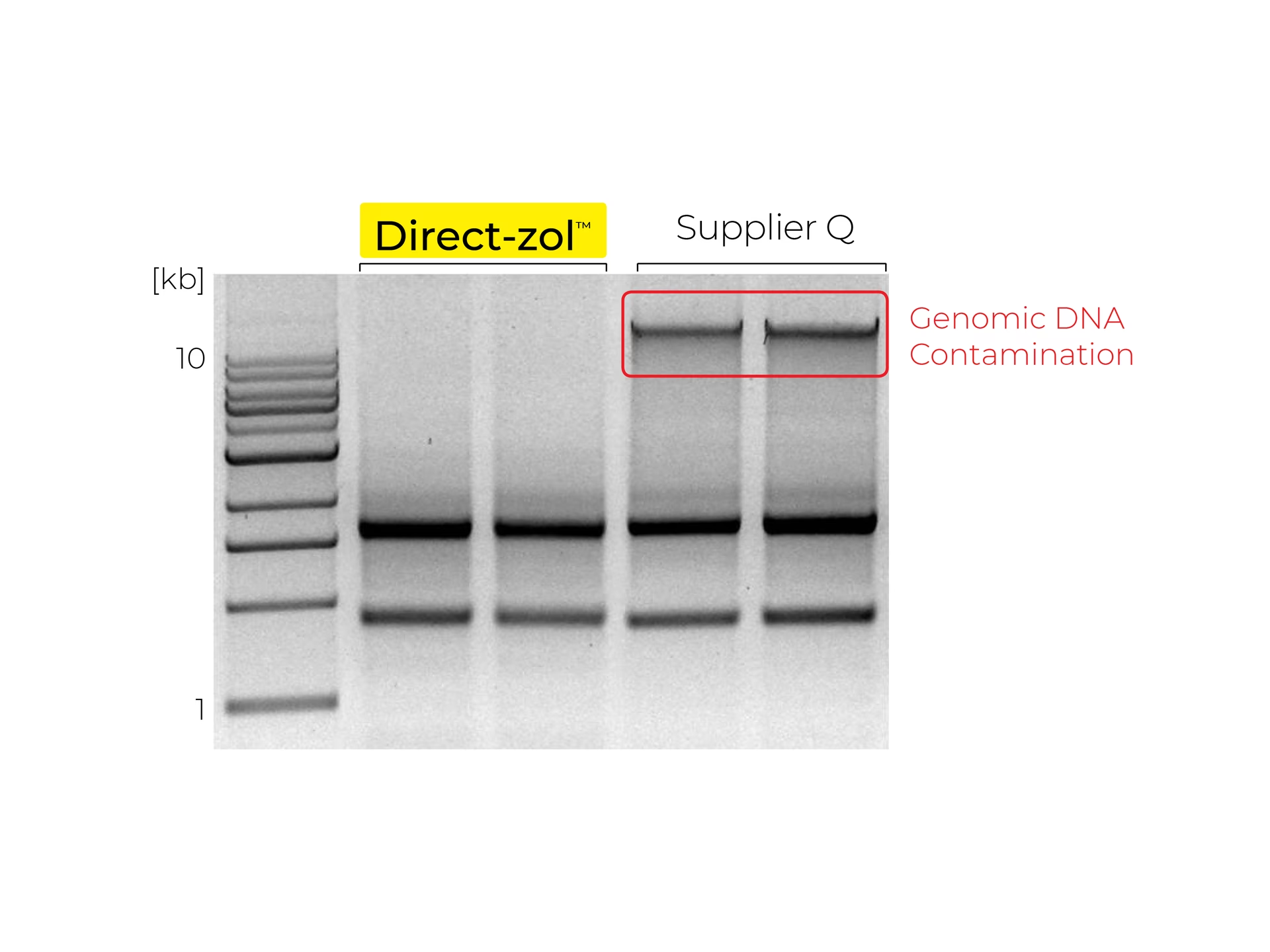
Este método ofrece una evaluación visual de la integridad del ARN. Un ARN total de alta calidad, corrido en un gel de agarosa, mostrará dos bandas nítidas y prominentes correspondientes al ARN ribosómico (ARNr), que en eucariotas son las subunidades 28S y 18S. Un ARN degradado aparecerá como una mancha o "smear" a lo largo del carril, indicando fragmentación. Además, la contaminación con ADN genómico es visible como una banda de alto peso molecular por encima de las bandas de ARNr.
Protocolos de Seguridad y Manejo
El TRIzol y los productos químicos asociados son peligrosos y exigen protocolos de seguridad estrictos. El fenol es corrosivo para la piel y los ojos, y tóxico si se inhala, ingiere o absorbe. El cloroformo también es dañino, considerado carcinogénico y tóxico por inhalación e ingestión. Es obligatorio el uso de Equipo de Protección Personal (EPP), incluyendo bata de laboratorio, guantes resistentes a productos químicos (nitrilo) y gafas de seguridad. Todos los procedimientos deben realizarse en una campana de extracción de gases certificada para evitar la inhalación de vapores peligrosos. La eliminación de residuos debe seguir las normativas para residuos peligrosos.
Problemas Comunes y Soluciones
| Problema | Causa Probable | Solución |
|---|---|---|
| Bajo rendimiento de ARN | Homogeneización incompleta o pérdida del pellet durante los lavados. | Asegurar una lisis completa de la muestra. Manipular con cuidado al decantar el sobrenadante. Usar un portador como glicógeno para visualizar mejor el pellet. |
| Contaminación con ADN genómico | Aspiración de la interfase durante la separación de fases. | Ser muy cuidadoso al recoger la fase acuosa. Realizar un tratamiento con DNasa después de la extracción. |
| Ratios de pureza bajos | Contaminación residual por fenol, proteínas o sales de guanidinio. | Realizar un lavado adicional con etanol al 75% para eliminar impurezas. Asegurarse de no transferir la fase orgánica. |
Preguntas Frecuentes (FAQ)
¿El reactivo TRIzol protege el ARN de la contaminación por RNasas?
Sí. Uno de los componentes principales del TRIzol, el isotiocianato de guanidinio, es un potente desnaturalizante que inactiva eficazmente las RNasas presentes en la muestra biológica, protegiendo así la integridad del ARN desde el primer momento de la lisis celular.
¿Por qué mi pellet de ARN es invisible?
Un pellet de ARN puede ser muy pequeño y translúcido, especialmente si se parte de una cantidad baja de material biológico. Si se sospecha un bajo rendimiento, se puede añadir un portador inerte como el glicógeno durante el paso de precipitación con isopropanol. Esto co-precipitará con el ARN, haciendo el pellet más grande y visible sin interferir en la mayoría de las aplicaciones posteriores.
¿Qué indica un ratio A260/A280 por debajo de 1.8?
Un ratio A260/A280 bajo es un indicador clásico de contaminación por proteínas o fenol. Esto suele ocurrir si parte de la interfase o de la fase orgánica se transfiere junto con la fase acuosa. Realizar un lavado adicional del pellet con etanol al 75% puede ayudar a mejorar este valor.
¿Puedo usar una cabina de bioseguridad en lugar de una campana de extracción de gases?
No. Las cabinas de bioseguridad están diseñadas para proteger la muestra de la contaminación y al usuario de agentes biológicos, pero no ofrecen protección adecuada contra los vapores químicos tóxicos del fenol y el cloroformo. Es imperativo realizar todos los pasos que involucran estos reactivos dentro de una campana de extracción de gases certificada.
Si quieres conocer otros artículos parecidos a Guía Completa para la Extracción de ARN con TRIzol puedes visitar la categoría Ecología.