09/09/2016
En el corazón de la física y la química, y extendiendo su influencia a campos tan diversos como la biología y la ingeniería, se encuentran las leyes de la termodinámica. Estos cuatro principios fundamentales no son meras ecuaciones en una pizarra; son las reglas universales que gobiernan el comportamiento de la energía, el calor, el trabajo y la materia. Comprenderlas es asomarse a la maquinaria más íntima del cosmos, desde el motor de un coche hasta el ciclo de vida de una estrella, y nos proporciona herramientas cruciales para abordar los desafíos energéticos y medioambientales de nuestro tiempo.
¿Qué son exactamente las Leyes de la Termodinámica?
Las leyes de la termodinámica son un conjunto de axiomas científicos que definen cantidades físicas fundamentales (temperatura, energía y entropía) y describen sus interacciones en sistemas físicos. Su validez es tan universal y han sido confirmadas tantas veces experimentalmente que se consideran "leyes" inquebrantables de la naturaleza. Aunque se han propuesto nuevas formulaciones, las cuatro leyes clásicas siguen siendo el pilar sobre el que se construye nuestra comprensión de la energía. Curiosamente, el orden en que las conocemos no corresponde al orden de su descubrimiento; la Ley Cero fue la última en ser formulada, pero su naturaleza fundamental le otorgó el primer lugar.
La Ley Cero: El Fundamento del Equilibrio Térmico
La Ley Cero puede parecer obvia, pero su simplicidad esconde un concepto revolucionario que permite toda la ciencia de la medición de la temperatura. Establece que: “Si dos sistemas están por separado en equilibrio térmico con un tercer sistema, entonces también están en equilibrio térmico entre sí”.
Pensemos en ello de esta manera: si tienes una taza de café (sistema A) y un termómetro (sistema C) marca 80°C, y luego usas el mismo termómetro para medir una sopa (sistema B) y también marca 80°C, puedes concluir sin que la taza y la sopa se toquen, que ambas están a la misma temperatura. Este principio es la razón por la que los termómetros funcionan y por la que el concepto de temperatura es universal y medible. El equilibrio térmico es ese estado en el que no hay un flujo neto de calor entre dos objetos en contacto.
La Primera Ley: La Conservación de la Energía
A menudo resumida en la famosa frase “la energía no se crea ni se destruye, solo se transforma”, la primera ley es una declaración del principio de conservación de la energía. Dicta que la energía total de un sistema aislado permanece constante. La energía puede cambiar de forma —de química a térmica, de térmica a mecánica— pero la cantidad total nunca varía.
La expresión matemática que encapsula esta ley es:
ΔU = Q - W
Donde:
- ΔU es el cambio en la energía interna del sistema (la suma de la energía de todas sus partículas).
- Q es el calor añadido al sistema desde su entorno.
- W es el trabajo realizado por el sistema sobre su entorno.
Esta ecuación nos dice que si añadimos calor a un sistema (como calentar un gas en un pistón), su energía interna aumentará. Si el sistema realiza un trabajo (el gas se expande y mueve el pistón), su energía interna disminuirá. Todo cambio energético debe estar perfectamente balanceado. Esta ley es la base para entender la eficiencia energética: ya que la energía no puede crearse, nuestro objetivo es maximizar la transformación a la forma útil (trabajo) y minimizar la pérdida en formas no deseadas (calor disipado).
La Segunda Ley: La Flecha del Tiempo y el Aumento de la Entropía
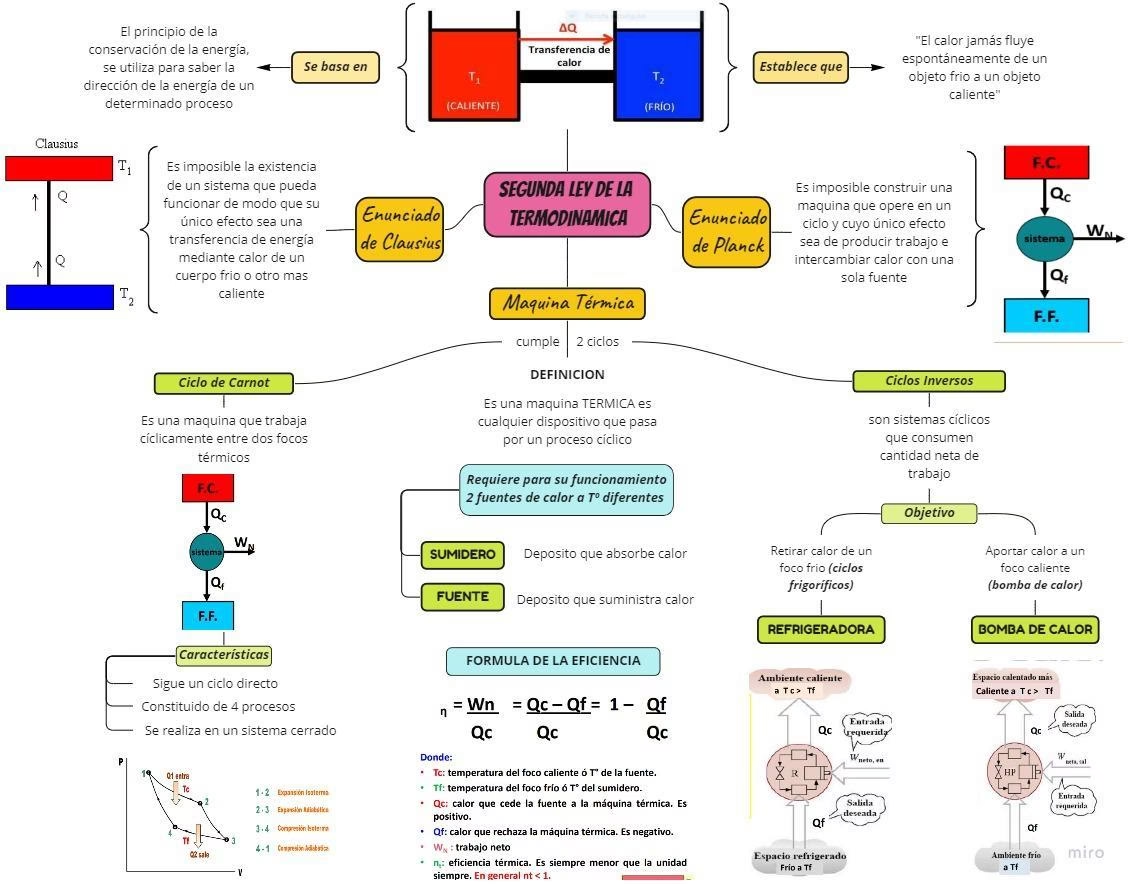
Si la primera ley nos dice que la energía se conserva, la segunda ley nos dice en qué dirección ocurren los procesos naturales. Es, quizás, la más profunda y con mayores implicaciones filosóficas. Establece que “la cantidad de entropía del universo tiende a incrementarse con el tiempo”.
La entropía es una medida del desorden, la aleatoriedad o la dispersión de la energía en un sistema. La segunda ley nos dice que los sistemas tienden naturalmente a evolucionar desde estados de orden hacia estados de mayor desorden. Este principio explica fenómenos cotidianos:
- El calor siempre fluye espontáneamente de un cuerpo caliente a uno frío, nunca al revés.
- Un cubito de hielo en una bebida caliente se derrite, dispersando su frío (absorbiendo calor), pero la bebida nunca volverá a formar el cubito de hielo por sí sola.
- El humo de una chimenea se dispersa en el aire, pero nunca se volverá a concentrar para entrar de nuevo por la chimenea.
Esta ley impone un límite fundamental a la eficiencia de cualquier máquina térmica. Es imposible construir un motor que convierta el 100% del calor en trabajo útil; siempre habrá una parte de la energía que se disipará como calor residual, aumentando la entropía del entorno. Esta es la razón por la que los motores se calientan y por la que la eficiencia energética es una batalla constante contra el desorden.
La Tercera Ley: La Búsqueda Inalcanzable del Cero Absoluto
La tercera y última ley se adentra en los límites del frío. Establece que “es imposible alcanzar la temperatura del cero absoluto mediante un número finito de procesos”. El cero absoluto (0 Kelvin, o -273.15 °C) es la temperatura teóricamente más baja posible, un estado en el que las partículas de un sistema tendrían la mínima energía posible y cesaría todo movimiento térmico.

Según esta ley, a medida que un sistema se acerca al cero absoluto, su entropía se aproxima a un valor mínimo constante. Podemos acercarnos increíblemente a esta temperatura en laboratorios, pero nunca alcanzarla por completo. Cada paso que damos para enfriar un sistema se vuelve progresivamente más difícil, requiriendo cada vez más trabajo para extraer una cantidad cada vez menor de calor. Esta ley es fundamental para campos como la criogenia y ha permitido el descubrimiento de fenómenos cuánticos como la superconductividad y la superfluidez, que ocurren a temperaturas extremadamente bajas.
Tabla Comparativa de las Leyes de la Termodinámica
| Ley | Principio Fundamental | Concepto Clave | Implicación Principal |
|---|---|---|---|
| Ley Cero | Si A=C y B=C, entonces A=B. | Equilibrio térmico | Permite la definición y medición universal de la temperatura. |
| Primera Ley | La energía no se crea ni se destruye. | Conservación de la energía | La energía total de un sistema aislado es constante. |
| Segunda Ley | El desorden del universo siempre aumenta. | Entropía | Define la dirección de los procesos naturales (la "flecha del tiempo") y limita la eficiencia de las máquinas. |
| Tercera Ley | Es imposible alcanzar el cero absoluto. | Cero absoluto | La entropía de un sistema se acerca a un mínimo constante a 0 K. |
Preguntas Frecuentes sobre las Leyes de la Termodinámica
¿Por qué se llama "Ley Cero" si se formuló después de las otras?
Aunque la primera y segunda ley ya estaban bien establecidas, los científicos se dieron cuenta de que necesitaban un principio más básico para justificar lógicamente el concepto de temperatura. Como este principio era más fundamental que los otros dos, se decidió llamarlo "Ley Cero" para darle la precedencia conceptual que merecía.
¿Cómo se relacionan estas leyes con la ecología y la sostenibilidad?
La relación es directa y profunda. La primera ley nos recuerda que no podemos crear energía de la nada; solo podemos aprovechar las fuentes existentes (solar, eólica, fósil). La segunda ley es aún más crítica: nos enseña que en cada conversión energética (por ejemplo, de carbón a electricidad) una parte de la energía se degrada inevitablemente en forma de calor no aprovechable, aumentando la entropía. Esto subraya la importancia vital de la eficiencia energética. Un uso más eficiente de la energía significa menos recursos consumidos y menos calor residual (contaminación térmica) liberado al medio ambiente para lograr el mismo trabajo útil.
¿La segunda ley significa que el universo está condenado al desorden total?
Esa es la idea detrás de la teoría de la "muerte térmica del universo". Si la entropía sigue aumentando indefinidamente, el universo podría alcanzar un estado de máximo desorden y equilibrio térmico total. En este escenario, toda la energía estaría distribuida de manera uniforme, no habría gradientes de temperatura y, por lo tanto, no sería posible realizar trabajo. Sería un universo estático y sin vida. Sin embargo, esto es solo una hipótesis cosmológica y existen otras teorías sobre el destino final del universo.
¿Es posible crear orden y disminuir la entropía?
Sí, pero solo a nivel local y a costa de aumentar la entropía en otro lugar. Un ser vivo, por ejemplo, es un sistema increíblemente ordenado. Mantiene su estructura (baja entropía) consumiendo energía (alimentos) y liberando calor y desechos (alta entropía) a su entorno. Un refrigerador crea un espacio ordenado y frío en su interior, pero lo hace expulsando una cantidad mayor de calor por su parte trasera, aumentando la entropía total de la habitación. El balance global siempre se inclina hacia un aumento neto de la entropía en el universo.
Si quieres conocer otros artículos parecidos a Leyes de la Termodinámica: Guía Esencial puedes visitar la categoría Ecología.
