13/01/2015
El pH es uno de los parámetros más fundamentales y universalmente medidos en el campo de la ciencia ambiental. Representa la medida de la acidez o alcalinidad de una solución, expresada en una escala logarítmica del 0 al 14. Un valor de 7 se considera neutro, por debajo de 7 indica acidez y por encima de 7, alcalinidad. Esta simple cifra, sin embargo, encierra una enorme cantidad de información sobre el estado químico de un sistema, ya sea un lago, una parcela de cultivo o un proceso industrial. Comprender cómo medirlo correctamente es, por tanto, una habilidad esencial para cualquier profesional dedicado al cuidado y la gestión de nuestros recursos naturales.
¿Por Qué es Tan Importante la Medición del pH?
La relevancia del pH trasciende el laboratorio; sus efectos se sienten en todos los aspectos de nuestro entorno. Una variación, por pequeña que parezca, puede desencadenar consecuencias significativas.
- En Ecosistemas Acuáticos: El pH del agua es un indicador vital de su salud. La mayoría de los organismos acuáticos, desde los peces hasta las algas microscópicas, prosperan en un rango de pH muy específico, generalmente cercano a la neutralidad. La lluvia ácida, la contaminación industrial o las descargas de aguas residuales pueden alterar drásticamente este equilibrio, afectando la vida acuática y la potabilidad del agua para el consumo humano.
- En la Agricultura y Suelos: El pH del suelo controla directamente la disponibilidad de nutrientes esenciales para las plantas. Un suelo demasiado ácido o alcalino puede "bloquear" nutrientes como el fósforo o el hierro, impidiendo que las raíces los absorban, incluso si están presentes en grandes cantidades. Medir y corregir el pH es una práctica agrícola clave para garantizar cosechas saludables y productivas.
- En la Industria: Desde la fabricación de alimentos y bebidas hasta la producción farmacéutica, el control del pH es crucial. Garantiza la estabilidad de los productos, la eficacia de las reacciones químicas y la seguridad de los procesos. Por ejemplo, en las plantas de tratamiento de aguas residuales, el ajuste del pH es un paso indispensable para la eliminación de contaminantes.
Métodos Esenciales para la Medición del pH
Para determinar el pH de una muestra, existen diversas técnicas que varían en precisión, coste y complejidad. La elección del método adecuado dependerá del objetivo de la medición, el entorno y la exactitud requerida. A continuación, exploramos los tres enfoques principales utilizados en laboratorios ambientales.
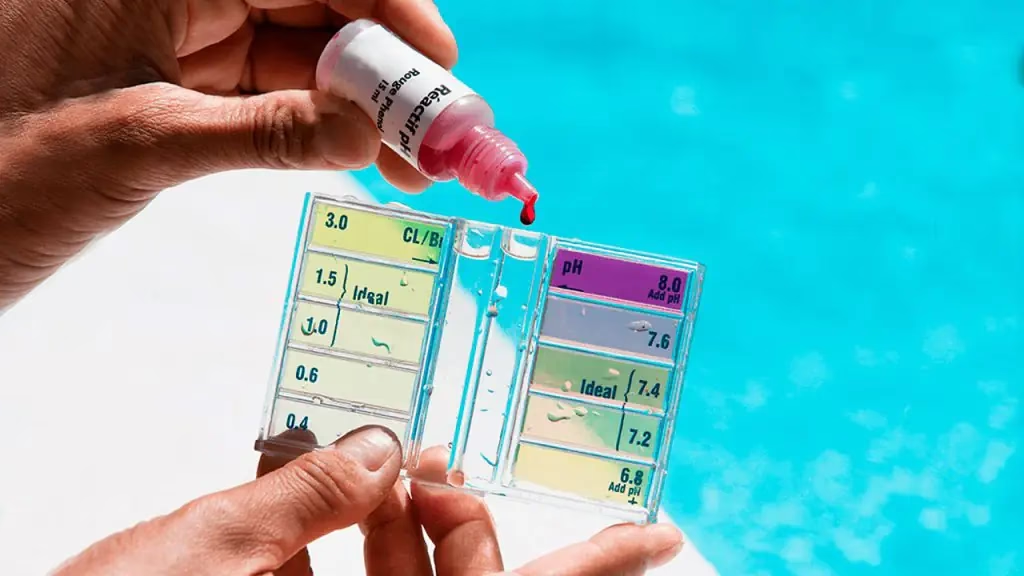
1. Indicadores Colorimétricos: La Solución Rápida y Sencilla
Los indicadores colorimétricos son la forma más básica y accesible de medir el pH. Se trata de sustancias químicas orgánicas que cambian de color en función del nivel de acidez o alcalinidad del medio. Se presentan comúnmente en dos formatos:
- Tiras de Papel pH (Papel Tornasol): Son pequeñas tiras de papel impregnadas con uno o varios indicadores. Al sumergir la tira en la muestra, esta cambia de color. Luego, se compara el color resultante con una escala de referencia provista en el empaque para obtener una lectura aproximada del pH.
- Soluciones Indicadoras: Son líquidos que se añaden en pequeñas gotas a la muestra. La solución entera cambia de color, indicando el rango de pH.
Aplicaciones y Limitaciones:
Estos indicadores son ideales para mediciones rápidas en campo, actividades educativas o para tener una idea preliminar del estado de una muestra. Su bajo costo y facilidad de uso los hacen muy populares. Sin embargo, su precisión es muy limitada (generalmente con un error de ±1 unidad de pH), y la lectura puede ser subjetiva y verse afectada por el color o la turbidez natural de la muestra. Por ello, no son adecuados para análisis que requieran datos exactos y trazables, como los exigidos por normativas ambientales.
2. Electrodos Potenciométricos (pH-metros): El Estándar de Precisión
El método potenciométrico es el estándar de oro en la medición de pH en laboratorios y aplicaciones profesionales. Se basa en el uso de un medidor de pH, también conocido como pH-metro o potenciómetro.

¿Cómo funciona?
Este dispositivo utiliza un electrodo combinado, que consta de un electrodo de vidrio sensible a los iones de hidrógeno (H⁺) y un electrodo de referencia. Al sumergirlo en la muestra, se genera una pequeña diferencia de voltaje entre ambos electrodos. Esta diferencia de potencial es directamente proporcional a la concentración de iones H⁺, según la ecuación de Nernst. El medidor convierte este voltaje en una lectura digital de pH, ofreciendo resultados rápidos y de alta precisión.
Componentes y Procedimiento:
Un sistema de medición típico incluye el medidor (consola digital), el electrodo, y soluciones tampón (buffers) para la calibración. El procedimiento correcto es clave para obtener resultados fiables:
- Calibración: Antes de medir, el equipo debe ser calibrado usando al menos dos soluciones buffer de pH conocido y estable (ej. pH 4.01, 7.00 y 10.01). Esto ajusta la respuesta del electrodo.
- Enjuague: El electrodo se enjuaga con agua destilada o desionizada y se seca suavemente antes y después de cada medición para evitar la contaminación cruzada.
- Medición: Se introduce el electrodo en la muestra, se agita ligeramente y se espera a que la lectura en la pantalla se estabilice. Los medidores modernos suelen tener un indicador de estabilidad.
- Almacenamiento: Tras su uso, el electrodo se limpia y se guarda en una solución de almacenamiento específica para mantenerlo hidratado y en óptimas condiciones.
Ventajas:
La principal ventaja es su alta precisión (típicamente ±0.01 unidades de pH). Además, puede usarse en una amplia variedad de muestras, incluyendo líquidos turbios, coloreados e incluso semisólidos (con electrodos especiales). En México, su uso es indispensable para cumplir con Normas Oficiales Mexicanas como la NOM-001-SEMARNAT-2021 (descargas de aguas residuales) y la NOM-127-SSA1-2021 (agua para uso y consumo humano).
3. Técnicas Espectrofotométricas: Alta Sensibilidad para Casos Complejos
La espectrofotometría es un método instrumental más avanzado que también se basa en el cambio de color de un indicador, pero elimina la subjetividad de la observación humana.
Principio de Funcionamiento:
Se añade un reactivo indicador a la muestra, que cambia de color según el pH. Luego, se introduce la muestra en un espectrofotómetro. Este equipo emite un haz de luz a una longitud de onda específica a través de la solución y mide cuánta luz es absorbida. La absorbancia está directamente relacionada con la concentración del indicador en su forma ácida o básica, lo que permite calcular el pH con gran precisión mediante una curva de calibración previamente establecida.

Aplicaciones:
Este método es particularmente útil para analizar matrices complejas, como aguas residuales industriales muy coloreadas o con presencia de aceites, donde un electrodo potenciométrico podría contaminarse o dar lecturas erróneas. También es ideal para análisis que requieren alta reproducibilidad o el uso de volúmenes de muestra muy pequeños, comunes en investigación bioquímica o microbiológica.
Tabla Comparativa de Métodos de Medición de pH
| Característica | Indicadores Colorimétricos | pH-metro (Potenciométrico) | Espectrofotometría |
|---|---|---|---|
| Precisión | Baja (±0.5 a ±1.0) | Muy Alta (±0.01 a ±0.05) | Alta a Muy Alta |
| Costo | Muy Bajo | Medio a Alto | Alto |
| Portabilidad | Excelente | Buena (existen modelos portátiles) | Baja (equipo de laboratorio) |
| Uso Ideal | Educación, monitoreo rápido, sondeos preliminares. | Laboratorios, control de calidad, cumplimiento de normativas, investigación. | Muestras complejas/coloreadas, investigación, microanálisis. |
Preguntas Frecuentes (FAQ)
¿Cuál es la influencia de la temperatura en las mediciones de pH?
La temperatura es un factor crítico que afecta la medición del pH de dos maneras principales. Primero, influye en la respuesta del propio electrodo; la pendiente de la relación entre el voltaje y el pH cambia con la temperatura. Para corregir esto, los pH-metros modernos incorporan una sonda de temperatura y aplican una Compensación Automática de Temperatura (ATC). Segundo, y más importante, el pH real de la solución cambia con la temperatura. La ATC solo corrige el comportamiento del electrodo, no el cambio real en la química de la muestra. Por ello, es fundamental registrar siempre la temperatura junto con el valor de pH para que la medición sea comparable y reproducible.
¿Con qué frecuencia se debe calibrar un pH-metro?
La frecuencia de calibración depende de la frecuencia de uso y la precisión requerida. Para mediciones críticas o de cumplimiento normativo, se recomienda calibrar el medidor diariamente, o incluso antes de cada tanda de mediciones. Para un uso menos frecuente o menos crítico, una calibración semanal puede ser suficiente. Siempre se debe recalibrar si se sospecha de lecturas incorrectas, después de cambiar el electrodo o tras medir muestras agresivas (muy ácidas, muy alcalinas o con disolventes orgánicos).
Conclusión
La medición del pH es una herramienta de diagnóstico indispensable para la gestión ambiental. La elección del método correcto, desde las sencillas tiras colorimétricas para una evaluación rápida hasta los precisos pH-metros para el cumplimiento normativo y la investigación, es fundamental para obtener datos fiables. Dominar estas técnicas y comprender sus principios y limitaciones permite a los profesionales del medio ambiente tomar decisiones informadas, proteger la salud de nuestros ecosistemas y garantizar la sostenibilidad de nuestros recursos para las futuras generaciones.
Si quieres conocer otros artículos parecidos a Guía Completa para Medir el pH Ambiental puedes visitar la categoría Medioambiente.
