18/04/2004
La enfermedad de Parkinson es uno de los trastornos neurodegenerativos más conocidos y desafiantes de nuestro tiempo. Afecta a millones de personas en todo el mundo, comprometiendo su capacidad motora y calidad de vida. Si bien sus síntomas, como los temblores y la rigidez, son visibles externamente, la verdadera batalla se libra en un escenario invisible al ojo humano: el interior de nuestras neuronas. Comprender los mecanismos moleculares que subyacen a esta enfermedad es fundamental, no solo para quienes la padecen, sino para desarrollar estrategias terapéuticas que puedan, algún día, detener su avance. La investigación actual nos sumerge en un complejo universo de proteínas, orgánulos y procesos de señalización que, cuando fallan, inician una cascada de eventos destructivos. Este artículo profundiza en esas causas, distinguiendo entre las formas familiares y esporádicas de la enfermedad y explorando los descubrimientos más recientes sobre el daño celular que la caracteriza.
- Parkinson Familiar vs. Esporádico: Dos Caminos hacia un Mismo Destino
- El Epicentro del Problema: Daño Mitocondrial
- La Danza Molecular: Parkin, Mitofusina y la Ubiquitinización
- Cuando el Equilibrio se Rompe: Las Consecuencias Celulares
- En Busca de una Solución: Las Enzimas de Desubiquitinización
- Preguntas Frecuentes (FAQ) sobre la Enfermedad de Parkinson
Parkinson Familiar vs. Esporádico: Dos Caminos hacia un Mismo Destino
Aunque los síntomas pueden ser muy similares, la enfermedad de Parkinson no tiene un único origen. Se clasifica principalmente en dos grandes grupos: familiar y esporádico. La distinción entre ambos es crucial para la investigación y el diagnóstico.
- Enfermedad de Parkinson Familiar: Como su nombre indica, esta forma tiene un componente genético claro. Se debe a mutaciones en genes específicos (como el gen de la α-sinucleína o el de la Parkina) que se heredan de padres a hijos. Aunque representa solo un pequeño porcentaje del total de casos (alrededor del 5-10%), su estudio ha sido invaluable. Las familias con múltiples miembros afectados han permitido a los científicos identificar los genes responsables y, a través de ellos, descifrar las vías moleculares que se ven alteradas. Suele presentarse a una edad más temprana que la forma esporádica.
- Enfermedad de Parkinson Esporádica: Esta es la forma más común, representando el 90-95% de todos los diagnósticos. Se considera "esporádica" porque no parece haber una causa genética directa o un patrón de herencia familiar claro. Se cree que su origen es multifactorial, una compleja interacción entre una predisposición genética sutil y factores ambientales a lo largo de la vida de una persona. La edad avanzada es el principal factor de riesgo, pero la exposición a ciertos pesticidas, toxinas o traumatismos craneales también se ha asociado con un mayor riesgo.
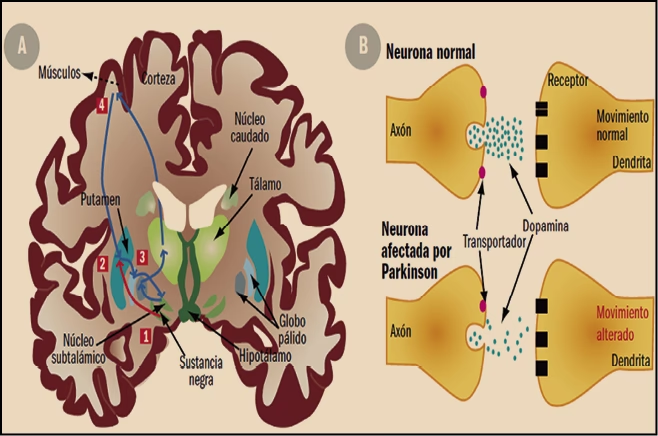
A pesar de sus diferentes puntos de partida, ambas formas convergen en un punto común: la muerte progresiva de las neuronas productoras de dopamina en una región del cerebro llamada sustancia nigra. Es esta pérdida celular la que provoca los conocidos síntomas motores de la enfermedad.
Tabla Comparativa: Parkinson Familiar vs. Esporádico
| Característica | Parkinson Familiar | Parkinson Esporádico |
|---|---|---|
| Prevalencia | 5-10% de los casos | 90-95% de los casos |
| Causa Principal | Mutaciones genéticas hereditarias específicas | Combinación de factores genéticos y ambientales |
| Edad de Inicio | Generalmente más temprana (antes de los 50 años) | Generalmente más tardía (después de los 60 años) |
| Patrón de Herencia | Claro, sigue patrones mendelianos | No hay un patrón de herencia claro |
El Epicentro del Problema: Daño Mitocondrial
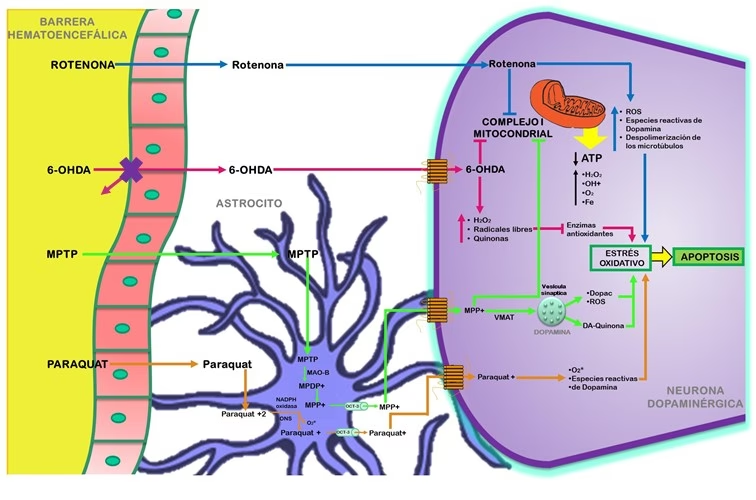
Una de las características distintivas que une tanto a la forma familiar como a la esporádica es la acumulación de daño en las mitocondrias. Las mitocondrias son los orgánulos encargados de producir energía para la célula; son sus "centrales eléctricas". Las neuronas, especialmente las de la sustancia nigra, tienen una demanda energética altísima para mantener su función y supervivencia. Cuando las mitocondrias fallan, la célula entra en una crisis energética que, sumada a otros factores de estrés, la conduce a la muerte.
Este fallo mitocondrial a menudo se asocia con un aumento del "estrés oxidativo". Durante la producción de energía, se generan subproductos tóxicos llamados radicales libres. Las mitocondrias sanas tienen sistemas para neutralizarlos, pero cuando están dañadas, esta producción se descontrola. En la sustancia nigra de pacientes con Parkinson, se detectan marcadores de este daño, como niveles elevados de malondialdehído, que indican que las defensas antioxidantes de la célula han sido superadas.
La Danza Molecular: Parkin, Mitofusina y la Ubiquitinización
Para entender cómo se daña la mitocondria, debemos adentrarnos en un proceso celular fundamental: la ubiquitinización. Imagina que es un sistema de etiquetado. Una pequeña proteína llamada ubiquitina se une a otras proteínas como si fuera una etiqueta de "correo". Esta etiqueta puede significar muchas cosas: "destruir esta proteína", "mover esta proteína a otro lugar" o "cambiar la función de esta proteína".
Aquí es donde entra en juego la proteína Parkin, cuyo gen está mutado en algunas formas de Parkinson familiar. Parkin es una enzima que actúa como el "etiquetador": su trabajo es colocar etiquetas de ubiquitina sobre otras proteínas. Uno de sus objetivos clave es una proteína llamada Mitofusina.
La Mitofusina es fascinante porque se encuentra en la superficie de dos orgánulos distintos: las mitocondrias y el retículo endoplasmático (RE), que es la fábrica de proteínas de la célula. La Mitofusina actúa como un puente o un ancla, manteniendo unidas físicamente a la mitocondria y al RE. Esta conexión es vital para la comunicación y el intercambio de moléculas entre ambos, especialmente el calcio (Ca2+).
El proyecto MITOFUSIN-PD, financiado por la Unión Europea, arrojó luz sobre este proceso. Descubrieron que Parkin ubiquitina (etiqueta) a la Mitofusina, regulando así la fuerza y duración de la conexión entre la mitocondria y el RE. Es un mecanismo de control exquisito.
Cuando el Equilibrio se Rompe: Las Consecuencias Celulares
¿Qué ocurre cuando Parkin no funciona correctamente, como sucede en los pacientes con mutaciones en este gen? La investigación reveló que en células deficientes de Parkin, el etiquetado de la Mitofusina falla. Como resultado:
- Disminuye la interacción física: La conexión entre la mitocondria y el RE se debilita. Los puentes que las mantenían unidas se vuelven menos estables.
- Falla la transferencia de calcio: El calcio es un mensajero celular vital. Su transferencia eficiente del RE (un gran almacén de calcio) a la mitocondria es crucial para la producción de energía y otras funciones. Con la conexión debilitada, esta transferencia se ve gravemente afectada.
- Se altera la señalización celular: Un manejo incorrecto del calcio desencadena una cascada de problemas. Afecta directamente al RE, que no puede procesar, plegar y exportar correctamente las proteínas que sintetiza. Esto genera un "atasco" de proteínas mal plegadas, una condición de estrés celular que es altamente tóxica para la neurona.
En resumen, la falla de una sola enzima (Parkin) provoca un efecto dominó que debilita la comunicación entre orgánulos, desata una crisis energética y de manejo de proteínas, y finalmente empuja a la célula hacia la autodestrucción. Este mecanismo proporciona una explicación molecular detallada de por qué las mutaciones en Parkin conducen a la neurodegeneración.
En Busca de una Solución: Las Enzimas de Desubiquitinización
Si la ubiquitinización es el acto de "poner la etiqueta", debe existir un proceso contrario para "quitarla". Este proceso se llama desubiquitinización y es llevado a cabo por una familia de enzimas conocidas como DUBs (Deubiquitinating enzymes). El equilibrio entre la acción de Parkin (poner la etiqueta) y la de una DUB (quitarla) es lo que ajusta finamente la conexión mitocondria-RE.
Los investigadores se propusieron identificar qué DUBs actuaban sobre la Mitofusina. Analizando una biblioteca de estas enzimas, encontraron cinco candidatas prometedoras. Una de ellas, la enzima Usp8, destacó particularmente. Descubrieron que reducir los niveles de Usp8 llevaba a una disminución de la proteína Mitofusina y promovía la fisión mitocondrial (un proceso de división de las mitocondrias que es importante para el control de calidad celular).

Este hallazgo es tremendamente emocionante desde una perspectiva terapéutica. Las DUBs se están convirtiendo en dianas farmacológicas muy atractivas. De hecho, ya existen inhibidores de DUBs en ensayos clínicos para el tratamiento del cáncer. La idea es que, de manera similar, se podrían desarrollar fármacos que inhiban o promuevan la actividad de DUBs específicas para restaurar el equilibrio perdido en las neuronas de pacientes con Parkinson. Podría ser una vía completamente nueva para proteger las células y frenar el avance de la enfermedad.
Preguntas Frecuentes (FAQ) sobre la Enfermedad de Parkinson
¿La enfermedad de Parkinson es puramente genética?
No. Solo un 5-10% de los casos (Parkinson familiar) se deben a mutaciones genéticas hereditarias directas. La gran mayoría (Parkinson esporádico) se considera el resultado de una interacción compleja entre una predisposición genética y factores ambientales y de estilo de vida a lo largo del tiempo.
¿Qué es el estrés oxidativo y qué papel juega?
El estrés oxidativo es un desequilibrio celular causado por un exceso de moléculas reactivas (radicales libres) y una capacidad insuficiente de la célula para neutralizarlas. En el Parkinson, las mitocondrias dañadas producen más radicales libres y tienen menos capacidad para defenderse, lo que daña componentes celulares vitales como lípidos, proteínas y ADN, contribuyendo a la muerte neuronal.
¿La acumulación de α-sinucleína está relacionada con el daño mitocondrial?
Sí, están íntimamente relacionados. La acumulación y agregación de la proteína α-sinucleína (formando los Cuerpos de Lewy, otra característica de la enfermedad) puede dañar directamente las mitocondrias. A su vez, las mitocondrias disfuncionales pueden perjudicar la capacidad de la célula para eliminar estas acumulaciones de proteínas, creando un círculo vicioso de toxicidad.
¿Existen tratamientos que apunten a estos mecanismos moleculares?
Actualmente, los tratamientos para el Parkinson se centran en manejar los síntomas, principalmente reemplazando la dopamina que falta en el cerebro. Sin embargo, la investigación descrita en este artículo es la base para el desarrollo de futuras terapias neuroprotectoras. Los fármacos que modulen la ubiquitinización, mejoren la función mitocondrial o reduzcan el estrés oxidativo son el santo grial de la investigación actual y ofrecen la esperanza de poder ralentizar o detener la progresión de la enfermedad en el futuro.
Si quieres conocer otros artículos parecidos a Parkinson: El Baile Molecular Dentro de tus Células puedes visitar la categoría Ecología.
