22/08/2022
En el corazón de la biología molecular y los diagnósticos médicos que han sido cruciales durante crisis sanitarias globales, como la pandemia de COVID-19, se encuentra un proceso fundamental: la extracción de ARN. Este procedimiento nos permite estudiar los virus, entender enfermedades y desarrollar vacunas. Sin embargo, detrás de este avance científico se esconde una realidad menos conocida y mucho más preocupante: el uso de productos químicos altamente tóxicos que representan un serio desafío para el medio ambiente. Dos de los protagonistas de este dilema son el tiocianato de guanidina y el fenol, componentes esenciales del método estándar para aislar ARN, pero cuyo manejo y desecho exigen una profunda reflexión ecológica.
¿Qué son el Tiocianato de Guanidina y el Fenol? El Dúo Potente pero Peligroso
Para entender el problema, primero debemos conocer a los actores. La extracción de ARN de una célula es como intentar sacar un hilo de seda frágil de una bola de lana enredada y pegajosa, todo mientras unas tijeras (enzimas llamadas RNasas) intentan cortarlo en pedazos. Aquí es donde intervienen nuestros dos químicos.
- Tiocianato de Guanidina: Es una sal caotrópica. Imagínalo como un agente de demolición molecular. Su función es desintegrar las estructuras de las proteínas y, lo más importante, desactivar por completo a las RNasas, esas enzimas destructoras que degradan el ARN. Al romper todo lo que podría dañar el ARN, preserva su integridad para el análisis posterior.
- Fenol: Juega un papel completamente diferente. El fenol es un compuesto orgánico no polar, lo que significa que no se mezcla bien con el agua o las moléculas polares como el ARN. Su trabajo es separar. Cuando se añade a la mezcla celular, actúa como el aceite en un aderezo de ensalada: separa los componentes solubles en agua (el ARN y el ADN) de los componentes grasos o no polares (lípidos y proteínas).
Juntos, forman la base de reactivos como el popular TRIzol o RNA-Bee, que lisan (rompen) las células y comienzan el delicado proceso de purificación.
El Proceso de Extracción: Un Baile Químico en Tres Fases
El método clásico, conocido como el método de fenol-cloroformo, es un procedimiento meticuloso. Una vez que las células se disuelven en la solución de tiocianato de guanidina y fenol, se añade cloroformo. El cloroformo, al ser más denso, ayuda a que la separación sea aún más nítida. La mezcla se centrifuga a alta velocidad, lo que la obliga a separarse en tres capas distintas, similar a cómo se asentarían el aceite, el vinagre y la miel si se agitaran juntos en una botella.
Las capas resultantes son:
- Fase Acuosa (superior): Es la capa más ligera y contiene lo que nos interesa: el ARN puro. Al ser polar, el ARN se queda en la fase a base de agua.
- Interfase (media): Una capa blanquecina y delgada donde se acumula el ADN y algunas proteínas.
- Fase Orgánica (inferior): La capa más densa, compuesta por fenol, cloroformo, lípidos y las proteínas desnaturalizadas. Es, en esencia, el "desecho" celular.
El científico recoge con cuidado la fase acuosa superior, precipita el ARN con alcohol (isopropanol) para solidificarlo en un pequeño pellet, y luego lo lava con etanol para eliminar sales e impurezas. Finalmente, el ARN purificado se disuelve en agua libre de RNasas, listo para su uso. Aunque efectivo, cada paso que involucra fenol y guanidina genera residuos peligrosos.
La Cara Oculta: Toxicidad y Riesgo Ambiental
Aquí es donde el ecologismo entra en escena. El fenol es corrosivo, tóxico por ingestión, inhalación o contacto con la piel, y perjudicial para la vida acuática. El tiocianato de guanidina, aunque es el héroe en la preservación del ARN, es igualmente dañino. Es nocivo si se ingiere y, en contacto con ácidos, libera gases muy tóxicos. La gestión de los residuos líquidos que contienen estos compuestos es una pesadilla para los laboratorios.
Estos desechos no pueden verterse por el desagüe. Deben ser recolectados en contenedores especiales, etiquetados como residuos peligrosos y gestionados por empresas especializadas en su tratamiento, lo que implica un costo económico y una huella de carbono considerable. En análisis masivos, como los realizados durante una pandemia, la cantidad de residuos tóxicos generados se multiplica exponencialmente, creando un problema ambiental a gran escala. La necesidad de un método rápido, simple y, sobre todo, seguro para el medio ambiente es más urgente que nunca.

La Búsqueda de Alternativas Más Verdes
Afortunadamente, la comunidad científica es consciente de este problema y ha estado desarrollando alternativas más seguras y sostenibles. Estos nuevos métodos buscan reducir o eliminar el uso de los reactivos más peligrosos.
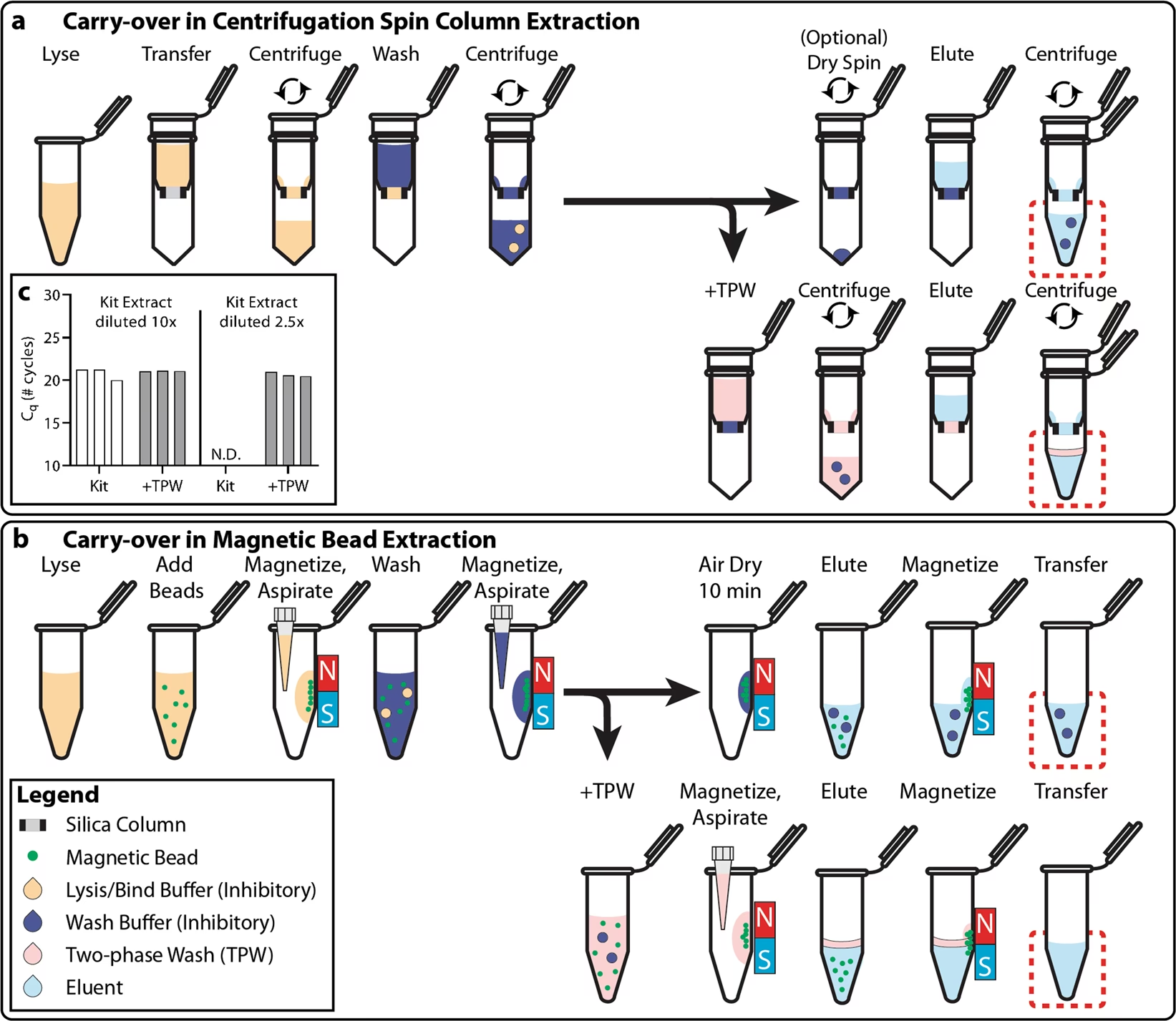
Una de las alternativas más extendidas son los kits comerciales basados en columnas de sílice. Estos kits utilizan membranas de sílice o partículas magnéticas que se unen específicamente al ARN en presencia de altas concentraciones de sales caotrópicas (a menudo todavía guanidina, pero sin la necesidad de fenol o cloroformo). El proceso es mucho más rápido y seguro:
- Las células se lisan en un tampón especial.
- La mezcla se pasa a través de una columna; el ARN se adhiere a la membrana de sílice.
- Se realizan varios lavados para eliminar contaminantes.
- Finalmente, el ARN puro se libera (eluye) de la membrana con agua.
Aunque estos kits son más seguros y rápidos, tienen sus propias desventajas ecológicas, como la generación de una gran cantidad de residuos plásticos de un solo uso (tubos, columnas, puntas de pipeta). Además, suelen ser más caros.
La investigación también avanza hacia reactivos fundamentalmente nuevos. Por ejemplo, se ha propuesto el uso de tricloroacetato de amonio (ATCA), un agente caotrópico potente pero no tóxico, que podría reemplazar al tiocianato de guanidina y simplificar el proceso sin comprometer la calidad del ARN.
Tabla Comparativa de Métodos de Extracción de ARN
| Característica | Método Fenol-Cloroformo | Kits Comerciales (Columna) | Método ATCA (Propuesto) |
|---|---|---|---|
| Reactivos Principales | Fenol, Tiocianato de Guanidina, Cloroformo | Sales caotrópicas, membranas de sílice, etanol | Tricloroacetato de amonio (ATCA), celulosa |
| Toxicidad | Alta | Reducida (sin fenol/cloroformo) | Baja (no tóxico) |
| Impacto Ambiental | Alto (residuos químicos peligrosos) | Medio (residuos plásticos de un solo uso) | Mínimo |
| Velocidad | Lento y laborioso | Rápido (30-60 min) | Rápido y simplificado |
¿Cómo se Mide la Pureza y Por Qué Importa?
La pureza del ARN es crítica. Contaminantes como el fenol o el tiocianato de guanidina pueden inhibir las reacciones posteriores, llevando a resultados falsos o no concluyentes. La calidad se mide con un espectrofotómetro, que analiza cuánta luz absorbe la muestra a diferentes longitudes de onda.
- La relación A260/A280 mide la contaminación por proteínas. Un valor ideal es ~2.0.
- La relación A260/A230 mide la contaminación por otros compuestos, como sales (incluido el tiocianato de guanidina). Un valor ideal es entre 2.0 y 2.2. Un valor bajo (inferior a 1.8) a menudo indica que quedan restos de guanidina en la muestra final.
Es un error común pensar que la contaminación por guanidina aumenta la concentración de ARN. En realidad, no lo hace. El problema es que el tiocianato de guanidina absorbe luz a una longitud de onda similar a la del ARN (alrededor de 260 nm), lo que puede inflar artificialmente la lectura de concentración y engañar al investigador.
Preguntas Frecuentes (FAQ)
- ¿Es venenoso el tiocianato de guanidina?
- Sí, es tóxico y nocivo si se ingiere. Además, su mezcla con ácidos puede liberar gases cianurados muy peligrosos. Su manejo requiere equipo de protección personal y protocolos de seguridad estrictos.
- ¿Por qué no se puede usar un detergente común para extraer ARN?
- Los detergentes comunes, como los utilizados para extraer proteínas (tampón RIPA), no son lo suficientemente potentes para desactivar completamente las enzimas RNasas, que son extremadamente resistentes. El ARN se degradaría rápidamente. Se necesitan agentes caotrópicos fuertes como el tiocianato de guanidina para garantizar su protección.
- ¿Qué significa una baja relación A260/A230 en una muestra de ARN?
- Generalmente indica la presencia de contaminantes que absorben luz a 230 nm. En el contexto del método de fenol-guanidina, es un signo clásico de contaminación residual por tiocianato de guanidina, lo que puede afectar gravemente los experimentos posteriores como la RT-PCR.
- ¿Existen métodos de extracción de ARN 100% ecológicos?
- Aún no existe una solución perfecta. Los métodos que eliminan los químicos tóxicos a menudo aumentan los residuos plásticos. La ciencia verde en el laboratorio busca un equilibrio, promoviendo reactivos más seguros, reduciendo los plásticos de un solo uso y optimizando protocolos para generar menos residuos. El camino es hacia una ciencia más sostenible, pero es un proceso en desarrollo.
En conclusión, el tiocianato de guanidina y el fenol son herramientas increíblemente poderosas que han impulsado la ciencia durante décadas. Sin embargo, su legado tóxico nos obliga a mirar hacia el futuro. La transición hacia una "química verde" en el laboratorio no es solo una opción, sino una necesidad para proteger tanto a los científicos como al planeta que todos compartimos. La próxima vez que escuches sobre un avance en diagnóstico molecular, recuerda el complejo equilibrio entre el progreso científico y la responsabilidad ambiental que se juega en cada tubo de ensayo.
Si quieres conocer otros artículos parecidos a El Dilema Tóxico del Laboratorio Moderno puedes visitar la categoría Contaminación.