12/12/2003
El agua subterránea, ese vasto y oculto recurso que fluye bajo nuestros pies, es un sistema químico complejo y dinámico. Su composición no es pura H₂O; es un cóctel de minerales y elementos disueltos que adquiere en su lento viaje a través del subsuelo. Uno de los elementos más significativos y omnipresentes en este entorno es el azufre. Comprender su comportamiento, sus formas predominantes y su origen es fundamental no solo para la geoquímica, sino también para la gestión de la calidad del agua que consumimos y para la protección de los ecosistemas subterráneos. Aunque existen varias especies químicas del azufre, una de ellas reina de forma casi absoluta en la mayoría de los acuíferos del planeta.
El Sulfato (SO₄²⁻): El Rey Indiscutible del Azufre Subterráneo
Cuando analizamos la química del agua subterránea, la especie de azufre que encontramos de manera predominante es, con diferencia, el ion sulfato (SO₄²⁻). Este anión, compuesto por un átomo de azufre y cuatro de oxígeno, es altamente soluble en agua y muy estable en condiciones óxicas, es decir, en presencia de oxígeno disuelto. Dado que muchos acuíferos, especialmente los más someros y con recarga activa, contienen niveles significativos de oxígeno, el sulfato se convierte en la forma termodinámicamente favorecida del azufre.
Su presencia es un indicador clave de diversos procesos geológicos y atmosféricos. La concentración de sulfato puede variar enormemente, desde niveles muy bajos, casi indetectables, en acuíferos prístinos y aislados, hasta concentraciones muy elevadas en zonas con geologías específicas o afectadas por contaminación.
El Origen del Sulfato: Un Viaje desde el Cielo a la Roca
La pregunta clave es: ¿de dónde proviene todo este sulfato? Su origen es doble y a menudo secuencial, un proceso en el que la señal inicial es frecuentemente enmascarada por una influencia posterior mucho más potente.
1. Aporte Atmosférico: La Primera Señal
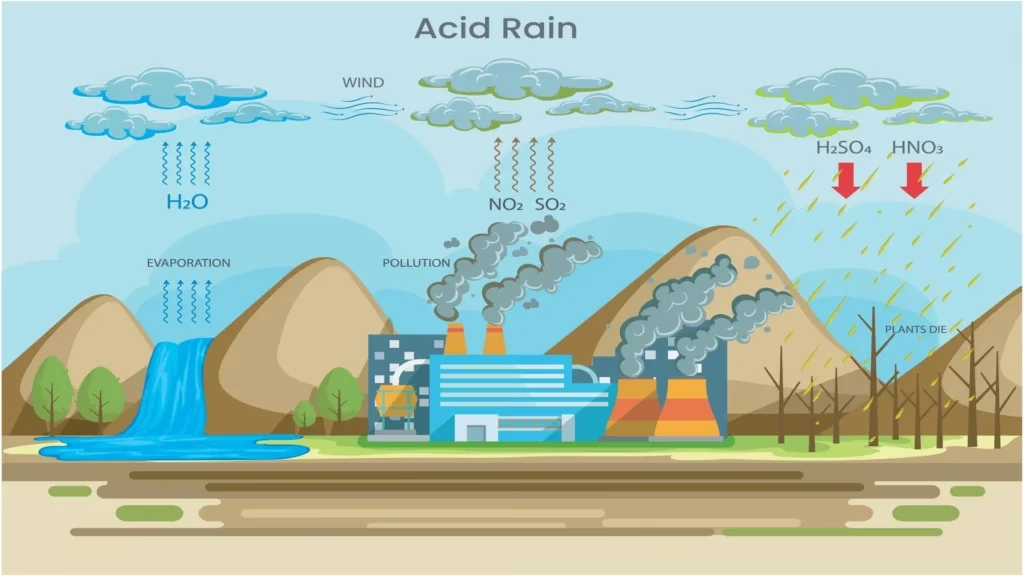
Inicialmente, una parte del sulfato presente en las aguas subterráneas proviene directamente de la atmósfera. El agua de lluvia no es pura; disuelve gases y arrastra partículas presentes en el aire. El azufre llega a la atmósfera por varias vías:
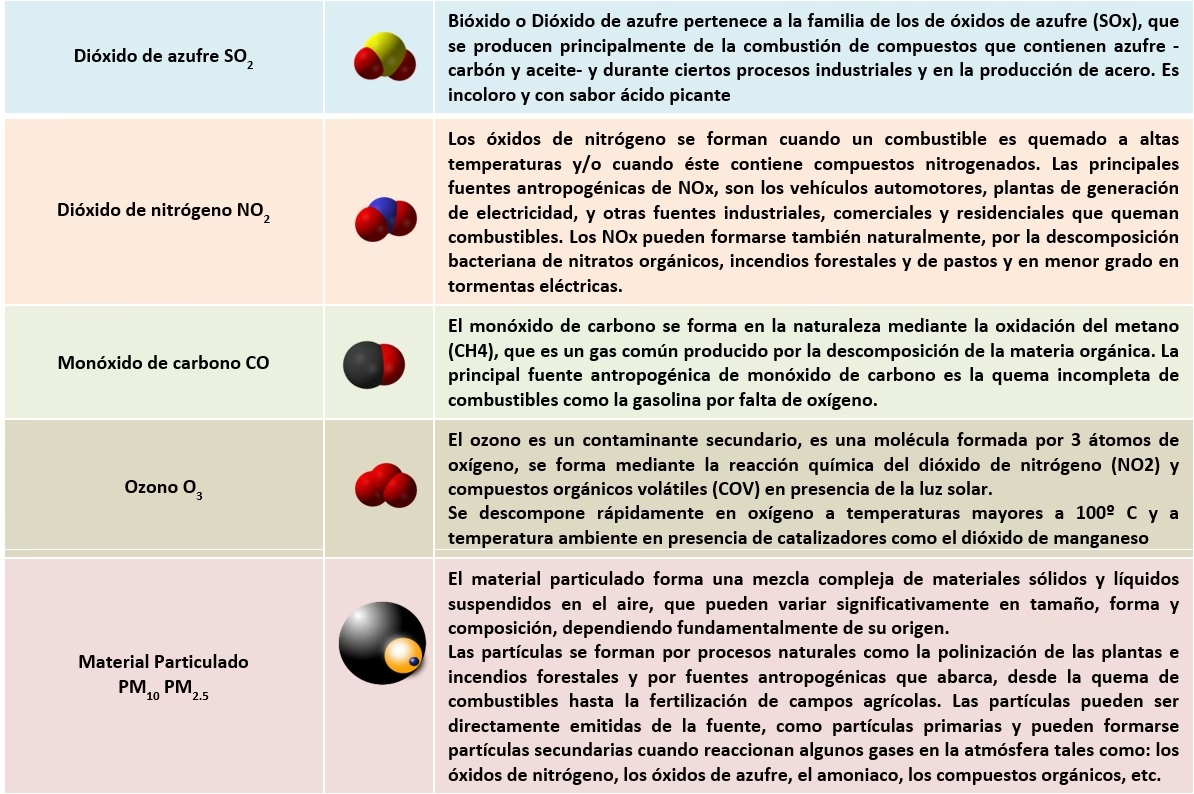
- Emisiones volcánicas: Los volcanes liberan grandes cantidades de dióxido de azufre (SO₂) a la atmósfera.
- Quema de combustibles fósiles: La industria y el transporte emiten SO₂, que reacciona con el agua y el oxígeno atmosférico para formar ácido sulfúrico (H₂SO₄), el principal componente de la lluvia ácida.
- Aerosoles marinos: La evaporación del agua de mar libera sulfatos en forma de pequeñas partículas que pueden ser transportadas tierra adentro.
Cuando llueve, este sulfato atmosférico se disuelve en el agua y se infiltra en el suelo. En teoría, si el subsuelo fuera completamente inerte, la concentración de sulfato en el agua subterránea reflejaría la de la lluvia. Sin embargo, esto rara vez ocurre.
2. Interacción Agua-Roca: La Influencia Geológica Dominante
Aquí es donde la historia se vuelve más compleja y fascinante. A medida que el agua infiltrada percola a través de la zona no saturada (el suelo por encima del nivel freático) y luego fluye por la zona saturada (el acuífero propiamente dicho), entra en contacto con rocas y minerales. Este proceso de interacción agua-roca es el factor que más contribuye a la concentración final de sulfato, borrando casi por completo la señal atmosférica inicial.
Existen minerales muy comunes en la corteza terrestre que son ricos en azufre. Los más importantes son:
- Evaporitas: Rocas formadas por la evaporación de antiguos mares o lagos. El yeso (CaSO₄·2H₂O) y la anhidrita (CaSO₄) son minerales de sulfato de calcio extremadamente comunes. Cuando el agua subterránea fluye a través de formaciones de yeso, lo disuelve fácilmente, liberando grandes cantidades de iones de calcio y sulfato al agua.
- Sulfuros metálicos: Minerales como la pirita (FeS₂), conocida como el "oro de los tontos", son comunes en muchos tipos de rocas. En presencia de oxígeno, la pirita se oxida en un proceso que libera sulfato y hierro, y además acidifica el agua, lo que a su vez puede disolver otros minerales.
Por lo tanto, la geología local es el principal controlador. Un acuífero que atraviesa capas de yeso tendrá concentraciones de sulfato naturalmente muy altas, mientras que uno alojado en rocas graníticas o arenas de cuarzo (pobres en azufre) tendrá niveles mucho más bajos.
El Otro Protagonista: El Sulfuro de Hidrógeno (H₂S)
Aunque el sulfato es el dominante, en ciertas condiciones aparece otra especie de azufre: el sulfuro de hidrógeno (H₂S), también conocido como ácido sulfhídrico. Este compuesto es un gas disuelto en agua, famoso por su característico y desagradable olor a huevos podridos.
El H₂S se forma en condiciones opuestas a las del sulfato: en ambientes reductores o anóxicos (sin oxígeno). Su aparición es principalmente un proceso biológico, mediado por un grupo de bacterias conocidas como bacterias sulfato-reductoras (BSR). En ausencia de oxígeno, estas bacterias utilizan el ion sulfato (SO₄²⁻) como agente oxidante para metabolizar materia orgánica, "respirando" sulfato en lugar de oxígeno. El producto de desecho de este metabolismo es el sulfuro de hidrógeno.
Estas condiciones se dan típicamente en:
- Partes profundas y estancadas de los acuíferos, donde el oxígeno se ha consumido.
- Zonas con alta concentración de materia orgánica (como acuíferos contaminados o en contacto con turberas).
- Sistemas geotérmicos y aguas termales.
Tabla Comparativa: Sulfato vs. Sulfuro de Hidrógeno en Aguas Subterráneas
| Característica | Sulfato (SO₄²⁻) | Sulfuro de Hidrógeno (H₂S) |
|---|---|---|
| Forma Química | Ion disuelto (anión) | Gas disuelto |
| Condiciones Ambientales | Óxicas (con oxígeno) | Anóxicas (sin oxígeno) |
| Origen Principal | Disolución de minerales (yeso, pirita) | Reducción bacteriana del sulfato |
| Características Organolépticas | Inodoro, insípido (a bajas concentraciones) | Olor a "huevos podridos" |
| Impacto en Calidad del Agua | A altas concentraciones, efecto laxante | Mal olor y sabor, corrosivo para tuberías |
Implicaciones para el Medio Ambiente y el Consumo Humano
La especiación del azufre no es una mera curiosidad científica; tiene consecuencias directas. Las altas concentraciones de sulfato en el agua potable, aunque no se consideran altamente tóxicas, pueden tener un efecto laxante, especialmente en personas no acostumbradas a su consumo. Por ello, las organizaciones de salud establecen límites recomendados para el sulfato en el agua de red (generalmente en torno a 250-500 mg/L).
Por su parte, el sulfuro de hidrógeno, incluso a concentraciones muy bajas, hace que el agua sea desagradable para el consumo debido a su olor. Además, es corrosivo y puede dañar tuberías y sistemas de fontanería metálicos. En concentraciones muy altas (raras en aguas subterráneas pero posibles en entornos industriales o geotérmicos), el H₂S es un gas tóxico.
Preguntas Frecuentes (FAQ)
¿El agua de mi pozo huele a azufre, significa que está contaminada?
No necesariamente. El olor a "huevos podridos" se debe al sulfuro de hidrógeno (H₂S), que a menudo se genera de forma natural por bacterias en condiciones de poco oxígeno. Si bien hace que el agua sea desagradable, no siempre indica una contaminación peligrosa, aunque es recomendable realizar un análisis completo del agua para descartar otros problemas.
¿Se puede eliminar el sulfato del agua?
Sí, pero los métodos suelen ser costosos y se reservan para casos de concentraciones muy altas. Tecnologías como la ósmosis inversa, la destilación o el intercambio iónico pueden reducir eficazmente los niveles de sulfato.
¿Toda el agua subterránea contiene sulfato?
Prácticamente toda, pero en concentraciones muy variables. Desde acuíferos en rocas silíceas con menos de 1 mg/L hasta acuíferos en zonas evaporíticas que pueden superar los 2000 mg/L. La geología local es el factor determinante.
En conclusión, el azufre en las aguas subterráneas es un elemento dinámico cuya forma predominante, el sulfato, nos cuenta una historia sobre el viaje del agua desde la atmósfera hasta las profundidades de la Tierra. Su concentración final es un testimonio de la íntima relación entre el agua y la roca, un diálogo químico silencioso y perpetuo que modela la calidad del recurso hídrico más importante del planeta.
Si quieres conocer otros artículos parecidos a Azufre en Aguas Subterráneas: Origen y Formas puedes visitar la categoría Ecología.