23/11/2017
En el mundo de la construcción, la ingeniería y hasta en los objetos más cotidianos, la durabilidad de los materiales es un pilar fundamental para la sostenibilidad. Sin embargo, existe un fenómeno químico sigiloso y destructivo que a menudo pasa desapercibido hasta que el daño es evidente: la corrosión galvánica. Este proceso no solo compromete la integridad estructural de piezas y equipos, sino que también implica un coste económico y ambiental significativo debido a la necesidad de reparaciones y reemplazos prematuros. Comprender sus causas y, sobre todo, cómo prevenirla, es esencial para un diseño responsable y un uso consciente de nuestros recursos metálicos.

Este artículo se sumerge en el corazón de este proceso electroquímico. Exploraremos desde sus fundamentos científicos hasta las estrategias más efectivas para su mitigación, proporcionando un conocimiento práctico para ingenieros, diseñadores, y cualquier persona interesada en la preservación de materiales y la promoción de prácticas más sostenibles.
¿Qué es Exactamente la Corrosión Galvánica?
La corrosión galvánica, también conocida como corrosión bimetálica, es un proceso electroquímico que ocurre cuando dos metales diferentes (o aleaciones) entran en contacto eléctrico en presencia de un electrolito, como el agua, la humedad del aire o el agua salada. En estas condiciones, se forma una especie de batería o celda galvánica a pequeña escala.
En esta celda, un metal se convierte en el ánodo (el polo negativo) y el otro en el cátodo (el polo positivo). El metal que actúa como ánodo es el menos noble o más activo, y es el que se corroe a una velocidad acelerada, sacrificándose para proteger al cátodo. Mientras tanto, el metal catódico, que es el más noble o menos activo, ve su propia tasa de corrosión disminuida o incluso detenida. El electrolito cierra el circuito, permitiendo el flujo de iones metálicos desde el ánodo hacia el cátodo, lo que resulta en la pérdida de material del primero.
Para predecir qué metal se corroerá, los ingenieros utilizan la "serie galvánica", una lista que ordena los metales y aleaciones según su potencial electroquímico en un electrolito específico (generalmente agua de mar). Cuanto más separados estén dos metales en esta serie, mayor será la diferencia de potencial y, por lo tanto, más rápida y severa será la corrosión del metal anódico.

Identificando los Síntomas en los Materiales
A diferencia de la oxidación uniforme, la corrosión galvánica presenta síntomas muy localizados. Generalmente, se observa un deterioro acelerado justo en la unión entre los dos metales diferentes. Los signos visibles incluyen:
- Picaduras o pérdida de material en uno de los metales (el anódico).
- Acumulación de óxido o productos de la corrosión en la interfaz.
- Decoloración o manchas que se extienden desde el punto de contacto.
- Fragilidad o fallo estructural prematuro en la zona de la unión.
Estrategias Clave para Prevenir la Corrosión Galvánica
Afortunadamente, existen múltiples métodos probados para combatir este fenómeno. La clave está en romper uno de los tres elementos necesarios para que se produzca: el contacto eléctrico, la presencia de un electrolito o la diferencia de potencial entre los metales.
1. Aislamiento Eléctrico
La estrategia más directa es evitar que los dos metales distintos entren en contacto eléctrico. Esto se logra interponiendo un material aislante y no conductor entre ellos.
- Juntas y Arandelas: Utilizar arandelas, juntas o empaques de materiales como neopreno, teflón (PTFE), nylon o caucho es una práctica común. Un excelente ejemplo se encuentra en los sistemas de escape de los automóviles, donde las sujeciones que unen partes de acero inoxidable al chasis de acero al carbono a menudo incorporan componentes de goma para evitar el contacto directo y la corrosión.
- Recubrimientos Aislantes: Aplicar pinturas, recubrimientos en polvo o epóxicos en las superficies de contacto puede crear una barrera dieléctrica eficaz.
2. Selección Inteligente de Materiales
En la fase de diseño, la mejor defensa es una buena ofensiva. Seleccionar metales que estén muy juntos en la serie galvánica minimiza la diferencia de potencial y, por ende, la tasa de corrosión. Si es inevitable usar metales disímiles, se debe intentar que el área del metal catódico (el más noble) sea pequeña en comparación con la del metal anódico (el que se corroe). Una gran área catódica y una pequeña área anódica es la peor combinación posible, ya que concentra todo el ataque corrosivo en una zona muy pequeña, provocando fallos rápidos.
3. Control del Entorno (Eliminar el Electrolito)
Si se puede mantener la unión de los metales completamente seca, la corrosión galvánica no puede ocurrir. Esto se logra diseñando las estructuras de manera que el agua no se acumule en las juntas bimetálicas. Un ejemplo práctico es la fijación de revestimientos de acero inoxidable a estructuras internas de acero al carbono; si esta unión se realiza en zonas interiores no expuestas a la humedad, el riesgo de corrosión se reduce drásticamente.
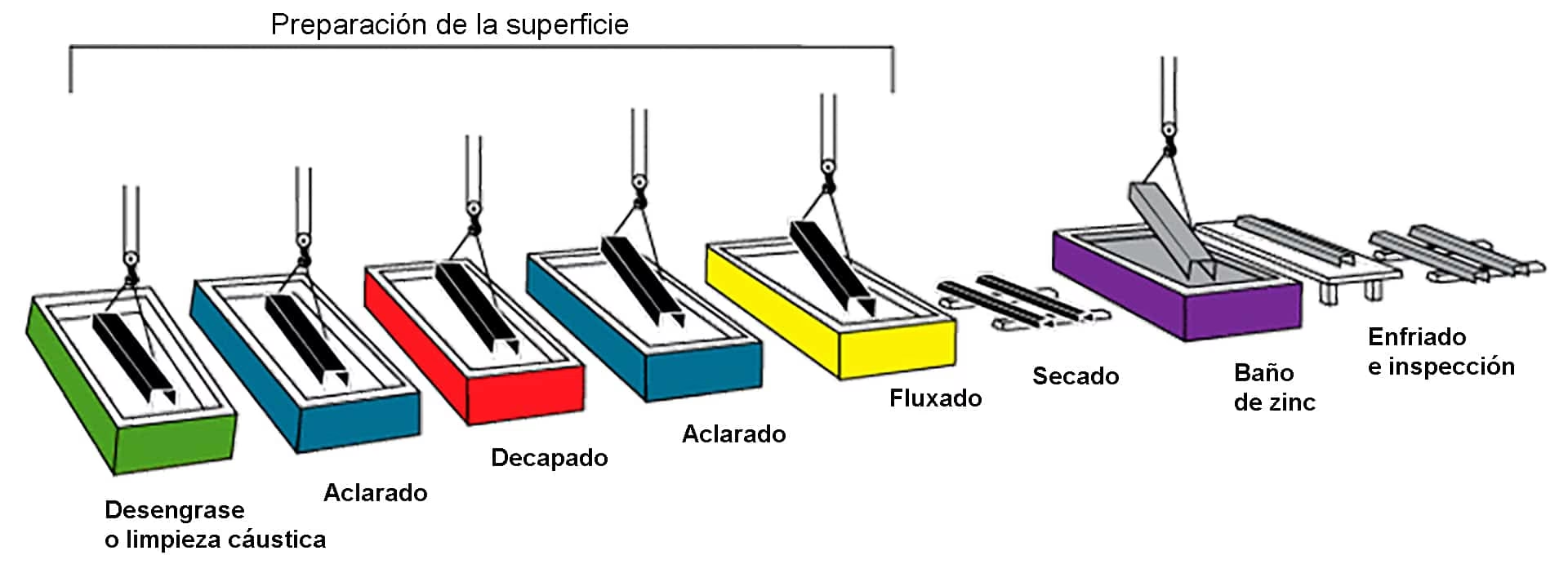
4. Recubrimientos Protectores: El Caso del Galvanizado
Una de las técnicas más extendidas para proteger un metal (generalmente acero) es recubrirlo con otro que actúe como ánodo de sacrificio. El proceso de galvanizado es el ejemplo por excelencia.
En el galvanizado en caliente, una pieza de acero se sumerge en un baño de zinc fundido a altas temperaturas (alrededor de 450°C). Se produce una reacción metalúrgica que une el zinc al acero, creando varias capas de aleación zinc-hierro con una capa exterior de zinc puro. Esta capa ofrece una doble protección:
- Protección de Barrera: El recubrimiento de zinc aísla físicamente al acero del entorno.
- Protección Catódica (o de Sacrificio): Si el recubrimiento se raya o daña, exponiendo el acero, el zinc circundante, al ser más anódico que el acero, se corroerá preferentemente, protegiendo el acero expuesto.
5. Ánodos de Sacrificio
Este método lleva la protección catódica un paso más allá. Consiste en conectar eléctricamente una pieza de un metal mucho más activo (como zinc, aluminio o magnesio) a la estructura metálica que se desea proteger. Este metal adicional, llamado ánodo de sacrificio, se corroe intencionadamente, consumiéndose con el tiempo para proteger la estructura principal. Es una técnica vital en aplicaciones marinas (cascos de barcos, plataformas petrolíferas) y en tuberías subterráneas.
Tabla Comparativa de Métodos de Prevención
| Método | Efectividad | Costo Inicial | Aplicabilidad | Consideración Ambiental |
|---|---|---|---|---|
| Aislamiento Eléctrico | Muy Alta | Bajo | Uniones atornilladas, ensamblajes mecánicos | Bajo impacto, aunque depende del material aislante. |
| Selección de Materiales | Alta (en diseño) | Variable | Fase de diseño de nuevos productos | Promueve el uso eficiente y duradero de recursos. |
| Galvanizado en Caliente | Muy Alta y Duradera | Medio | Estructuras de acero, piezas pequeñas, tornillería | Proceso intensivo en energía. El zinc es reciclable. |
| Ánodos de Sacrificio | Alta (requiere mantenimiento) | Medio-Alto | Estructuras marinas, tanques, tuberías | Los ánodos se consumen y deben ser reemplazados. |
Riesgos Laborales Asociados a la Manipulación de Metales Galvanizados
Es importante hacer una distinción crucial: los metales galvanizados en su estado normal son seguros. Sin embargo, los procesos que los alteran drásticamente, como la soldadura o el corte a alta temperatura, pueden liberar humos de óxido de zinc. La inhalación de estos humos puede provocar una condición conocida como "fiebre del soldador" o "fiebre de los humos metálicos", cuyos síntomas (fatiga, dificultades para respirar, fiebre) son temporales pero desagradables. En procesos industriales más complejos que involucran otros metales como plomo o cadmio, los riesgos pueden ser mucho más graves, llegando a causar daños en el sistema nervioso. Por ello, la protección respiratoria y una ventilación adecuada son absolutamente críticas al trabajar con estos materiales en caliente, siendo una cuestión de salud laboral y no un síntoma del metal en sí.
Preguntas Frecuentes (FAQ)
¿El acero inoxidable se puede corroer galvánicamente?
Sí. Aunque el acero inoxidable es muy resistente a la corrosión (es un metal noble), si se pone en contacto con un metal aún más noble como el titanio o el grafito en un electrolito, puede actuar como ánodo y corroerse. Más comúnmente, si se une con un metal menos noble como el aluminio o el acero al carbono, acelerará drásticamente la corrosión de estos últimos.

¿El agua dulce también puede actuar como electrolito?
Sí, aunque es un electrolito mucho más débil que el agua salada. La corrosión galvánica será significativamente más lenta en agua dulce o en ambientes con baja humedad en comparación con entornos marinos o industriales con alta salinidad y contaminación.
¿Es la corrosión galvánica siempre perjudicial?
No. El principio de la corrosión galvánica se aprovecha deliberadamente en tecnologías como las baterías (pilas alcalinas, por ejemplo) para generar una corriente eléctrica, y en los sistemas de protección catódica (con ánodos de sacrificio) para proteger infraestructuras valiosas.
En conclusión, la corrosión galvánica es una fuerza natural que no puede ser eliminada, pero sí gestionada y controlada con conocimiento y un diseño adecuado. Al aplicar estrategias de aislamiento, selección de materiales, recubrimientos y protección catódica, no solo extendemos la vida útil de nuestros bienes y estructuras, sino que también contribuimos a un futuro más sostenible, reduciendo el desperdicio de materiales y la energía necesaria para reemplazarlos. La prevención es, sin duda, la mejor herramienta contra este silencioso pero implacable proceso de degradación.
Si quieres conocer otros artículos parecidos a Corrosión Galvánica: Guía para Proteger Metales puedes visitar la categoría Sostenibilidad.

