27/09/2009
En nuestro planeta, y en el universo entero, la materia se presenta en un fascinante baile constante, una coreografía dictada por la energía y las fuerzas invisibles que unen o separan a sus componentes más pequeños: las partículas. A simple vista vemos un cubo de hielo, un vaso de agua o el vapor que se eleva de una taza caliente, pero en su interior se libra una batalla microscópica que define su forma, su comportamiento y su rol en la naturaleza. Comprender la diferencia entre los estados sólido, líquido y gaseoso no es solo una lección de química, es entender los cimientos de los ciclos vitales de la Tierra, desde la formación de las nubes hasta el deshielo de los glaciares.
El Corazón de la Materia: La Teoría Cinética Molecular
Para desentrañar el misterio de los estados de la materia, debemos acudir a la Teoría Cinética Molecular. Esta teoría postula algo fundamental: toda la materia está compuesta por partículas (átomos, moléculas o iones) que están en perpetuo movimiento. Este movimiento es lo que conocemos como energía cinética. Cuanto más rápido se mueven las partículas, mayor es su energía cinética y, generalmente, mayor es la temperatura de la sustancia.
Sin embargo, el movimiento no es lo único que importa. Existen también dos fuerzas en constante competencia:
- Fuerzas de Cohesión (Atracción): Son las fuerzas que tienden a mantener unidas a las partículas. Imagínalas como pequeños imanes que intentan que las partículas se queden juntas y ordenadas.
- Fuerzas de Repulsión: Son las fuerzas asociadas al propio movimiento de las partículas, que tienden a separarlas y dispersarlas.
El estado en que encontramos una sustancia (sólido, líquido o gas) es el resultado directo de cuál de estas fuerzas predomina en un momento dado, lo cual depende en gran medida de la temperatura y la presión.
Un Vistazo Detallado a los Estados de Agregación
Con la base de la teoría cinética, podemos ahora explorar las características únicas de cada estado principal de la materia.
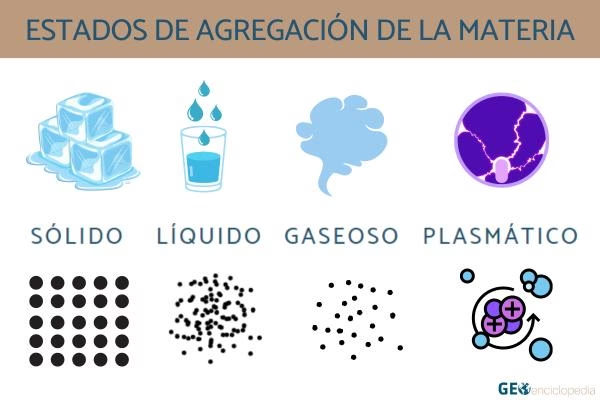
Estado Sólido: Orden y Estabilidad
En el estado sólido, las fuerzas de cohesión son inmensamente superiores a las fuerzas de repulsión. Las partículas están fuertemente atraídas entre sí, empaquetadas en una estructura ordenada y definida, a menudo cristalina. Esto no significa que estén quietas; en realidad, vibran constantemente en sus posiciones fijas, pero no tienen la energía suficiente para desplazarse. Por esta razón, los sólidos tienen una forma y un volumen definidos y su nivel de energía es el más bajo de los tres estados.
Estado Líquido: Fluidez y Adaptabilidad
Al aumentar la temperatura de un sólido, sus partículas ganan energía cinética y vibran con más intensidad. Llega un punto en que la energía es suficiente para vencer parcialmente las rígidas fuerzas de cohesión. Las partículas pueden entonces deslizarse unas sobre otras. Esto es el estado líquido. Las fuerzas de atracción y repulsión están más equilibradas. Por ello, los líquidos no tienen una forma propia (se adaptan al recipiente que los contiene), pero sí mantienen un volumen constante. Su energía es intermedia.
Estado Gaseoso: Libertad y Expansión
Si continuamos aportando energía a un líquido, sus partículas se moverán tan rápido que las fuerzas de repulsión dominarán por completo a las de cohesión. Las partículas se separan enormemente unas de otras y se mueven a gran velocidad en todas las direcciones, chocando entre sí y con las paredes del recipiente. Esto es el estado gaseoso. Los gases no tienen ni forma ni volumen definidos; tienden a ocupar todo el espacio disponible, un fenómeno conocido como expansión. Este es el estado con mayor nivel de energía cinética.
Tabla Comparativa de los Estados de la Materia
| Característica | Sólido | Líquido | Gaseoso |
|---|---|---|---|
| Fuerzas Intermoleculares | Predomina la atracción (cohesión) | Atracción y repulsión equilibradas | Predomina la repulsión |
| Movimiento de Partículas | Vibración en posiciones fijas | Se deslizan unas sobre otras | Movimiento libre, rápido y caótico |
| Forma | Definida | Adopta la del recipiente | Indefinida |
| Volumen | Definido | Definido | Indefinido (ocupa todo el espacio) |
| Nivel de Energía Cinética | Bajo | Intermedio | Alto |
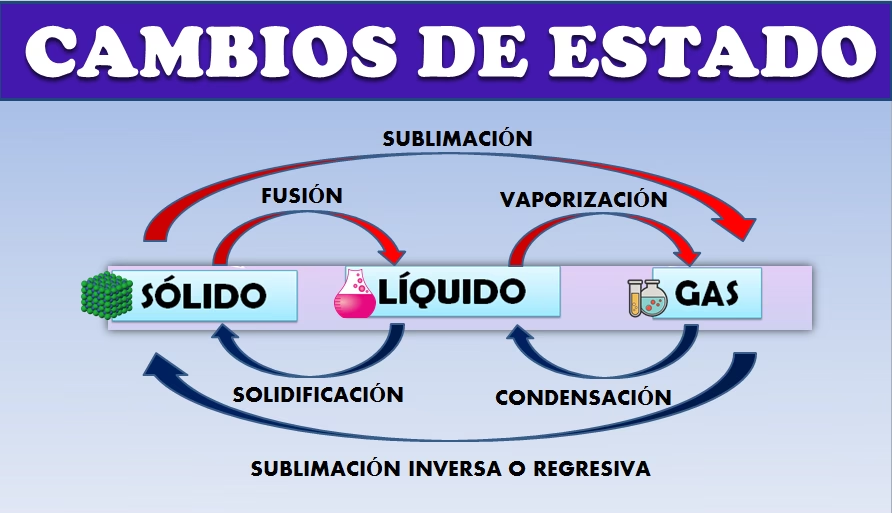
La Danza de la Transformación: Cambios de Estado
La materia no está condenada a un solo estado. Puede transicionar de uno a otro mediante la adición o eliminación de energía, generalmente en forma de calor. Estos cambios son fenómenos físicos que vemos a diario y son cruciales para los ciclos de la naturaleza. Los principales cambios de estado son:
- Fusión: Paso de sólido a líquido (ej. derretir hielo). Requiere un aumento de temperatura.
- Solidificación: Paso de líquido a sólido (ej. congelar agua). Requiere una disminución de temperatura.
- Vaporización: Paso de líquido a gas (ej. hervir agua). Requiere un aumento de temperatura.
- Condensación: Paso de gas a líquido (ej. el rocío en una mañana fría). Requiere una disminución de temperatura.
- Sublimación: Paso directo de sólido a gas sin pasar por el estado líquido (ej. el hielo seco).
- Sublimación inversa o deposición: Paso directo de gas a sólido (ej. la formación de escarcha).
Además de la temperatura, la presión es el otro factor externo crucial que puede inducir un cambio de estado. Aumentar la presión sobre un gas puede forzar a sus partículas a juntarse hasta que se convierte en líquido, incluso sin bajar la temperatura.

El Vínculo Ambiental: Estados de la Materia en Nuestro Ecosistema
Como ecologistas, entender estos principios es vital. El ciclo del agua, motor de la vida en la Tierra, no es más que una serie continua de cambios de estado: la evaporación del agua líquida de los océanos, la condensación en las nubes y la precipitación en forma líquida (lluvia) o sólida (nieve). Los casquetes polares, en su estado sólido, actúan como gigantescos reflectores de la luz solar, ayudando a regular la temperatura del planeta. El dióxido de carbono en estado gaseoso en la atmósfera es fundamental para la fotosíntesis, pero su exceso provoca el efecto invernadero.
El cambio climático está alterando drásticamente este equilibrio. El aumento de la temperatura global está inyectando una cantidad masiva de energía térmica en el sistema, acelerando la fusión de glaciares y hielo polar (paso de sólido a líquido). Esto no solo eleva el nivel del mar, sino que también libera gases de efecto invernadero atrapados en el hielo, creando un peligroso ciclo de retroalimentación. Entender la física de los estados de la materia nos da las herramientas para comprender la magnitud de estos cambios y la urgencia de actuar.
Preguntas Frecuentes (FAQ)
¿Por qué un gas ocupa todo el espacio disponible?
Porque sus partículas tienen una energía cinética muy alta y las fuerzas de repulsión superan con creces a las de atracción. Esto hace que se muevan libremente y se expandan hasta chocar con las paredes del recipiente que las contiene, sin importar su tamaño.

¿Qué estado de la materia tiene más energía y por qué?
El estado gaseoso. La energía de un estado está directamente relacionada con la energía cinética de sus partículas. En los gases, las partículas se mueven a la mayor velocidad y con la mayor libertad, por lo que su nivel energético es el más elevado.
Si las partículas de los sólidos siempre están en movimiento, ¿por qué son rígidos?
Porque su movimiento se limita a una vibración en un punto fijo. Las fuerzas de cohesión son tan intensas que las mantienen ancladas en una estructura definida, impidiendo que se desplacen. Es como una multitud de personas bailando en su sitio sin moverse del lugar.
¿Solo la temperatura puede cambiar el estado de la materia?
No. La presión es el otro factor determinante. Por ejemplo, podemos licuar un gas como el butano simplemente aumentando la presión sobre él, como ocurre dentro de un encendedor. Del mismo modo, el agua hierve a menor temperatura en la cima de una montaña porque la presión atmosférica es menor.
Si quieres conocer otros artículos parecidos a Estados de la Materia: El Baile de las Partículas puedes visitar la categoría Ecología.
