28/01/2006
En el vasto universo de los compuestos químicos, pocos tienen una dualidad tan marcada como el dióxido de azufre (SO₂). Por un lado, es un pilar fundamental en numerosos procesos industriales que sostienen nuestro modo de vida moderno. Por otro, es un notorio contaminante atmosférico con graves repercusiones para el medio ambiente y la salud humana. Este gas incoloro, pero de olor penetrante y sofocante, similar al de una cerilla recién quemada, se encuentra en el centro de un debate crucial sobre el progreso industrial y la sostenibilidad ecológica. Comprender su naturaleza, sus fuentes, sus efectos y las formas de mitigarlo es esencial para forjar un futuro donde la actividad humana y la salud del planeta puedan coexistir en armonía.
- ¿Qué es Exactamente el Dióxido de Azufre (SO₂)?
- El Origen del SO₂: Fuentes Naturales e Industriales
- La Cara Útil: Aplicaciones Industriales del SO₂
- La Sombra del Progreso: El Devastador Impacto Ambiental
- Un Enemigo Silencioso para la Salud Humana
- Hacia un Aire Más Limpio: Estrategias de Control y Reducción
- Preguntas Frecuentes sobre el Dióxido de Azufre
¿Qué es Exactamente el Dióxido de Azufre (SO₂)?
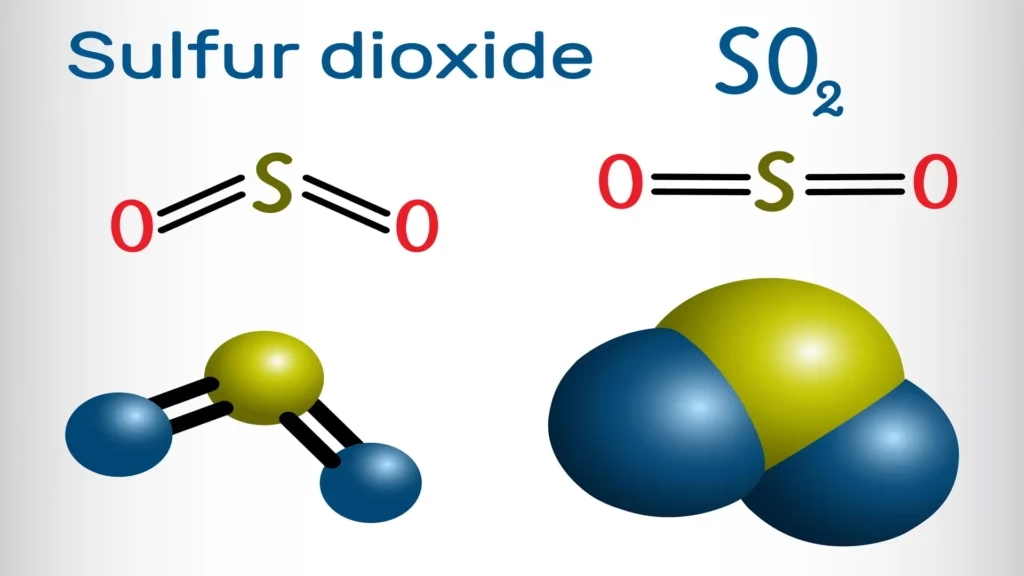
Desde una perspectiva química, el dióxido de azufre es un compuesto simple formado por un átomo de azufre (S) unido a dos átomos de oxígeno (O). A temperatura y presión ambiente, se presenta como un gas. Una de sus características más notables es que es considerablemente más denso que el aire, lo que significa que, en caso de una fuga o emisión concentrada, tiende a acumularse en zonas bajas como sótanos o valles, aumentando el riesgo de exposición en esos lugares.
Aunque es un gas en condiciones normales, puede ser licuado con relativa facilidad aplicando presión, lo que facilita su almacenamiento y transporte para usos industriales. Químicamente, actúa como un potente agente reductor, lo que significa que puede donar electrones en reacciones químicas. Esta propiedad es clave para muchos de sus usos, pero también para su transformación en la atmósfera, donde puede reaccionar con el oxígeno para formar trióxido de azufre (SO₃), el precursor directo del ácido sulfúrico.
Propiedades Físicas Clave
Para entender mejor su comportamiento, aquí se presentan sus propiedades físicas más importantes en una tabla comparativa:
| Propiedad | Valor |
|---|---|
| Fórmula Química | SO₂ |
| Punto de Fusión | -72 °C |
| Punto de Ebullición | -10 °C |
| Densidad (a 25°C) | 2.63 kg/m³ (Más denso que el aire) |
| Apariencia | Gas incoloro |
| Olor | Agudo, picante y sofocante |
El Origen del SO₂: Fuentes Naturales e Industriales
Las emisiones de dióxido de azufre a la atmósfera provienen tanto de fuentes naturales como de actividades humanas (antropogénicas), si bien estas últimas son las principales responsables de las altas concentraciones que generan problemas ambientales.
Fuentes Naturales
La fuente natural más importante de SO₂ son las erupciones volcánicas. Un solo volcán activo puede liberar miles de toneladas de este gas a la atmósfera en un corto período. Estos eventos, aunque esporádicos, pueden tener impactos climáticos y ambientales a escala global. Otras fuentes naturales menores incluyen la descomposición de materia orgánica en humedales y la oxidación de gases que contienen azufre producidos por la vida marina.
Fuentes Antropogénicas
La gran mayoría del SO₂ presente en la atmósfera hoy en día es resultado de la actividad humana. La principal fuente es la quema de combustibles fósiles que contienen azufre, como el carbón y el petróleo, para la generación de electricidad en centrales térmicas y en procesos industriales. Otras fuentes significativas incluyen:
- Fundición de metales: La extracción de metales como el cobre, el níquel o el plomo a partir de sus minerales (que suelen ser sulfuros) libera grandes cantidades de SO₂.
- Refinerías de petróleo: Durante el proceso de refinado, el azufre presente en el crudo se elimina para producir combustibles más limpios, generando SO₂ como subproducto.
- Transporte: Los motores diésel, especialmente en barcos y maquinaria pesada, que utilizan combustibles con alto contenido de azufre, son una fuente importante de emisiones.
La Cara Útil: Aplicaciones Industriales del SO₂
A pesar de su mala reputación como contaminante, el dióxido de azufre es una materia prima indispensable en la industria química. Su principal aplicación, que consume la mayor parte de su producción, es la fabricación de ácido sulfúrico (H₂SO₄), a menudo llamado el "rey de los productos químicos" por su volumen de producción y su infinidad de usos en la fabricación de fertilizantes, baterías, pigmentos, detergentes y explosivos.
Además, el SO₂ tiene otros usos importantes:
- Industria Alimentaria: Se utiliza como conservante y antioxidante, identificado con el código E220. Previene el crecimiento de bacterias y mohos y evita la oxidación que oscurece el color de ciertos alimentos. Es común encontrarlo en frutos secos (como los orejones), zumos de frutas y, de forma muy destacada, en la producción de vino.
- Vinicultura: En la elaboración del vino, el SO₂ (en forma de sulfitos) es crucial. Actúa como un agente antimicrobiano que elimina levaduras y bacterias indeseadas y como un antioxidante que protege el sabor y el color del vino del deterioro por el contacto con el oxígeno.
- Blanqueamiento: Se emplea como agente blanqueador en la producción de pulpa de papel y en la industria textil para tratar fibras como la lana y la seda.
La Sombra del Progreso: El Devastador Impacto Ambiental
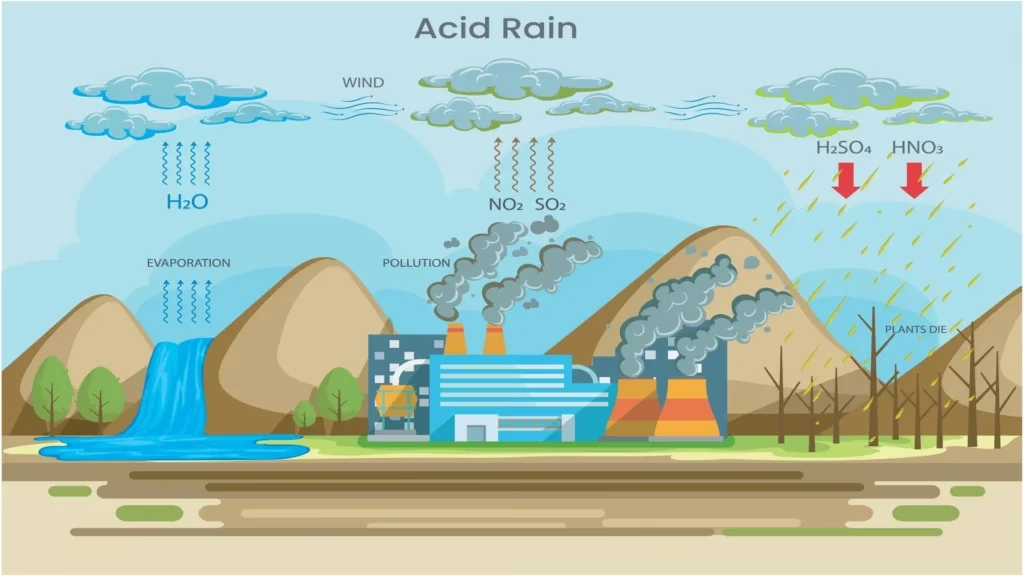
El impacto ambiental más conocido y dañino del dióxido de azufre es su papel como principal causante de la lluvia ácida. Este fenómeno ocurre cuando el SO₂ y otros óxidos, como los de nitrógeno, se liberan a la atmósfera.
El proceso químico es el siguiente:
- El SO₂ emitido reacciona con el oxígeno en el aire, a menudo con la ayuda de la luz solar y partículas contaminantes, para formar trióxido de azufre (SO₃).
- Este SO₃ es altamente reactivo y se disuelve rápidamente en el vapor de agua atmosférico (H₂O) para formar ácido sulfúrico (H₂SO₄).
- Este ácido, junto con el ácido nítrico formado a partir de los óxidos de nitrógeno, cae a la tierra disuelto en la lluvia, la nieve, la niebla o el rocío, creando lo que conocemos como deposición ácida.
Las consecuencias de la lluvia ácida son nefastas:
- Acidificación de Lagos y Ríos: Altera el pH del agua, volviéndola tóxica para muchas formas de vida acuática. Poblaciones enteras de peces, anfibios e insectos pueden desaparecer, rompiendo la cadena trófica.
- Daño a los Bosques: La lluvia ácida debilita los árboles al dañar sus hojas y al lixiviar (arrastrar) nutrientes vitales del suelo, como el calcio y el magnesio. Esto los hace más vulnerables a enfermedades, plagas y sequías.
- Corrosión de Materiales: Acelera el deterioro de edificios, estatuas y monumentos históricos, especialmente aquellos construidos con piedra caliza o mármol, disolviendo literalmente nuestro patrimonio cultural.
Un Enemigo Silencioso para la Salud Humana
La exposición al dióxido de azufre, incluso a corto plazo, puede tener efectos perjudiciales para la salud humana. El sistema respiratorio es el principal afectado. Al ser inhalado, el SO₂ irrita las vías respiratorias, provocando inflamación y una serie de síntomas como tos, producción de mucosidad y dificultad para respirar (disnea).
Los grupos de población más vulnerables son:
- Personas con asma: Son especialmente sensibles. La exposición a concentraciones incluso bajas de SO₂ puede desencadenar broncoespasmos severos, es decir, un estrechamiento repentino de las vías respiratorias que puede derivar en un ataque de asma agudo.
- Niños y ancianos: Sus sistemas respiratorios son más susceptibles a los efectos irritantes de los contaminantes.
- Personas con enfermedades respiratorias crónicas: Quienes padecen bronquitis crónica o enfisema ven agravada su condición.
Además, el SO₂ en la atmósfera puede contribuir a la formación de partículas finas (PM2.5), que son lo suficientemente pequeñas como para penetrar profundamente en los pulmones y pasar al torrente sanguíneo, asociándose con problemas cardiovasculares y un aumento de la mortalidad prematura.
Hacia un Aire Más Limpio: Estrategias de Control y Reducción
Afortunadamente, la concienciación sobre los peligros del SO₂ ha llevado a la implementación de regulaciones estrictas y al desarrollo de tecnologías eficaces para controlar sus emisiones.
- Uso de Combustibles con Bajo Contenido de Azufre: Una de las estrategias más directas es utilizar combustibles que naturalmente contienen menos azufre, como el gas natural, o procesar el carbón y el petróleo para eliminar gran parte del azufre antes de su combustión (desulfuración).
- Tecnologías de Control de Emisiones: La instalación de "lavadores de gases" o "scrubbers" en las chimeneas de centrales eléctricas e industrias es una de las medidas más efectivas. Estos sistemas hacen pasar los gases de escape a través de una sustancia, como una lechada de caliza, que reacciona con el SO₂ y lo convierte en un subproducto sólido (sulfato de calcio o yeso) que puede ser retirado de forma segura.
- Transición a Energías Renovables: La solución a largo plazo más sostenible es abandonar la dependencia de los combustibles fósiles. Las fuentes de energía como la solar, la eólica o la hidroeléctrica generan electricidad sin emitir dióxido de azufre ni otros contaminantes atmosféricos.
Preguntas Frecuentes sobre el Dióxido de Azufre
- ¿El dióxido de azufre tiene algún olor característico?
- Sí, tiene un olor muy distintivo, agudo y picante, que a menudo se compara con el de una cerilla o fósforo recién quemado. Este olor es detectable por los humanos incluso a bajas concentraciones.
- ¿Es seguro consumir alimentos que contienen sulfitos (derivados del SO₂)?
- Para la mayoría de la población, el consumo de alimentos con sulfitos en las cantidades autorizadas es seguro. Sin embargo, un pequeño porcentaje de personas, especialmente aquellas con asma, son sensibles a los sulfitos y pueden experimentar reacciones alérgicas o ataques de asma tras su consumo.
- ¿La lluvia ácida sigue siendo un problema grave en la actualidad?
- Gracias a las regulaciones implementadas en Norteamérica y Europa desde los años 80 y 90, el problema de la lluvia ácida ha disminuido significativamente en estas regiones. No obstante, sigue siendo una preocupación ambiental importante en partes de Asia y otras regiones del mundo con una industrialización rápida y controles de emisiones menos estrictos.
En conclusión, el dióxido de azufre encapsula a la perfección la complejidad de la era industrial. Es un compuesto que ha impulsado el desarrollo tecnológico y económico, pero a un coste ambiental y sanitario muy alto. Si bien hemos logrado avances significativos en la reducción de sus emisiones en muchas partes del mundo, la batalla no ha terminado. La vigilancia continua, la aplicación de tecnologías limpias y, sobre todo, una transición decidida hacia un modelo energético renovable son los únicos caminos para asegurar que el aire que respiramos sea limpio y seguro para las generaciones futuras, relegando los peores efectos del SO₂ a los libros de historia.
Si quieres conocer otros artículos parecidos a Dióxido de Azufre: Impacto Ambiental y Salud puedes visitar la categoría Contaminación.