10/06/2000
En el complejo entramado de la naturaleza, existen fuerzas y balances que, aunque invisibles a simple vista, determinan la salud y la supervivencia de ecosistemas enteros. Una de las más fundamentales y a la vez más sensibles es el pH. Este término, que para muchos puede sonar a una lejana clase de química, es en realidad un indicador vital que dicta las reglas del juego para cada ser vivo, desde la bacteria más pequeña en el suelo hasta la ballena más grande en el océano. El pH de un ambiente es crítico porque tiene un efecto directo y profundo sobre el funcionamiento de todas las enzimas, hormonas y proteínas que constituyen la maquinaria biológica de la vida. Un ligero desvío en esta escala puede significar la diferencia entre un ecosistema próspero y uno al borde del colapso.
¿Qué es Exactamente el pH? Desglosando la Química Ambiental
Para comprender su importancia, primero debemos saber qué es. El término pH significa potencial de hidrógeno y es, en esencia, una medida que nos indica el grado de acidez o alcalinidad de una disolución acuosa. Esta medida se basa en la concentración de iones de hidrógeno (H+) presentes. De forma sencilla:
- Sustancias Ácidas: Tienen una alta concentración de iones de hidrógeno (H+) y son capaces de cederlos.
- Sustancias Básicas o Alcalinas: Tienen una baja concentración de H+ y una alta concentración de iones hidroxilo (OH-), que pueden aceptar iones de hidrógeno.
Esta dinámica se mide en una escala logarítmica que va del 0 al 14:
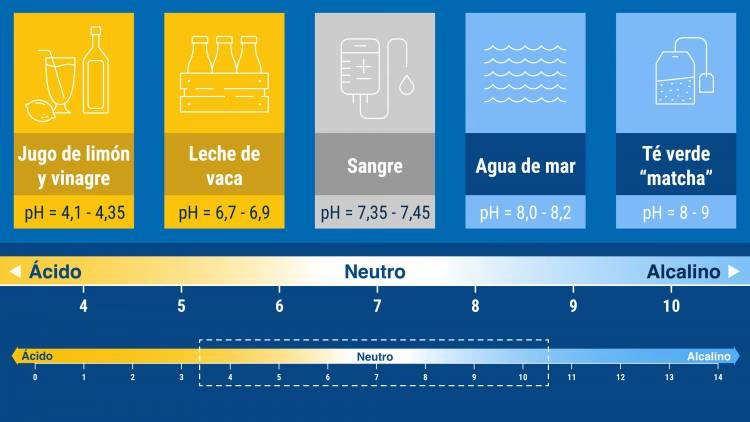
- pH 7: Se considera neutro (ejemplo: agua pura).
- pH menor a 7: Se considera ácido (ejemplo: jugo de limón, vinagre). Cuanto más bajo el número, mayor la acidez.
- pH mayor a 7: Se considera básico o alcalino (ejemplo: bicarbonato de sodio, lejía). Cuanto más alto el número, mayor la alcalinidad.
Es crucial entender que, al ser una escala logarítmica, un cambio de un solo punto (por ejemplo, de pH 6 a pH 5) representa un aumento de diez veces en la acidez. Este es el motivo por el cual pequeñas variaciones pueden tener consecuencias tan drásticas en el medio ambiente.
El pH del Suelo: El Fundamento de Nuestra Alimentación
El suelo no es solo tierra; es un ecosistema vibrante y complejo del cual depende la agricultura y, por ende, nuestra alimentación. El pH del suelo es uno de los factores más determinantes para su fertilidad. La mayoría de los cultivos prosperan en un rango de pH entre 6.0 y 7.5, considerado de ligeramente ácido a neutro. ¿Por qué este rango es tan importante?
La respuesta está en la disponibilidad de nutrientes. El pH del suelo controla las reacciones químicas que determinan si los nutrientes esenciales para las plantas (como el nitrógeno, fósforo, potasio, calcio y magnesio) están en una forma que las raíces puedan absorber. Fuera del rango óptimo, estos nutrientes pueden quedar "bloqueados" en el suelo, inaccesibles para las plantas aunque estén presentes físicamente.
Tabla Comparativa: Disponibilidad de Nutrientes según el pH del Suelo
| Rango de pH | Disponibilidad de Nutrientes | Consecuencias |
|---|---|---|
| Muy Ácido (Menor a 5.5) | Baja disponibilidad de Fósforo, Calcio, Magnesio. Alta solubilidad de metales tóxicos como Aluminio y Manganeso. | Toxicidad para las raíces, crecimiento deficiente de las plantas, baja productividad de los cultivos. |
| Óptimo (6.0 - 7.5) | Máxima disponibilidad de la mayoría de los macro y micronutrientes esenciales. | Plantas sanas, crecimiento vigoroso, cosechas abundantes y de calidad. |
| Alcalino (Mayor a 7.5) | Baja disponibilidad de Fósforo, Hierro, Manganeso, Zinc y Cobre. | Clorosis (hojas amarillas por falta de hierro), deficiencias nutricionales, crecimiento limitado. |
Factores como la roca madre sobre la que se forma el suelo, la descomposición de la materia orgánica y, de forma muy significativa, la contaminación atmosférica que causa la lluvia ácida, pueden alterar drásticamente el pH del suelo, comprometiendo la seguridad alimentaria y la salud de los bosques.
El Delicado Equilibrio del pH en el Agua
Los ecosistemas acuáticos, desde pequeños arroyos hasta vastos océanos, son extremadamente sensibles a los cambios de pH. El agua de mar, por ejemplo, es naturalmente ligeramente alcalina, con un pH promedio de alrededor de 8.1. Este valor es crucial para la vida marina, especialmente para los organismos que construyen conchas o esqueletos de carbonato de calcio, como los corales, los moluscos y ciertos tipos de plancton.
El fenómeno conocido como acidificación de los océanos es una de las consecuencias más graves del aumento de dióxido de carbono (CO2) en la atmósfera. Alrededor de un cuarto del CO2 que emitimos es absorbido por los océanos, donde reacciona con el agua para formar ácido carbónico, disminuyendo el pH del agua. Aunque el cambio parezca pequeño (se estima que el pH oceánico ha bajado 0.1 unidades desde la era preindustrial), representa un aumento del 30% en la acidez. Esto dificulta enormemente la capacidad de los organismos calcificadores para formar sus estructuras, amenazando la base de la cadena alimentaria marina y la existencia de los arrecifes de coral, los ecosistemas más biodiversos del planeta.
En los ecosistemas de agua dulce, como lagos y ríos, la lluvia ácida y los vertidos industriales pueden reducir el pH de forma catastrófica, volviendo el agua inhabitable para muchas especies de peces, anfibios e insectos, y alterando todo el equilibrio ecológico.

Cuando el Cielo se Vuelve Ácido: El pH del Aire
Si bien el aire en sí no tiene un pH, los contaminantes que contiene sí. Gases como el dióxido de azufre (SO2) y los óxidos de nitrógeno (NOx), liberados por la quema de combustibles fósiles en industrias y vehículos, reaccionan con el vapor de agua en la atmósfera para formar ácido sulfúrico y ácido nítrico. Estas sustancias regresan a la Tierra en forma de lluvia, nieve o niebla ácida.
La lluvia ácida tiene efectos devastadores:
- Acidifica lagos y ríos, matando la vida acuática.
- Daña los bosques al lixiviar los nutrientes del suelo y liberar aluminio tóxico.
- Corroe edificios, estatuas y monumentos históricos hechos de piedra caliza o mármol.
- Afecta la salud humana al contribuir a problemas respiratorios.
Preguntas Frecuentes (FAQ)
¿Cómo se puede medir el pH en el campo o en casa?
Existen métodos sencillos y accesibles. Las tiras reactivas de pH son económicas y fáciles de usar: se sumergen en la muestra (agua o una mezcla de suelo y agua destilada) y cambian de color, que luego se compara con una escala. Para mediciones más precisas, se utilizan medidores de pH digitales o "pH-metros".
¿Es posible corregir el pH de un suelo?
Sí, es una práctica común en la agricultura. Para subir el pH de un suelo demasiado ácido, los agricultores añaden enmiendas alcalinas como la cal (carbonato de calcio). Para bajar el pH de un suelo muy alcalino, se puede incorporar materia orgánica como el compost o añadir azufre elemental.
¿Toda la lluvia es ácida?
Técnicamente, incluso la lluvia no contaminada es ligeramente ácida, con un pH de alrededor de 5.6, debido a que el dióxido de carbono de la atmósfera se disuelve en ella. Sin embargo, el término "lluvia ácida" se refiere a la lluvia que es significativamente más ácida de lo normal (con un pH inferior a 5.0) debido a la contaminación industrial.
En conclusión, el pH es mucho más que un número en una escala; es un pilar fundamental que sostiene el equilibrio de todos los ecosistemas de nuestro planeta. Desde la fertilidad del suelo que nos alimenta hasta la salud de los océanos que regulan nuestro clima, todo depende de mantener este delicado balance. Comprender su importancia y el impacto de nuestras actividades sobre él es el primer paso para tomar conciencia y actuar en la protección de nuestro medio ambiente.
Si quieres conocer otros artículos parecidos a El pH: El Equilibrio Invisible de la Vida puedes visitar la categoría Ecología.
