06/03/2012
En la vasta y compleja ecuación del cambio climático y la degradación ambiental, existen actores silenciosos pero increíblemente destructivos. Entre ellos, los óxidos de azufre (SOx) ocupan un lugar protagónico. Este grupo de gases, liberado principalmente por actividades humanas, representa una de las formas más perniciosas de contaminación del aire, con efectos que van desde problemas respiratorios agudos hasta la acidificación de nuestros bosques y lagos. Comprender su origen, naturaleza y consecuencias es el primer paso para dimensionar la magnitud del problema y buscar soluciones efectivas para mitigar su impacto en nuestro planeta.
- ¿Qué son exactamente los Óxidos de Azufre (SOx)?
- Fuentes de Emisión: ¿De Dónde Proviene esta Amenaza?
- El Dióxido de Azufre (SO₂): El Villano Principal
- El Trióxido de Azufre (SO₃): Un Agente Aún Más Peligroso
- Tabla Comparativa: Dióxido de Azufre (SO₂) vs. Trióxido de Azufre (SO₃)
- Impactos en la Salud y el Medio Ambiente
- Manejo, Seguridad y Primeros Auxilios
- Preguntas Frecuentes (FAQ)
¿Qué son exactamente los Óxidos de Azufre (SOx)?
Cuando hablamos de óxidos de azufre, nos referimos a un grupo de compuestos químicos gaseosos formados por azufre y oxígeno. Los dos más relevantes en el contexto de la contaminación atmosférica son el dióxido de azufre (SO₂) y el trióxido de azufre (SO₃). Aunque ambos son nocivos, el dióxido de azufre es el más común y se considera el contaminante primario, ya que el SO₃ se forma generalmente a partir de la oxidación del SO₂ en la atmósfera. Juntos, son los precursores directos de uno de los fenómenos ambientales más conocidos: la lluvia ácida.
Fuentes de Emisión: ¿De Dónde Proviene esta Amenaza?
Más de la mitad de las emisiones de SOx que llegan a nuestra atmósfera son de origen antropogénico, es decir, causadas por la actividad humana. La fuente principal es, sin lugar a dudas, la quema de combustibles fósiles (carbón y petróleo) que contienen azufre en su composición. Este proceso es fundamental en:
- Centrales termoeléctricas: La generación de electricidad quemando carbón o petróleo de baja calidad, ricos en azufre, libera enormes cantidades de SO₂. En España, por ejemplo, zonas con importantes instalaciones de este tipo, como Galicia y Aragón, han sido históricamente focos de emisión.
- Procesos industriales: La industria metalúrgica es otra gran fuente, ya que muchos metales se extraen de minerales en forma de sulfuros. Al procesarlos, el azufre se combina con el oxígeno y se libera como SO₂.
- Transporte: Los motores diésel de barcos y, en menor medida, de camiones, también contribuyen a las emisiones, aunque las regulaciones sobre el contenido de azufre en los combustibles han ayudado a reducir su impacto.
Por otro lado, la naturaleza también produce óxidos de azufre, principalmente a través de las erupciones volcánicas, que pueden inyectar cantidades masivas de SO₂ en la atmósfera en un corto período de tiempo.
El Dióxido de Azufre (SO₂): El Villano Principal
El SO₂ es un gas incoloro, no inflamable, pero con un olor fuerte e irritante, similar al de una cerilla recién encendida. Su vida en la atmósfera es relativamente corta, de dos a cuatro días, tiempo durante el cual puede viajar cientos de kilómetros. Durante este periodo, una parte se deposita en la superficie, mientras que el resto sufre una transformación química que agrava el problema.
Propiedades y Características del SO₂
- Fórmula química: SO₂
- Aspecto: Gas incoloro de olor penetrante.
- Solubilidad: Es soluble en agua, formando una disolución ácida (ácido sulfuroso, H₂SO₃), lo que explica su papel en la lluvia ácida.
- Reactividad: Con el tiempo, y en presencia de luz solar y otros catalizadores en el aire, se oxida para formar trióxido de azufre (SO₃).
Usos Industriales del SO₂
A pesar de ser un contaminante, el SO₂ tiene aplicaciones industriales importantes. Es un paso intermedio crucial en la fabricación del ácido sulfúrico, uno de los productos químicos más utilizados en el mundo. Además, en estado líquido, es un buen disolvente y se utiliza en la industria alimentaria como conservante y antioxidante (conocido como E220) en productos como vinos, zumos y frutos secos, gracias a sus propiedades para inhibir el crecimiento de bacterias y mohos.
El Trióxido de Azufre (SO₃): Un Agente Aún Más Peligroso
El SO₃, también conocido como anhídrido sulfúrico, es un compuesto mucho más reactivo y agresivo que el SO₂. En condiciones normales, es un sólido de aspecto fibroso o de agujas blancas. Su principal relevancia ambiental es que reacciona de forma casi explosiva con el agua para formar ácido sulfúrico (H₂SO₄), el componente principal de la lluvia ácida.

Reactividad Extrema y Peligrosidad
El trióxido de azufre es un oxidante fuerte y su manejo es extremadamente peligroso. Reacciona violentamente no solo con el agua, sino también con bases, metales y una amplia gama de compuestos orgánicos, pudiendo causar incendios y explosiones. Absorbe la humedad del aire con gran rapidez, emitiendo densos humos blancos de ácido sulfúrico. Es altamente corrosivo para los tejidos vivos y los metales.
Tabla Comparativa: Dióxido de Azufre (SO₂) vs. Trióxido de Azufre (SO₃)
| Característica | Dióxido de Azufre (SO₂) | Trióxido de Azufre (SO₃) |
|---|---|---|
| Estado a 25°C | Gas incoloro | Sólido cristalino incoloro |
| Fuente Principal | Combustión de fósiles, volcanes | Oxidación del SO₂ en la atmósfera |
| Reactividad con Agua | Moderada, forma ácido sulfuroso (H₂SO₃) | Extremadamente violenta, forma ácido sulfúrico (H₂SO₄) |
| Principal Impacto | Irritante respiratorio, precursor de SO₃ | Agente corrosivo y principal causante de la lluvia ácida |
| Olor | Fuerte e irritante (similar a cerilla quemada) | Asfixiante |
Impactos en la Salud y el Medio Ambiente
Efectos en la Salud Humana
La exposición a los óxidos de azufre es perjudicial para la salud. El SO₂ es un gas irritante que afecta principalmente al sistema respiratorio.
- Inhalación: Provoca irritación de las mucosas, tos y broncoconstricción. Las personas con asma son especialmente sensibles, y la exposición puede desencadenar ataques severos. Concentraciones altas pueden causar bronquitis, espasmos y, en casos extremos, parada respiratoria.
- Contacto: El SO₃ y el ácido sulfúrico que forma son extremadamente corrosivos. Causan quemaduras graves en la piel y los ojos. La ingestión es devastadora, provocando quemaduras severas en boca, esófago y estómago. El SO₂ líquido se evapora rápidamente y puede causar congelación por contacto.
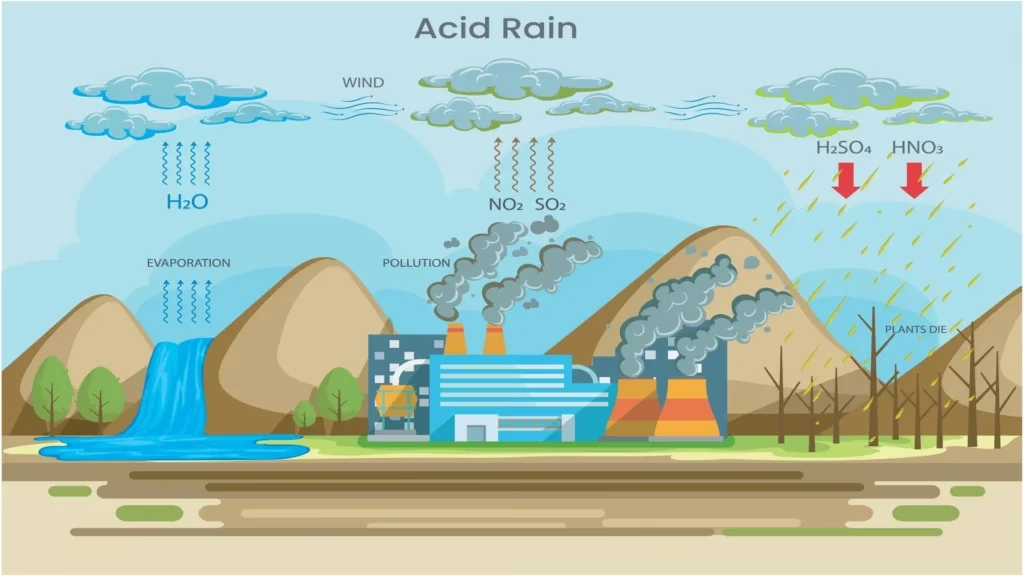
Impacto Ambiental: La Devastadora Lluvia Ácida
El efecto ambiental más grave de los SOx es, sin duda, la lluvia ácida. Cuando el SO₂ y el SO₃ se combinan con el agua en las nubes, forman ácido sulfúrico y sulfuroso. Esta lluvia, nieve o niebla acidificada cae a la tierra con consecuencias nefastas:
- Acidificación de aguas: Lagos y ríos se vuelven demasiado ácidos para sostener la vida, provocando la muerte de peces y otros organismos acuáticos.
- Daño a los bosques: La lluvia ácida debilita los árboles, dañando sus hojas, limitando su crecimiento y haciéndolos más vulnerables a enfermedades, plagas y heladas.
- Corrosión de materiales: Acelera el deterioro de edificios, estatuas y monumentos, especialmente los construidos con piedra caliza o mármol. También corroe estructuras metálicas.
Manejo, Seguridad y Primeros Auxilios
Debido a su toxicidad, el manejo de los óxidos de azufre requiere estrictas medidas de seguridad. Es clasificado como tóxico por inhalación (R23) y causa quemaduras (R34). En caso de exposición accidental, es crucial actuar rápidamente:
- Contacto con los ojos: Enjuagar inmediatamente con abundante agua durante al menos 15 minutos, manteniendo los párpados abiertos, y buscar atención médica de inmediato.
- Contacto con la piel: Retirar la ropa contaminada y lavar la zona afectada con agua y jabón suave. Si la exposición fue a SO₃ o SO₂ líquido, se debe tratar como una quemadura química o por congelación y buscar ayuda médica.
- Inhalación: Trasladar a la víctima a un lugar con aire fresco. Si la respiración es difícil, administrar oxígeno. Si no respira, realizar reanimación, teniendo cuidado de que el material no sea tóxico para el rescatador. Buscar atención médica urgente en todos los casos.
Preguntas Frecuentes (FAQ)
¿La contaminación por óxidos de azufre solo proviene de las fábricas?
No. Si bien las centrales eléctricas y la industria pesada son las mayores fuentes humanas, las erupciones volcánicas son una fuente natural muy importante. Además, el transporte marítimo y los vehículos diésel pesados también contribuyen.
¿Qué es exactamente la lluvia ácida y cómo la causan los SOx?
La lluvia ácida es cualquier forma de precipitación (lluvia, nieve, niebla) que es más ácida de lo normal. Se forma cuando el dióxido de azufre (SO₂) y los óxidos de nitrógeno (NOx) reaccionan en la atmósfera con el agua, el oxígeno y otras sustancias químicas para formar ácido sulfúrico y nítrico. Estos ácidos se disuelven en las gotas de agua de las nubes y caen a la tierra.
¿Se está haciendo algo para reducir las emisiones de SOx?
Sí. A nivel global, se han implementado numerosas regulaciones. Estas incluyen el uso de combustibles con bajo contenido de azufre, la instalación de tecnologías de desulfuración de gases en chimeneas industriales (conocidas como "scrubbers") y la transición hacia fuentes de energía más limpias y renovables. Gracias a estas medidas, las emisiones han disminuido significativamente en muchas regiones, aunque sigue siendo un problema en países con regulaciones más laxas o alta dependencia del carbón.
Si quieres conocer otros artículos parecidos a Óxidos de Azufre: El Contaminante Invisible puedes visitar la categoría Contaminación.

