19/04/2006
En la industria farmacéutica, el empaque es mucho más que una simple capa protectora; es un componente crítico que salvaguarda la seguridad, eficacia e integridad del medicamento. La contaminación durante el proceso de envasado puede tener consecuencias devastadoras, comprometiendo la calidad del producto, poniendo en riesgo la salud del paciente y resultando en graves incumplimientos regulatorios. Las Buenas Prácticas de Manufactura (BPM o GMP por sus siglas en inglés) establecen estándares rigurosos para los procesos de empaque, diseñados para ayudar a los fabricantes a eliminar los riesgos de contaminación y entregar productos farmacéuticos seguros y de alta calidad al mercado.
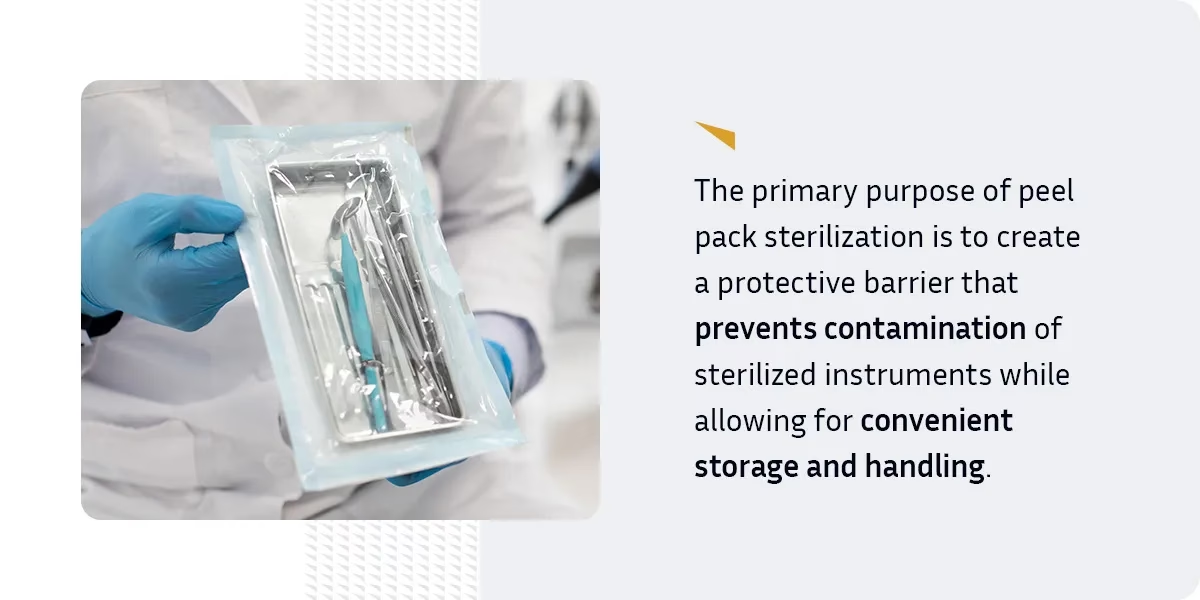
- Comprendiendo las Fuentes de Contaminación en el Empaque
- Guía Práctica para un Empaque Libre de Contaminación bajo Normas BPM
- Paso 1: Diseñar un Entorno de Empaque Controlado
- Paso 2: Utilizar Materiales de Empaque Conformes a las BPM
- Tabla Comparativa: Materiales de Empaque Farmacéutico Comunes
- Paso 3: Validar los Procesos de Empaque
- Paso 4: Capacitar al Personal en Estándares BPM
- Paso 5: Implementar un Control de Calidad Robusto
- Preguntas Frecuentes (FAQ)
- Conclusión: Hacia un Empaque de Contaminación Cero
Comprendiendo las Fuentes de Contaminación en el Empaque
Para implementar medidas preventivas eficaces, es fundamental primero identificar y comprender las fuentes comunes de contaminación que pueden surgir durante la producción de empaques. Un enfoque proactivo comienza con el conocimiento.
Contaminación Microbiana
Bacterias, hongos, levaduras y otros microorganismos pueden contaminar tanto los materiales de empaque como los productos terminados. Este riesgo es especialmente alto en entornos que requieren esterilidad. La presencia de microbios puede degradar el producto, reducir su eficacia o, en el peor de los casos, causar infecciones graves en los pacientes.
Contaminación por Partículas
El polvo, las fibras de la ropa, fragmentos de materiales de empaque, partículas metálicas del equipo o cualquier otro material ajeno pueden introducirse en el producto final. Estas partículas no solo comprometen la pureza del medicamento, sino que también pueden causar reacciones adversas si se administran, especialmente en productos inyectables.
Contaminación Cruzada
La contaminación cruzada ocurre cuando hay una mezcla accidental entre diferentes productos, lotes o materiales de empaque. Esto suele ser el resultado de una segregación inadecuada, procedimientos de limpieza deficientes entre lotes o errores de etiquetado. Las consecuencias pueden variar desde una dosis incorrecta hasta la exposición de un paciente a un alérgeno o a un fármaco que no debería recibir.

Contaminación Química
Residuos de agentes de limpieza, desinfectantes, lubricantes de maquinaria u otros productos químicos utilizados en el área de producción pueden transferirse a los materiales de empaque o directamente al producto. Esta transferencia química puede alterar la composición del fármaco, afectar su estabilidad o introducir sustancias tóxicas.
Guía Práctica para un Empaque Libre de Contaminación bajo Normas BPM
Adoptar un enfoque sistemático y basado en las directrices de las BPM es la única forma de garantizar un proceso de empaque seguro y controlado. A continuación, se detallan los pasos cruciales a seguir.
Paso 1: Diseñar un Entorno de Empaque Controlado
Un ambiente controlado es la primera línea de defensa contra la contaminación. Esto implica la creación de áreas específicas diseñadas para minimizar la exposición a contaminantes.
- Implementar Estándares de Salas Blancas (Cleanrooms): Para productos estériles o de alto riesgo, es obligatorio el uso de salas blancas con clasificaciones ISO apropiadas (como ISO 7 o ISO 8). Estas salas cuentan con filtros HEPA (High-Efficiency Particulate Air) que purifican el aire, mantienen una presión de aire positiva para evitar la entrada de contaminantes externos y exigen estrictos protocolos de vestimenta para todo el personal.
- Monitoreo Ambiental Constante: Es vital monitorear y registrar regularmente parámetros como la temperatura, la humedad y los niveles de partículas en el aire. Esto asegura que las condiciones ambientales se mantengan dentro de los límites aceptables de manera consistente.
- Control de Acceso: El acceso a las áreas de empaque debe estar restringido únicamente al personal autorizado y debidamente capacitado, minimizando así la introducción de contaminantes desde el exterior.
Paso 2: Utilizar Materiales de Empaque Conformes a las BPM
La calidad y el manejo de los materiales de empaque tienen un impacto directo en el riesgo de contaminación.

- Seleccionar Proveedores de Alta Calidad: Asegúrese de que todos los materiales de empaque (viales, blísteres, frascos, etc.) cumplan con las especificaciones de las BPM y sean compatibles con el producto farmacéutico. La elección del material es crucial para proteger el medicamento.
- Inspección Rigurosa a la Recepción: Realice inspecciones visuales y funcionales de todos los materiales entrantes para identificar defectos, daños o cualquier signo de contaminación antes de que ingresen al almacén.
- Almacenamiento Adecuado: Los materiales de empaque deben almacenarse en áreas limpias, secas y segregadas para prevenir la contaminación, la degradación y las confusiones.
Tabla Comparativa: Materiales de Empaque Farmacéutico Comunes
| Material | Propiedades Clave | Usos Comunes |
|---|---|---|
| Vidrio | Alta inercia química, transparencia, barrera impermeable. | Viales, ampollas, jeringas para productos inyectables y sensibles. |
| Blísteres (Plástico/Aluminio) | Excelente protección contra la humedad y el oxígeno, dosificación individual. | Comprimidos, cápsulas y otras formas farmacéuticas sólidas. |
| Contenedores de Plástico (HDPE, PET) | Ligeros, duraderos, resistentes a la rotura, versátiles. | Líquidos orales, jarabes, cremas y productos semisólidos. |
Paso 3: Validar los Procesos de Empaque
La validación de procesos es la prueba documentada de que un proceso de empaque produce consistentemente un producto que cumple con las especificaciones predeterminadas y los atributos de calidad.
- Validación de Equipos y Procesos: Todos los equipos y procesos, incluyendo el sellado, etiquetado y ensamblaje, deben ser validados. Las pruebas deben incluir la verificación de la integridad del sello para blísteres y viales, inspecciones visuales para defectos y pruebas funcionales de características de seguridad como los sellos a prueba de manipulaciones.
- Mantenimiento Preventivo: Establezca un calendario de mantenimiento preventivo para todos los equipos de empaque. Esto previene averías que podrían comprometer el proceso y evita la contaminación por componentes desgastados.
- Automatización: Los sistemas de empaque automatizados reducen la intervención humana, lo que minimiza significativamente el riesgo de contaminación y errores operativos.
Paso 4: Capacitar al Personal en Estándares BPM
El personal bien capacitado es el pilar para mantener procesos de empaque libres de contaminación. El error humano es uno de los mayores riesgos.
- Formación Específica por Rol: Capacite al personal sobre sus funciones específicas, enfatizando los riesgos de contaminación, las directrices de las BPM y el funcionamiento correcto del equipo.
- Reforzar Protocolos de Higiene: Asegúrese de que todo el personal se adhiera a prácticas de higiene estrictas, incluyendo el lavado de manos, el uso correcto de la indumentaria de protección y evitar el contacto innecesario con los materiales.
- Cursos de Actualización Periódicos: Ofrezca sesiones de capacitación regulares para mantener al personal actualizado sobre nuevas tecnologías, regulaciones o estrategias de prevención de la contaminación.
Paso 5: Implementar un Control de Calidad Robusto
El control de calidad es esencial para identificar y corregir los riesgos de contaminación en tiempo real.
- Inspecciones en Proceso: Realice inspecciones continuas durante las operaciones de empaque para detectar y corregir problemas de inmediato.
- Tecnologías de Inspección Avanzadas: Implemente sistemas de inspección automatizados, como cámaras de visión, para verificar la contaminación por partículas, la precisión de las etiquetas y la integridad del sello a una velocidad y precisión que superan la capacidad humana.
- Documentación Detallada: Documente todas las actividades de control de calidad, incluyendo resultados de inspección, desviaciones y acciones correctivas. Esta documentación es crucial para demostrar el cumplimiento durante las auditorías.
Preguntas Frecuentes (FAQ)
¿Qué son las BPM (GMP) y por qué son cruciales en el empaque farmacéutico?
Las Buenas Prácticas de Manufactura (BPM) son un conjunto de normativas y directrices que aseguran que los productos se fabriquen y controlen de forma consistente según los estándares de calidad. En el empaque, son cruciales porque el envase es la última barrera que protege el medicamento, y cualquier fallo puede afectar directamente la seguridad y eficacia del producto final.

¿Cuál es la diferencia entre contaminación cruzada y contaminación química?
La contaminación cruzada se refiere a la transferencia de un producto farmacéutico (o sus ingredientes) a otro. Por ejemplo, si residuos de un antibiótico permanecen en una línea de envasado y contaminan un lote de analgésicos. La contaminación química, por otro lado, implica la introducción de sustancias no farmacéuticas, como residuos de agentes de limpieza, lubricantes o vapores.
¿Qué son las salas blancas (cleanrooms) y cómo funcionan?
Las salas blancas son entornos controlados diseñados para mantener niveles extremadamente bajos de contaminantes como polvo, partículas en el aire y microorganismos. Funcionan mediante un sistema de filtración de aire de alta eficiencia (HEPA), manteniendo una presión de aire positiva para que el aire limpio salga y el aire exterior contaminado no pueda entrar, y exigiendo protocolos estrictos de vestimenta y comportamiento para el personal.
Conclusión: Hacia un Empaque de Contaminación Cero
Prevenir la contaminación durante la producción de empaques farmacéuticos es un pilar fundamental para garantizar la seguridad del medicamento, el cumplimiento normativo y la confianza del paciente. Al comprender los riesgos, diseñar entornos controlados, validar procesos, capacitar al personal e implementar controles de calidad robustos, los fabricantes pueden cumplir con las exigentes normativas BPM. Este es un esfuerzo continuo que requiere vigilancia, documentación meticulosa e innovación constante para proteger la salud pública en un mercado global cada vez más complejo.
Si quieres conocer otros artículos parecidos a Empaque Farmacéutico: Guía Contra la Contaminación puedes visitar la categoría Ecología.

