07/07/2011
La terapia génica, especialmente aquella que utiliza vectores virales adeno-asociados (AAV), representa una de las fronteras más prometedoras de la medicina moderna. Estos diminutos vehículos biológicos son capaces de entregar material genético directamente a las células para corregir enfermedades de origen genético. Sin embargo, detrás de esta increíble promesa se esconde un desafío monumental: la producción. El proceso de fabricación de vectores AAV es increíblemente complejo y, como en cualquier proceso de alta tecnología, pueden generarse subproductos no deseados. Estas impurezas, si no se controlan y eliminan adecuadamente, pueden comprometer tanto la eficacia del tratamiento como la seguridad del paciente. Comprender qué son estas impurezas, cómo se originan y qué impacto tienen es fundamental para el avance seguro y responsable de la terapia génica.
¿Qué Son Exactamente las Impurezas en un Lote de AAV?
Cuando hablamos de impurezas en el contexto de la producción de AAV, nos referimos a cualquier sustancia presente en el producto final que no sea el vector AAV terapéutico completo y funcional. Estas impurezas se pueden clasificar en dos grandes categorías:
- Impurezas relacionadas con el proceso: Son aquellas que se introducen durante las fases de fabricación y purificación. Incluyen proteínas de la célula huésped (HCPs) donde se produjeron los virus, ADN de la célula huésped (HCDNA), componentes del medio de cultivo o sustancias utilizadas en la purificación.
- Impurezas relacionadas con el producto: Son variantes del propio vector AAV que se desvían de la forma deseada. Son particularmente difíciles de eliminar porque se parecen mucho al producto correcto en tamaño y composición. Es en estas donde nos centraremos, ya que representan un desafío único para los desarrolladores de terapias génicas.
Los Principales Tipos de Impurezas Relacionadas con el Producto
Dentro de un lote de producción de AAV, podemos encontrar una mezcla heterogénea de partículas. El objetivo es maximizar la proporción de vectores "completos", es decir, aquellos que contienen el gen terapéutico correcto. Las impurezas más comunes son:
1. Cápsides Vacías (Empty Capsids)
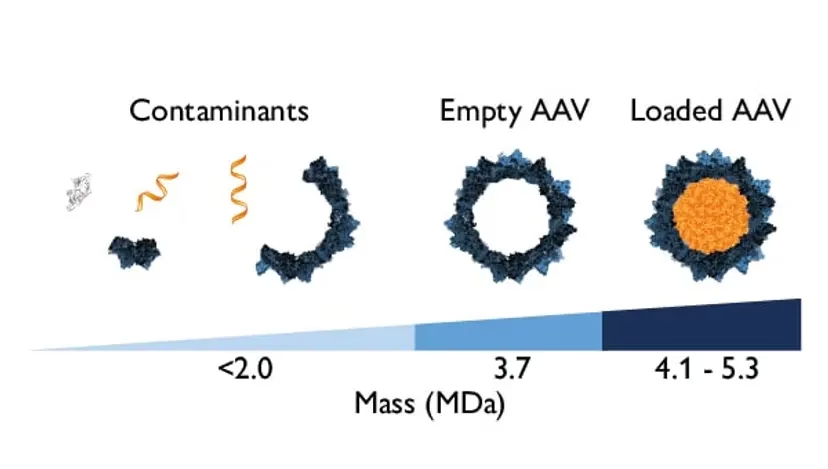
Probablemente la impureza más abundante y conocida. Como su nombre indica, son cápsides virales perfectamente ensambladas pero que carecen del material genético en su interior. Durante el proceso de producción, el ensamblaje de la cubierta proteica (cápside) y el empaquetamiento del ADN son dos procesos que, aunque relacionados, no están perfectamente sincronizados. Esto a menudo resulta en la formación de más cápsides que genomas disponibles para ser empaquetados.
El impacto de las cápsides vacías es un tema de debate. Por un lado, no aportan ningún beneficio terapéutico y diluyen la dosis efectiva, lo que podría obligar a administrar un mayor número de partículas totales al paciente para lograr el efecto deseado. Una alta concentración de estas partículas proteicas podría, teóricamente, desencadenar una respuesta inmune no deseada sin ofrecer la contrapartida de la corrección génica. Curiosamente, algunos estudios sugieren que una cierta proporción de cápsides vacías podría ser beneficiosa, actuando como señuelos para el sistema inmunitario y permitiendo que más vectores completos lleguen a su destino.
2. Cápsides Parcialmente Llenas (Partial Capsids)
Estas son cápsides que han comenzado el proceso de empaquetamiento del genoma pero que no lo han completado. El resultado es una partícula que contiene solo un fragmento del ADN terapéutico. Estas impurezas son ineficaces, ya que no pueden expresar la proteína terapéutica completa y funcional. Además, existe la preocupación de que puedan expresar proteínas truncadas o aberrantes, con consecuencias biológicas desconocidas. La presencia de genomas parciales es un indicador de que el proceso de empaquetamiento del ADN puede no estar optimizado.
3. Cápsides con ADN Contaminante
Quizás una de las impurezas más preocupantes desde el punto de vista de la seguridad. Durante la producción, la maquinaria de empaquetamiento del AAV puede encapsidar accidentalmente fragmentos de ADN contaminante en lugar del genoma terapéutico. Este ADN puede provenir de dos fuentes principales:
- ADN de la Célula Huésped: Fragmentos del genoma de las células utilizadas para la producción (generalmente células HEK293 o células de insecto Sf9).
- ADN de Plásmidos: Secuencias de los plásmidos utilizados para introducir los genes necesarios para la producción del AAV. Se ha demostrado que secuencias específicas de estos plásmidos, como las que se encuentran cerca del promotor P5 en el plásmido Rep-Cap, son empaquetadas preferentemente.
El riesgo asociado a estas partículas es que podrían introducir genes no deseados en las células del paciente, como genes de resistencia a antibióticos o secuencias que podrían activar oncogenes, aunque este riesgo es considerado bajo pero no nulo.
4. Cápsides con Estequiometría Incorrecta
La cápside de un AAV está compuesta por 60 proteínas virales (VP) de tres tipos: VP1, VP2 y VP3. La proporción generalmente aceptada es de 1:1:10. Sin embargo, estudios recientes han demostrado que esta proporción puede variar significativamente dependiendo de las condiciones de producción. Una desviación de la estequiometría ideal puede afectar la estabilidad de la cápside, su capacidad para infectar células (tropismo) y, en última instancia, la potencia del fármaco. Por tanto, una composición proteica incorrecta puede ser considerada una forma sutil de impureza relacionada con el producto.
La Lucha por la Pureza: Métodos Analíticos para Detectar Impurezas
Identificar y cuantificar estas impurezas es un paso crítico y no negociable en el desarrollo de cualquier terapia génica. La pureza del producto final debe ser demostrada ante las agencias reguladoras. Para ello, los científicos utilizan un arsenal de técnicas analíticas avanzadas, cada una con sus fortalezas y debilidades.
Tabla Comparativa de Técnicas Analíticas
| Técnica Analítica | Principio de Funcionamiento | Impurezas que Detecta | Ventajas | Desventajas |
|---|---|---|---|---|
| Ultracentrifugación Analítica (AUC) | Separa partículas basado en su velocidad de sedimentación en una fuerza centrífuga. Las cápsides llenas son más densas que las vacías. | Vacías, parciales, llenas, agregados. | Alta resolución y precisión. Considerado un "estándar de oro". | Bajo rendimiento, requiere grandes cantidades de muestra, equipo especializado y costoso. |
| Microscopía Electrónica de Transmisión (TEM) | Visualización directa de partículas. Las cápsides llenas aparecen oscuras y las vacías claras. | Vacías, llenas, morfología, agregados. | Proporciona confirmación visual. | Bajo rendimiento, preparación de muestra compleja, puede ser difícil distinguir parciales. |
| Cromatografía de Intercambio Aniónico (AEX) | Separa partículas basado en diferencias sutiles de carga superficial entre cápsides vacías y llenas. | Vacías y llenas. | Alto rendimiento, buena precisión. | Requiere optimización para cada serotipo y producto. Puede no resolver bien las parciales. |
| Espectrometría de Masas con Detección de Carga (CDMS) | Mide la masa de partículas individuales con alta precisión, distinguiendo la masa extra del ADN. | Vacías, parciales, llenas y sobrellenadas. | Resolución y precisión muy altas. | Tecnología emergente, equipo muy especializado y costoso. |
| Fotometría de Masas | Mide la masa de partículas individuales a medida que aterrizan en una superficie, basándose en la dispersión de la luz. | Vacías, parciales, llenas, agregados. | Rápida, requiere muy poca muestra, fácil de usar. | Menor resolución que CDMS. |
Preguntas Frecuentes (FAQ)
¿Son peligrosas las impurezas en las terapias génicas con AAV?
El principal objetivo es minimizar cualquier riesgo potencial. Si bien no se han reportado efectos adversos graves directamente atribuidos a impurezas como cápsides vacías, la preocupación principal es la inmunogenicidad. Una alta carga de proteínas virales (de cápsides vacías y llenas) podría provocar una respuesta inmune que neutralice el vector y reduzca la eficacia del tratamiento o impida futuras administraciones. Las impurezas de ADN contaminante conllevan un riesgo teórico, aunque bajo, de efectos genotóxicos a largo plazo.
¿Es posible producir un lote de AAV 100% puro?
Actualmente, no es posible alcanzar una pureza del 100%. El objetivo de los procesos de desarrollo y purificación es reducir las impurezas a niveles tan bajos como sea posible y mantener una consistencia lote a lote. Las agencias reguladoras establecen umbrales aceptables para diferentes tipos de impurezas, los cuales deben cumplirse para que un producto sea aprobado.
¿Qué diferencia hay entre impurezas relacionadas con el producto y con el proceso?
La diferencia clave es su origen. Las impurezas relacionadas con el proceso son materiales extraños al producto (ej. proteínas de la célula que fabricó el virus). Las impurezas relacionadas con el producto son variantes del propio producto (ej. un virus sin su carga genética). Estas últimas son mucho más difíciles de separar porque sus propiedades físicas y químicas son muy similares a las del producto deseado.
¿Por qué se forman cápsides vacías en un lote de producción?
La formación de cápsides vacías es una consecuencia natural de la biología de la producción de AAV. El ensamblaje de las proteínas de la cápside es un proceso muy eficiente. Sin embargo, la replicación y disponibilidad del genoma viral que debe ser empaquetado puede ser un paso limitante. Como resultado, a menudo se producen más "contenedores" (cápsides) que "contenido" (genomas), llevando a la acumulación de partículas vacías.
Conclusión: La Calidad como Pilar de la Terapia Génica
El camino de la terapia génica desde el laboratorio hasta la clínica está pavimentado con desafíos científicos y técnicos. La caracterización y el control de las impurezas relacionadas con el producto no son meros detalles técnicos; son el núcleo de la garantía de calidad, seguridad y eficacia de estos revolucionarios tratamientos. A medida que la tecnología avanza, también lo hacen las herramientas analíticas que nos permiten ver con mayor claridad la composición de estos complejos productos biológicos. Asegurar la máxima pureza posible no es solo un requisito regulatorio, sino un compromiso ético con los pacientes que depositan su esperanza en la promesa de la medicina genética.
Si quieres conocer otros artículos parecidos a Impurezas en Vectores AAV: El Lado Oculto puedes visitar la categoría Ecología.