15/05/1999
En nuestro día a día, estamos rodeados de mezclas que, a simple vista, parecen homogéneas pero que a nivel microscópico revelan una complejidad fascinante. Hablamos de la leche que añadimos al café, la niebla que reduce la visibilidad en una mañana fría, la pintura con la que decoramos nuestras paredes o incluso el citoplasma de nuestras propias células. Todas ellas tienen algo en común: son sistemas coloidales. Un coloide es un tipo de mezcla intermedia entre una solución verdadera (como el agua con sal) y una suspensión grosera (como la arena en el agua). Comprender su naturaleza, propiedades y comportamiento es adentrarse en un campo de la fisicoquímica con inmensas aplicaciones prácticas e industriales.
¿Qué Define a un Sistema Coloidal?
Un sistema coloidal, también conocido como dispersión coloidal, se compone de dos fases distintas: una fase dispersa y una fase continua (o medio dispersante). La fase dispersa consiste en partículas diminutas, cuyo tamaño suele oscilar entre 1 y 1000 nanómetros (millonésimas de milímetro). Estas partículas son más grandes que las moléculas individuales de una solución, pero lo suficientemente pequeñas como para no sedimentar por la fuerza de la gravedad y para permanecer suspendidas indefinidamente en la fase continua.
La clave de su comportamiento único reside precisamente en este tamaño de partícula. No son lo bastante grandes para ser vistas a simple vista ni para ser filtradas con papel de filtro común, pero sí lo suficientemente grandes como para dispersar la luz y exhibir fenómenos físicos particulares que los distinguen de otros tipos de mezclas.
Clasificación y Tipos de Coloides
Los coloides se pueden clasificar de diversas maneras, pero una de las más comunes se basa en la afinidad entre la fase dispersa y la fase continua.
- Coloides Liófilos (amantes del disolvente): En estos sistemas, existe una fuerte atracción entre las partículas de la fase dispersa y las moléculas del medio dispersante. Son termodinámicamente estables y se forman de manera espontánea. Un ejemplo clásico es la gelatina disuelta en agua caliente. Cuando el medio es agua, se les denomina hidrófilos.
- Coloides Liófobos (temerosos del disolvente): Aquí, la atracción entre las fases es muy débil o inexistente. Estos coloides son inherentemente inestables y requieren de agentes estabilizadores y métodos de preparación específicos para formarse y perdurar. Las dispersiones de metales como el oro o la plata en agua son ejemplos típicos. Si el medio es agua, se les llama hidrófobos.
Otra forma fundamental de clasificarlos es según el estado de agregación (sólido, líquido o gas) de sus fases. Esta clasificación da lugar a una gran variedad de sistemas que encontramos constantemente.
Tabla de Tipos de Coloides según sus Fases
| Fase Dispersa | Fase Continua | Nombre del Coloide | Ejemplos Cotidianos |
|---|---|---|---|
| Sólido | Gas | Aerosol sólido | Humo, polvo en suspensión |
| Líquido | Gas | Aerosol líquido | Niebla, bruma, desodorante en spray |
| Gas | Líquido | Espuma | Espuma de afeitado, nata montada, espuma de cerveza |
| Líquido | Líquido | Emulsión | Leche, mayonesa, cremas cosméticas, aderezos |
| Sólido | Líquido | Sol | Pinturas, tintas, sangre, almidón en agua |
| Gas | Sólido | Espuma Sólida | Piedra pómez, merengue seco, poliestireno expandido (corcho blanco) |
| Líquido | Sólido | Gel | Gelatina, gominolas, queso, gel de sílice |
| Sólido | Sólido | Sol Sólido | Cristales de rubí (óxido de cromo en alúmina), vidrio coloreado |
Propiedades Únicas que Definen a los Coloides
El comportamiento de los coloides se rige por una serie de propiedades características que los hacen tan especiales y útiles.
Efecto Tyndall
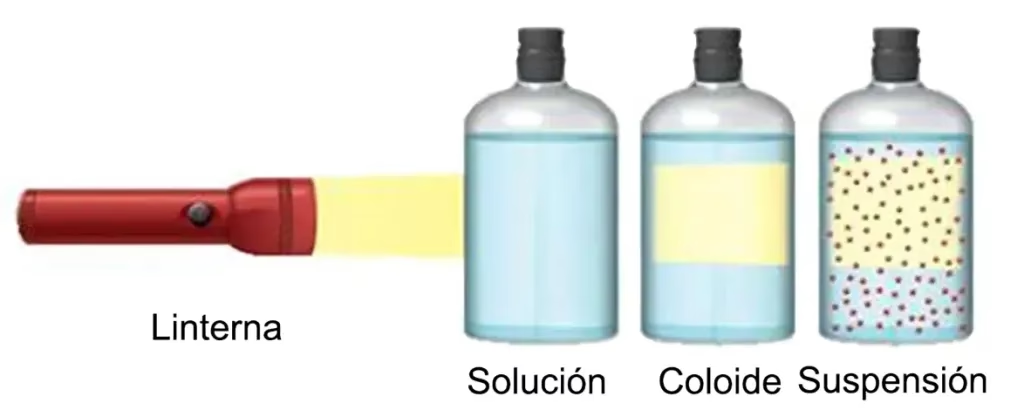
Quizás la propiedad óptica más distintiva. Cuando un haz de luz atraviesa un sistema coloidal, las partículas dispersas son lo suficientemente grandes como para dispersar la luz en todas las direcciones, haciendo que el haz sea visible. Es el mismo fenómeno que nos permite ver los rayos del sol atravesando un bosque neblinoso o el haz de un proyector en una sala de cine polvorienta. Las soluciones verdaderas, con partículas mucho más pequeñas, no muestran este efecto.
Movimiento Browniano
Observadas bajo un microscopio, las partículas coloidales no están quietas. Muestran un movimiento caótico, rápido y en zigzag. Este fenómeno, descubierto por el botánico Robert Brown, se debe al bombardeo incesante y desigual de las moléculas del medio dispersante sobre las partículas coloidales. Este movimiento constante es un factor crucial que contrarresta la gravedad y evita que las partículas se asienten, contribuyendo a la estabilidad del coloide.
Propiedades Eléctricas y Electroforesis
Las partículas coloidales tienen una superficie increíblemente grande en relación con su masa. Esta superficie tiende a adsorber (adherir) iones presentes en el medio, adquiriendo una carga eléctrica neta (positiva o negativa). Todas las partículas de un mismo coloide adquieren la misma carga, lo que genera una fuerza de repulsión electrostática entre ellas, impidiendo que se agrupen y precipiten. Este fenómeno es la base de la estabilización electrostática. La electroforesis es la migración de estas partículas cargadas hacia un electrodo de carga opuesta cuando se aplica un campo eléctrico externo al sistema.
Adsorción
Como se mencionó, la enorme área superficial de los coloides los convierte en excelentes adsorbentes. Esta capacidad no solo es clave para sus propiedades eléctricas, sino que también se aprovecha en aplicaciones como la purificación de agua (donde los coloides de hidróxido de aluminio adsorben impurezas) o en las mascarillas de carbón activado.
La Estabilidad Coloidal: Un Equilibrio Delicado
Mantener un coloide estable es un desafío constante contra las fuerzas de atracción (fuerzas de Van der Waals) que tienden a agrupar las partículas (proceso llamado agregación, coagulación o floculación). Para evitarlo, se recurre a dos mecanismos principales de estabilización:
- Estabilización Electrostática: Se basa en la repulsión mutua de las partículas cargadas eléctricamente, como se describió anteriormente. La adición de pequeñas cantidades de electrolitos puede fortalecer esta carga y aumentar la estabilidad.
- Estabilización Estérica: Consiste en recubrir las partículas con una capa de moléculas grandes, como polímeros o surfactantes. Esta capa actúa como una barrera física que impide que las partículas se acerquen lo suficiente como para que las fuerzas de atracción predominen.
Por el contrario, la desestabilización es el proceso de provocar la agregación y es fundamental en técnicas como el tratamiento de aguas residuales. Se puede lograr añadiendo una alta concentración de sal (que neutraliza las cargas), cambiando el pH o añadiendo polímeros floculantes que actúan como puentes entre las partículas.
Tabla Comparativa: Solución vs. Coloide vs. Suspensión
| Característica | Solución Verdadera | Sistema Coloidal | Suspensión |
|---|---|---|---|
| Tamaño de partícula | < 1 nm | 1 - 1000 nm | > 1000 nm |
| Apariencia | Transparente y homogénea | Generalmente translúcido u opaco | Opaca y heterogénea |
| Efecto Tyndall | No lo muestra | Lo muestra | Lo muestra (a veces) |
| Sedimentación | No sedimenta | No sedimenta espontáneamente | Sedimenta con el tiempo |
| Separación por filtración | No se puede separar | No con filtro común (sí con ultrafiltración) | Se puede separar con filtro común |
Preguntas Frecuentes (FAQ)
¿La sangre es un coloide?
Sí, la sangre es un sistema coloidal muy complejo. Técnicamente, es un sol donde partículas sólidas como los glóbulos rojos, glóbulos blancos y plaquetas están dispersas en un medio líquido, el plasma. El plasma a su vez es un coloide que contiene grandes moléculas de proteínas como la albúmina.
¿Cuál es la diferencia entre una emulsión y un sol?
La diferencia radica en el estado de la fase dispersa. En una emulsión, tanto la fase dispersa como la fase continua son líquidos inmiscibles entre sí (por ejemplo, aceite en agua para la mayonesa). En un sol, la fase dispersa es un sólido y la fase continua es un líquido (por ejemplo, partículas de pigmento en agua para la pintura).
¿Cómo se purifican los coloides?
Un método común es la diálisis. El sistema coloidal se coloca dentro de una bolsa hecha de una membrana semipermeable (como el celofán) y se sumerge en agua pura. Los poros de la membrana son lo suficientemente pequeños para retener las partículas coloidales, pero permiten que los iones pequeños y otras impurezas moleculares salgan de la bolsa hacia el agua, purificando así el coloide.
En conclusión, los sistemas coloidales representan una frontera fascinante de la materia, un estado intermedio que desafía las clasificaciones simples y que gobierna las propiedades de innumerables productos y procesos naturales. Desde la textura de nuestros alimentos hasta la eficacia de los medicamentos y la limpieza de nuestro medio ambiente, la ciencia de los coloides está presente, demostrando que en el mundo de lo pequeño se encuentran las claves para entender el mundo a gran escala.
Si quieres conocer otros artículos parecidos a Sistemas Coloidales: Guía Esencial puedes visitar la categoría Ecología.
