12/03/2015
La Reacción en Cadena de la Polimerasa, o PCR, es una de las herramientas más poderosas y revolucionarias en la biología molecular. Su exquisita sensibilidad nos permite tomar cantidades ínfimas de material genético, como el ADN o el ARN, y amplificar una secuencia específica millones de veces en cuestión de horas. Esta capacidad de generar una señal detectable a partir de unas pocas moléculas es lo que la hace indispensable en diagnósticos clínicos, ciencia forense, investigación genética y mucho más. Sin embargo, esta misma sensibilidad es su talón de Aquiles. Si no se maneja con un cuidado extremo, la técnica puede amplificar ADN contaminante presente en el ambiente, en los reactivos o por transferencia entre muestras, llevando a resultados falsos positivos, artefactos y conclusiones erróneas. Prevenir la contaminación no es una opción, es un requisito fundamental para obtener datos fiables y reproducibles. En este artículo, desglosaremos las estrategias y buenas prácticas de laboratorio indispensables para minimizar el riesgo de contaminación y asegurar el éxito de tus experimentos de PCR.
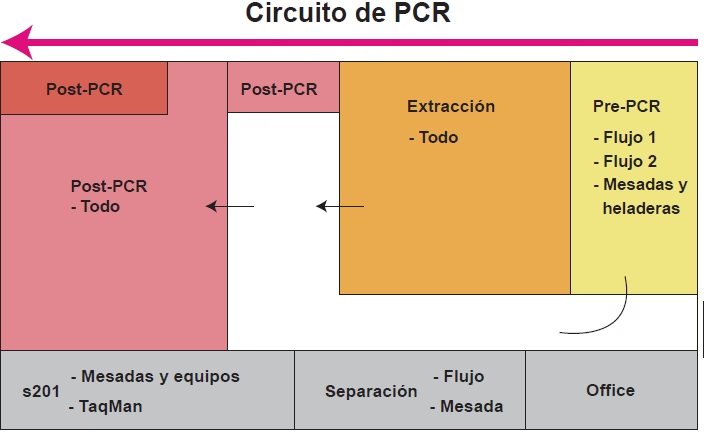
La Clave del Éxito: Una Distribución Estratégica del Laboratorio
El primer y más importante paso para prevenir la contaminación cruzada es el diseño físico del espacio de trabajo. El concepto fundamental es la separación estricta de las áreas donde se realizan las etapas previas a la amplificación (Pre-PCR) y las etapas posteriores (Post-PCR). Idealmente, estas deberían ser habitaciones completamente separadas, pero si el espacio es limitado, pueden ser áreas claramente delimitadas en extremos opuestos de una misma sala, con equipos y materiales dedicados exclusivamente a cada una.
Área de Pre-PCR: La Zona Limpia
Esta es la zona de máxima pureza. Aquí se manejan los componentes que aún no han sido amplificados y, por lo tanto, son más susceptibles a la contaminación. Esta área, a su vez, suele subdividirse en dos secciones:
- Preparación de la Mastermix: Un espacio, preferiblemente una cabina de PCR con luz UV, dedicado exclusivamente a la preparación de la mezcla de reacción (Tampón, dNTPs, polimerasa, magnesio y cebadores). Aquí no debe entrar nunca ADN molde (ni muestras ni controles positivos).
- Adición de la Muestra: Un segundo espacio donde se añade el ADN o ARN molde a los tubos que ya contienen la mastermix.
El equipamiento en la zona Pre-PCR debe ser exclusivo y nunca debe salir de ella. Esto incluye pipetas, puntas con filtro, vórtex, minicentrífugas y los reactivos de PCR.
Área de Post-PCR: La Zona de Amplicones
Esta área se considera "sucia" porque en ella se manejan los productos de PCR, es decir, miles de millones de copias de la secuencia de ADN de interés (amplicones). Estos amplicones son la fuente más peligrosa de contaminación, ya que una mínima cantidad en aerosol puede viajar y contaminar la zona Pre-PCR. En esta sala se ubican los termocicladores y todo el equipo necesario para el análisis de los resultados, como los sistemas de electroforesis en gel (cubetas, fuentes de alimentación, transiluminador), espectrofotómetros o equipos de PCR en tiempo real para el análisis de curvas de fusión.
Tabla Comparativa de Zonas PCR
| Característica | Área Pre-PCR (Zona Limpia) | Área Post-PCR (Zona de Amplicones) |
|---|---|---|
| Actividades Principales | Preparación de Mastermix, adición de ADN/ARN molde, extracción de ácidos nucleicos. | Ciclos de amplificación (termociclador), análisis de resultados (electroforesis, qPCR). |
| Equipamiento Clave | Cabina de PCR, pipetas y puntas con filtro dedicadas, vórtex, centrífuga, congeladores para reactivos y muestras. | Termocicladores, equipos de electroforesis, transiluminador UV, ordenadores para análisis. |
| Material de Laboratorio | Batas de laboratorio exclusivas (preferiblemente de otro color), guantes, tubos y placas de PCR estériles. | Batas de laboratorio exclusivas, guantes. |
| Riesgo Principal | Contaminación de reactivos y muestras con ADN exógeno o amplicones. | Dispersión de amplicones al ambiente, que pueden contaminar la zona Pre-PCR. |
El Flujo de Trabajo Unidireccional: Una Regla de Oro
Estrechamente ligado a la separación física, se encuentra el principio del flujo de trabajo unidireccional. Esto significa que el movimiento de materiales, muestras y personal debe seguir siempre una única dirección: desde la zona Pre-PCR hacia la zona Post-PCR. Nunca al revés.
Un tubo que ha estado en el termociclador jamás debe volver a la zona de preparación de la mastermix. El personal que ha trabajado en el área Post-PCR y necesita regresar a la zona Pre-PCR debe, como mínimo, quitarse la bata y los guantes utilizados en la zona "sucia" y ponerse unos limpios antes de entrar en la zona "limpia". Este protocolo evita que los amplicones, invisibles pero potentes contaminantes, viajen de polizones en la ropa o los materiales. Por ello, es crucial duplicar muchos de los materiales básicos:
- Juegos de pipetas para cada zona.
- Batas de laboratorio exclusivas para cada área.
- Cajas de guantes, gradillas, rotuladores y otros consumibles.
Técnicas Impecables para un Trabajo Preciso
Dominando el Arte del Pipeteo
Una técnica de pipeteo deficiente es una fuente común de contaminación. Al pipetear, se pueden generar aerosoles, microgotas invisibles que contienen ADN y que pueden quedar suspendidas en el aire o contaminar el interior de la pipeta. Para evitarlo:
- Utiliza siempre puntas con filtro: Actúan como una barrera que impide que los aerosoles de la muestra entren en el cuerpo de la pipeta y contaminen las siguientes muestras.
- Pipetea lentamente: Aspira y dispensa los líquidos de forma suave, apoyando la punta en la pared interior del tubo para evitar salpicaduras.
- Centrifuga los tubos: Antes de abrir cualquier tubo de reactivo o muestra, realiza una centrifugación rápida (un "spin") para bajar todo el líquido y las gotas de condensación de la tapa al fondo. Esto previene que al abrirlo se dispersen aerosoles.
- Cambia de punta: Utiliza una punta nueva para cada muestra o reactivo diferente sin excepción.
La Importancia de los Guantes Limpios
Las manos son un vehículo principal de contaminación. Es fundamental usar guantes en todo momento y cambiarlos con frecuencia. Si sospechas que has tocado una superficie potencialmente contaminada (como el exterior de un tubo de muestra, un pomo de puerta o tu propio teléfono móvil), cámbiate los guantes inmediatamente antes de tocar cualquier reactivo o tubo de PCR limpio.
Manteniendo un Ambiente Estéril: Protocolos de Limpieza
Una rutina de limpieza rigurosa es tu mejor defensa contra la contaminación ambiental. Las superficies de trabajo, pipetas, gradillas y manijas de los equipos deben descontaminarse antes y después de cada experimento. El protocolo más extendido y eficaz consiste en:
- Limpieza con Lejía (Hipoclorito de Sodio): Una solución fresca de lejía al 10-15% es muy efectiva para degradar ácidos nucleicos. Aplícala sobre las superficies y déjala actuar durante 10-15 minutos.
- Aclarado con Agua Desionizada: La lejía es corrosiva, por lo que es importante eliminar sus residuos con papel humedecido en agua estéril.
- Secado con Etanol: Finalmente, aplica etanol al 70% para eliminar los restos de agua y ayudar a que la superficie se seque rápidamente.
Adicionalmente, muchas cabinas de PCR están equipadas con lámparas de luz ultravioleta (UV) que se pueden encender durante 15-30 minutos (con la cabina vacía) para dañar el ADN que pueda quedar en las superficies.
Los Guardianes de tu Experimento: El Uso de Controles
Incluir controles adecuados en cada tanda de PCR es la única forma de verificar que el experimento ha funcionado correctamente y que no ha habido contaminación. Los dos controles indispensables son:
- Control Negativo o NTC (Non-Template Control): Es una reacción de PCR que contiene todos los componentes de la mastermix, pero en lugar de añadir la muestra de ADN, se añade agua libre de nucleasas. Este tubo pasa por todo el proceso de amplificación. Si al final del experimento se detecta un producto en el NTC, significa que ha habido una contaminación en alguno de los reactivos, consumibles o en el ambiente. Este resultado invalida toda la tanda experimental.
- Control Positivo: Es una reacción que contiene una muestra de ADN que se sabe con certeza que debe amplificar con los cebadores utilizados. Sirve para confirmar que la mastermix, los reactivos y las condiciones del termociclador son correctos y que la reacción funciona como se esperaba. Si el control positivo falla, indica un problema con el protocolo o los reactivos, no necesariamente con las muestras.
Preguntas Frecuentes (FAQ)
¿Qué hago si mi control negativo (NTC) muestra amplificación?
Un NTC positivo es una señal de alarma clara de contaminación. Debes detenerte y no confiar en los resultados de esa tanda. El siguiente paso es investigar la fuente: desecha todos los reactivos de la mastermix (alicuotas de trabajo), descontamina a fondo todo el área de Pre-PCR, las pipetas y el material, y repite el experimento con reactivos y consumibles nuevos.
¿Es realmente necesario tener dos salas separadas?
Es el estándar de oro y lo más recomendable. Sin embargo, si es imposible por limitaciones de espacio, se puede trabajar con áreas físicas bien delimitadas y separadas en la misma sala. La clave es mantener una disciplina férrea en el flujo unidireccional y en el uso de equipos y batas dedicadas para cada zona. Nunca se debe comprometer la separación de actividades Pre y Post-PCR.
¿La luz UV es suficiente para eliminar toda la contaminación por ADN?
La luz UV es una herramienta útil pero no infalible. Solo descontamina las superficies que irradia directamente y su eficacia disminuye con la distancia y puede no penetrar en pequeñas grietas o gotas de líquido. No debe reemplazar, sino complementar, la limpieza química con lejía y etanol.
En conclusión, la fiabilidad de los resultados de PCR depende directamente de la meticulosidad y la disciplina del investigador. Adoptar estas prácticas no es una carga, sino una inversión que garantiza la calidad y reproducibilidad de tu trabajo científico, ahorrando tiempo, recursos y evitando la frustración de perseguir resultados falsos.
Si quieres conocer otros artículos parecidos a PCR sin Contaminación: Guía Esencial puedes visitar la categoría Ecología.

