10/11/2005
En el vasto universo de la química orgánica, las reacciones son el corazón que bombea vida a la innovación y al desarrollo. Sin embargo, no todas las reacciones son iguales desde una perspectiva medioambiental. Durante décadas, la síntesis química se ha basado en reactivos potentes y poco selectivos, generando a menudo una cantidad considerable de residuos y subproductos no deseados. Aquí es donde la química verde emerge como una filosofía transformadora, buscando procesos más eficientes, seguros y, sobre todo, sostenibles. Uno de los desafíos más clásicos y elegantes en este campo es la oxidación selectiva: ¿cómo podemos modificar una parte de una molécula, como un grupo aldehído, sin afectar a otra parte sensible, como un grupo alcohol? La respuesta a esta pregunta no solo es un triunfo de la ciencia, sino también un paso crucial hacia una industria química que trabaja en armonía con nuestro planeta.
- Entendiendo a los Protagonistas: Aldehídos, Cetonas y Alcoholes
- El Dilema de la Oxidación: Fuerza Bruta vs. Precisión Quirúrgica
- Las Herramientas de la Química Sostenible: Reactivos Selectivos
- Tabla Comparativa: Aldehídos vs. Cetonas
- El Impacto Real: ¿Por Qué Nos Debe Importar la Selectividad?
- Preguntas Frecuentes (FAQ)
Entendiendo a los Protagonistas: Aldehídos, Cetonas y Alcoholes
Para comprender la importancia de la selectividad, primero debemos conocer a los actores principales de esta obra química. Los aldehídos, las cetonas y los alcoholes son compuestos orgánicos que contienen oxígeno y son omnipresentes tanto en la naturaleza como en la industria.
- Alcoholes: Se caracterizan por tener un grupo hidroxilo (-OH) unido a un átomo de carbono. Son la base de muchas bebidas, disolventes y combustibles. Un alcohol primario, por ejemplo, tiene el grupo -OH en un carbono que está unido a solo otro carbono.
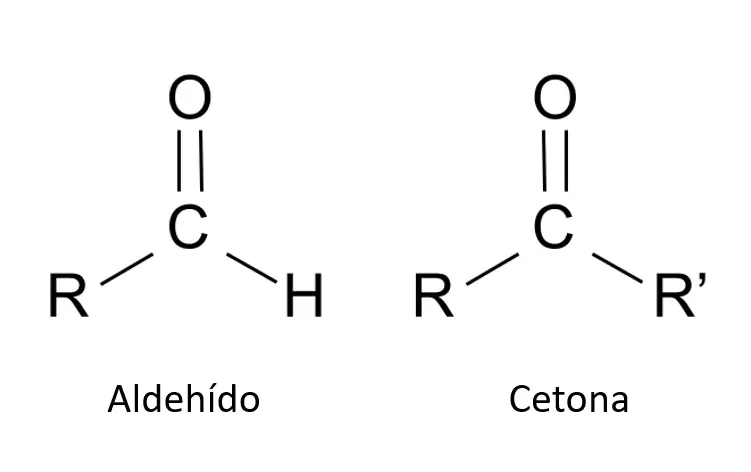
- Aldehídos y Cetonas: Ambos contienen un grupo carbonilo, que es un átomo de carbono unido por un doble enlace a un átomo de oxígeno (C=O). La diferencia fundamental radica en su ubicación. En un aldehído, el grupo carbonilo se encuentra en el extremo de una cadena de carbono, lo que significa que el carbono del carbonilo está unido al menos a un átomo de hidrógeno. En una cetona, el grupo carbonilo está en el interior de la cadena, unido a otros dos átomos de carbono.
Esta sutil diferencia estructural es la clave de todo. El hidrógeno unido al carbonilo del aldehído es el punto vulnerable, el "talón de Aquiles" que permite que sea oxidado con relativa facilidad, mientras que la cetona, al carecer de este hidrógeno, es mucho más resistente a la oxidación.
El Dilema de la Oxidación: Fuerza Bruta vs. Precisión Quirúrgica
Imaginemos una molécula compleja que contiene tanto un grupo alcohol primario como un grupo aldehído. Si aplicamos un agente oxidante fuerte y tradicional, como el permanganato de potasio (KMnO₄) o el dicromato de potasio (K₂Cr₂O₇), el resultado sería un caos químico. Estos reactivos son como un martillo pilón: oxidarían tanto el aldehído como el alcohol, convirtiéndolos a ambos en ácidos carboxílicos. Este enfoque de "fuerza bruta" no solo destruye la funcionalidad que queríamos preservar, sino que también genera subproductos, reduce el rendimiento del producto deseado y, a menudo, utiliza metales pesados tóxicos como el cromo, con un impacto ambiental negativo.
La selectividad es la alternativa elegante y sostenible. Consiste en utilizar reactivos diseñados para actuar como un bisturí de precisión, capaces de reconocer y reaccionar únicamente con el grupo funcional de interés (el aldehído) mientras dejan intacto al resto de la molécula (el alcohol). Este es el núcleo de la pregunta: ¿cómo oxidar el aldehído y no el alcohol?
Las Herramientas de la Química Sostenible: Reactivos Selectivos
Para lograr esta hazaña, los químicos han desarrollado una serie de reactivos suaves que explotan la mayor reactividad del grupo aldehído. Estos no solo son fundamentales para la síntesis, sino que también sirven como pruebas de diagnóstico para diferenciar entre aldehídos y cetonas, respondiendo así a la segunda pregunta clave.
Reactivo de Tollens: El Espejo de Plata
El reactivo de Tollens es quizás el ejemplo más famoso y visualmente impactante. Se trata de una solución amoniacal de nitrato de plata, que contiene el ion complejo diaminaplata(I), [Ag(NH₃)₂]⁺. Cuando esta solución incolora se calienta suavemente con un aldehído, ocurre una reacción redox fascinante:
- El aldehído se oxida para formar un ion carboxilato (la forma básica de un ácido carboxílico).
- El ion de plata (Ag⁺) en el complejo se reduce a plata metálica (Ag⁰).
Esta plata metálica se deposita como una capa fina y uniforme en las paredes internas del recipiente de vidrio, creando un hermoso espejo. Esta "prueba del espejo de plata" es una indicación inequívoca de la presencia de un aldehído. Lo más importante es que ni las cetonas ni los alcoholes reaccionan en estas condiciones suaves, lo que convierte al reactivo de Tollens en una herramienta perfecta para la oxidación selectiva y la identificación.
Reactivo de Fehling y Reactivo de Benedict
Mencionados en la información de partida, los reactivos de Fehling y Benedict funcionan bajo un principio similar, pero utilizando cobre en lugar de plata. Ambos contienen iones de cobre(II) (Cu²⁺) en un complejo dentro de una solución básica. El ion Cu²⁺ le da a la solución un característico color azul brillante.
Cuando se calienta con un aldehído:
- El aldehído, nuevamente, se oxida a un ion carboxilato.
- El ion de cobre(II) (Cu²⁺), de color azul, se reduce a óxido de cobre(I) (Cu₂O).
El óxido de cobre(I) es un sólido insoluble que precipita fuera de la solución con un color que va del rojo ladrillo al naranja o amarillo. El cambio de un azul transparente a un precipitado rojizo es la señal de una prueba positiva. Al igual que con Tollens, ni las cetonas ni los alcoholes provocan esta reacción. Estos ensayos son históricamente importantes y todavía se utilizan, por ejemplo, para detectar la presencia de azúcares reductores (como la glucosa, que contiene un grupo aldehído) en muestras biológicas.
Tabla Comparativa: Aldehídos vs. Cetonas
Para visualizar mejor estas diferencias cruciales, la siguiente tabla resume sus características principales:
| Característica | Aldehído | Cetona |
|---|---|---|
| Estructura del Carbonilo | El carbono del C=O está unido a un grupo R y a un Hidrógeno (R-CHO). | El carbono del C=O está unido a dos grupos R (R-CO-R'). |
| Ubicación del Carbonilo | En el extremo de la cadena de carbono. | En el interior de la cadena de carbono. |
| Oxidación con Reactivos Suaves | Sí reacciona (positivo en Tollens, Fehling, Benedict). | No reacciona (negativo en estas pruebas). |
| Producto de la Oxidación | Ácido carboxílico (o su base conjugada, el carboxilato). | No se oxida en condiciones suaves. Requiere condiciones muy drásticas que rompen la cadena. |
| Ejemplo Común | Formaldehído (Metanal), Acetaldehído (Etanal). | Acetona (Propanona). |
El Impacto Real: ¿Por Qué Nos Debe Importar la Selectividad?
Esta discusión puede parecer puramente académica, pero sus implicaciones para la sostenibilidad son enormes. La industria farmacéutica, de fragancias, de polímeros y de agroquímicos depende de la capacidad para construir moléculas complejas con precisión. Utilizar métodos selectivos significa:
- Menos Residuos: Al dirigir la reacción a un solo punto, se evita la formación de una mezcla de subproductos que son difíciles de separar y que a menudo terminan como residuos contaminantes.
- Mayor Eficiencia: Se obtiene un mayor rendimiento del producto deseado a partir de la misma cantidad de materia prima, un principio clave de la economía de átomos.
- Condiciones más Seguras y Suaves: Los reactivos selectivos suelen operar a temperaturas y presiones más bajas, lo que ahorra energía. Además, se evita el uso de compuestos altamente tóxicos y peligrosos, como los basados en cromo hexavalente.
- Productos más Puros: La pureza es crítica, especialmente en farmacia. Un proceso selectivo conduce a un producto final más limpio, reduciendo la necesidad de costosos y energéticamente intensivos procesos de purificación.
Preguntas Frecuentes (FAQ)
¿Por qué una cetona es tan resistente a la oxidación en comparación con un aldehído?
La clave está en la estructura. Para oxidar el carbono del carbonilo, generalmente se necesita romper un enlace. En un aldehído, hay un enlace C-H que es relativamente fácil de romper. En una cetona, el carbono del carbonilo está flanqueado por dos enlaces C-C, que son mucho más fuertes y estables. Romper uno de estos enlaces requiere una gran cantidad de energía (condiciones drásticas), lo que a menudo fragmenta la molécula en lugar de oxidarla limpiamente.
¿Qué sucede si intento oxidar un alcohol secundario?
Un alcohol secundario puede ser oxidado, pero su producto de oxidación es una cetona. Por lo tanto, si tuviéramos una molécula con un grupo aldehído y un grupo alcohol secundario y usáramos un oxidante fuerte, obtendríamos un ácido carboxílico y una cetona. Si usáramos un reactivo suave como el de Tollens, solo el aldehído reaccionaría, dejando el alcohol secundario intacto. Esto demuestra aún más el poder de la selectividad.
¿Existen otros reactivos selectivos además de los mencionados?
¡Absolutamente! La química moderna ha desarrollado un arsenal de reactivos aún más sofisticados y ecológicos. Por ejemplo, el periodinano de Dess-Martin (DMP) o la oxidación de Swern son métodos que pueden oxidar alcoholes primarios a aldehídos sin llevar la oxidación hasta el ácido carboxílico, demostrando otro nivel de control selectivo. La investigación en catálisis, utilizando metales para guiar las reacciones de manera eficiente y con pocos residuos, es una de las fronteras más activas de la química verde.
En conclusión, la capacidad de oxidar un aldehído sin afectar a un alcohol no es solo un truco de laboratorio. Es un ejemplo perfecto de cómo la inteligencia y el diseño a nivel molecular pueden tener un impacto macroscópico en nuestro medio ambiente. Al elegir la precisión sobre la fuerza bruta, la química verde nos muestra el camino hacia una industria más limpia, segura y eficiente, demostrando que el progreso científico y la protección del planeta pueden y deben ir de la mano.
Si quieres conocer otros artículos parecidos a Oxidación Selectiva: Un Pilar de la Química Verde puedes visitar la categoría Sostenibilidad.
