29/12/2020
La electroquímica, la ciencia que estudia la interrelación entre la energía eléctrica y las reacciones químicas, se ha posicionado como una de las herramientas más prometedoras para abordar algunos de los desafíos ambientales más apremiantes de nuestro tiempo. Desde la descontaminación de aguas hasta el desarrollo de sistemas de almacenamiento de energía más eficientes y sostenibles, sus aplicaciones son vastas y crecientes. Sin embargo, en el corazón de muchos de estos procesos se encuentra un elemento con una reputación compleja y, a menudo, contradictoria: el cloro. Dependiendo del contexto, el ion cloruro (Cl⁻) puede ser un componente esencial para el éxito de una tecnología o un precursor indeseado de subproductos tóxicos. Este artículo explora el doble filo del cloro en el mundo electroquímico, desentrañando su papel como héroe y villano en la búsqueda de un futuro más verde.
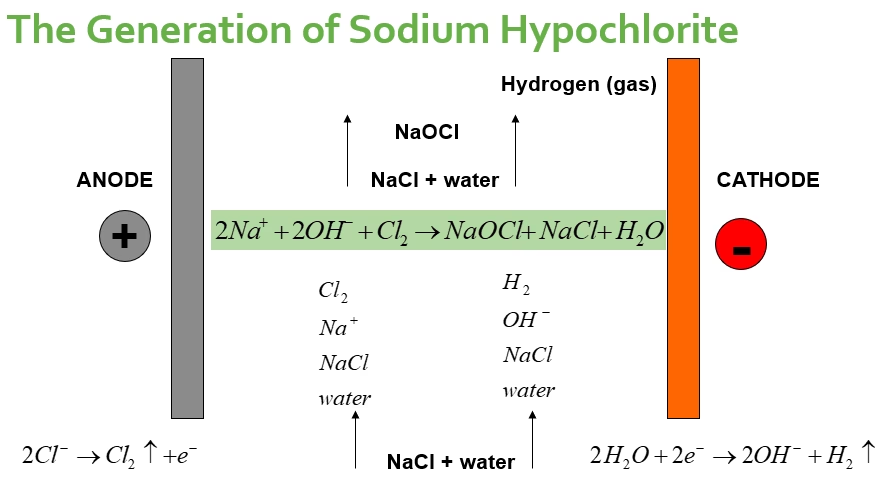
Descontaminación Electroquímica: Rompiendo las Cadenas del Cloro
Uno de los grandes problemas de contaminación a nivel mundial es la presencia de compuestos orgánicos clorados en el medio ambiente. Estas sustancias, que incluyen desde pesticidas hasta solventes industriales y subproductos de diversos procesos, son a menudo tóxicas, persistentes y bioacumulables. Su estructura química, caracterizada por uno o más enlaces entre átomos de carbono y cloro (C-Cl), los hace muy estables y difíciles de degradar por medios naturales.
Aquí es donde la electroquímica interviene como una fuerza de cambio. La deshalogenación electro-reductiva es una estrategia que ha ganado una atención considerable por su capacidad para romper selectivamente estos robustos enlaces C-Cl. El objetivo es transformar los contaminantes peligrosos en compuestos menos tóxicos o completamente inocuos. Este proceso puede llevarse a cabo a través de varios mecanismos fascinantes:
- Reducción Electroquímica Directa: Es el mecanismo más común. En este caso, se aplica un potencial eléctrico a un cátodo (el electrodo negativo), que transfiere electrones directamente a la molécula del contaminante. Esta inyección de energía electrónica desestabiliza el enlace C-Cl, provocando su ruptura. La transferencia de electrones puede ocurrir de forma concertada (el electrón llega y el enlace se rompe en un solo paso) o por etapas (la molécula acepta primero el electrón y luego se rompe el enlace).
- Hidrodescloración Electrocatalítica: Este enfoque es más indirecto y sofisticado. Se utilizan materiales catalíticos en el cátodo (como metales de transición tipo paladio) que, bajo el potencial adecuado, son capaces de descomponer el agua presente para generar hidrógeno atómico (H•) en su superficie. Estos átomos de hidrógeno son extremadamente reactivos y atacan el enlace C-Cl, reemplazando el átomo de cloro por uno de hidrógeno y liberando el cloruro como un ion inofensivo.
- Reducción Mediada Electroquímicamente: En esta tercera vía, se utiliza una molécula "mediadora" que actúa como un transportista de electrones. El cátodo primero reduce al mediador, y este, a su vez, viaja por la solución hasta encontrar una molécula del contaminante, a la cual le transfiere el electrón. Es un sistema de reparto de electrones que puede superar ciertas limitaciones de la transferencia directa.
En todos estos casos, el cloro, como parte del compuesto orgánico, es el enemigo a batir. El éxito del proceso se mide por la eficiencia con la que se eliminan los átomos de cloro de las estructuras moleculares, demostrando el poder de la electroquímica para remediar la contaminación existente.
Oxidación Electroquímica: Cuando la Solución Crea un Nuevo Problema
Si en la deshalogenación el objetivo es romper enlaces con cloro, en la oxidación electroquímica para el tratamiento de aguas residuales, la presencia de cloro puede ser un arma de doble filo. Los procesos de oxidación avanzada (POA) electroquímicos son increíblemente potentes para destruir una amplia gama de contaminantes orgánicos, desde fármacos hasta colorantes, que son resistentes a los tratamientos convencionales. Utilizan ánodos (electrodos positivos) de alto rendimiento, como los de diamante dopado con boro (BDD), que pueden generar radicales hidroxilo (•OH), uno de los oxidantes más fuertes que se conocen.
El problema surge cuando el agua a tratar contiene iones cloruro (Cl⁻), algo extremadamente común en aguas residuales industriales, aguas salobres o incluso en el agua potable. En la superficie del ánodo, estos iones cloruro pueden oxidarse para formar cloro activo (como el hipoclorito, ClO⁻), el mismo agente de la lejía. Si bien este cloro activo puede contribuir a la desinfección y a la degradación de algunos contaminantes, también tiene un lado oscuro: puede reaccionar con la materia orgánica natural presente en el agua o con los propios contaminantes para formar subproductos de desinfección (DBPs, por sus siglas en inglés) clorados. Compuestos como el cloroformo, los ácidos haloacéticos y otras moléculas organocloradas pueden generarse involuntariamente. Irónicamente, en un esfuerzo por eliminar contaminantes, se pueden crear otros nuevos, algunos de los cuales están regulados por su potencial carcinogénico.

La investigación actual se centra en controlar este fenómeno, ya sea ajustando los parámetros del proceso (como el voltaje aplicado) o desarrollando nuevos materiales para los ánodos que favorezcan la generación de radicales hidroxilo sobre la oxidación del cloruro, buscando maximizar la destrucción de contaminantes minimizando la formación de subproductos no deseados.
Tabla Comparativa: Las Dos Caras del Cloro Electroquímico
| Característica | Deshalogenación Reductiva | Oxidación Electroquímica en Presencia de Cloruro |
|---|---|---|
| Objetivo Principal | Eliminar contaminantes orgánicos clorados. | Eliminar contaminantes orgánicos en general. |
| Rol del Cloro | Parte del contaminante a ser eliminado (el "villano"). | Ion presente en el agua que puede convertirse en un precursor de nuevos contaminantes. |
| Proceso Clave | Reducción en el cátodo (ganancia de electrones). | Oxidación en el ánodo (pérdida de electrones). |
| Resultado Deseado | Ruptura del enlace Carbono-Cloro. | Mineralización completa del contaminante a CO₂, agua y sales. |
| Riesgo Principal | Reacciones incompletas o formación de subproductos menos clorados pero aún tóxicos. | Formación de subproductos de desinfección clorados y tóxicos. |
Una Perspectiva Diferente: El Cloruro como Héroe en las Baterías de Magnesio
Para completar el cuadro de la dualidad del cloro, es útil mirar más allá de la remediación ambiental, hacia el campo del almacenamiento de energía. Las baterías recargables de magnesio (Mg) son una alternativa interesante a las de ion-litio debido a la alta abundancia del magnesio y su menor tendencia a formar dendritas peligrosas. Sin embargo, uno de los mayores desafíos es la compatibilidad del electrolito con el electrodo de magnesio metálico.
El magnesio tiende a reaccionar con muchos electrolitos, formando una "capa de pasivación" en su superficie. Esta capa, compuesta por productos de la descomposición del electrolito, bloquea el movimiento de los iones de magnesio, ahogando la batería y reduciendo drásticamente su eficiencia y vida útil. Aquí, sorprendentemente, el cloruro añadido al electrolito (en forma de MgCl₂) actúa como un héroe. Las investigaciones han demostrado que el cloruro es un acelerador de la disolución de esta capa de pasivación. Ayuda a mantener la superficie del magnesio "limpia" y activa, permitiendo que el proceso de deposición y disolución de magnesio durante los ciclos de carga y descarga ocurra de manera mucho más eficiente. En electrolitos inestables, la ausencia de cloruro conduce a una eficiencia coulómbica muy baja y a la formación de una capa de pasivación gruesa y creciente que inutiliza la batería. Por lo tanto, en este contexto, el cloruro es un aditivo crucial que permite el funcionamiento de la tecnología.
Preguntas Frecuentes (FAQ)
- ¿Son todos los compuestos clorados malos para el medio ambiente?
- No. El ion cloruro (Cl⁻) es un componente natural y esencial de los océanos y de muchos procesos biológicos. El problema reside en los compuestos orgánicos clorados de origen sintético, que no existen en la naturaleza y que los ecosistemas no pueden degradar fácilmente.
- ¿Qué es exactamente una "capa de pasivación"?
- Es una capa muy delgada de material que se forma en la superficie de un metal y lo protege de una mayor reacción o corrosión. En el caso de los metales para construcción, es un efecto deseable. En una batería, donde se necesita que la superficie del electrodo esté activa, esta capa es perjudicial.
- ¿La formación de subproductos clorados significa que la oxidación electroquímica no es una buena tecnología?
- No necesariamente. Significa que es una tecnología poderosa que debe ser entendida y controlada. La investigación se enfoca en optimizar las condiciones de operación y los materiales para minimizar o eliminar la formación de estos subproductos, aprovechando su gran poder destructivo de contaminantes de manera segura.
- ¿Por qué la electroquímica es tan prometedora para el medio ambiente?
- Por su versatilidad. Puede ser utilizada para destruir contaminantes (oxidación) o para detoxificarlos (reducción). Además, es un proceso que funciona con electricidad, la cual puede provenir de fuentes renovables como la solar o la eólica, convirtiéndola en una tecnología potencialmente muy sostenible y limpia.
En conclusión, el cloro en los sistemas electroquímicos no puede ser etiquetado simplemente como bueno o malo. Su comportamiento es un claro ejemplo de la complejidad de la química. Es un componente de contaminantes que buscamos destruir, un precursor de nuevos tóxicos que debemos evitar y un aditivo esencial que hace posible nuevas tecnologías de energía. Comprender esta dualidad es fundamental para los científicos e ingenieros que trabajan en el desarrollo de soluciones electroquímicas, asegurando que aprovechemos su poder para el bien del medio ambiente mientras mitigamos sus riesgos potenciales.
Si quieres conocer otros artículos parecidos a El Rol Dual del Cloro en Procesos Electroquímicos puedes visitar la categoría Ecología.
