11/01/2024
En el vasto universo de la biotecnología y la producción farmacéutica, existen desafíos invisibles que son cruciales para la seguridad del paciente. Uno de los más significativos es la contaminación por endotoxinas bacterianas. Estas moléculas, aunque fascinantes desde el punto de vista biológico, representan un grave riesgo cuando están presentes en productos inyectables, como medicamentos basados en proteínas. Su eliminación no es una tarea sencilla; las endotoxinas son increíblemente resistentes y los métodos para deshacerse de ellas deben ser lo suficientemente delicados para no dañar las valiosas y frágiles proteínas que se buscan purificar. Este artículo profundiza en la naturaleza de las endotoxinas, los desafíos que presentan y las estrategias más efectivas para su remoción.

¿Qué Son las Endotoxinas y Por Qué Son un Problema?
Las endotoxinas son componentes estructurales de la membrana externa de las bacterias Gram-negativas, como la famosa Escherichia coli, ampliamente utilizada en la producción de proteínas recombinantes. Químicamente, son conocidas como lipopolisacáridos (LPS), una compleja molécula que la bacteria libera principalmente cuando muere y su pared celular se descompone.
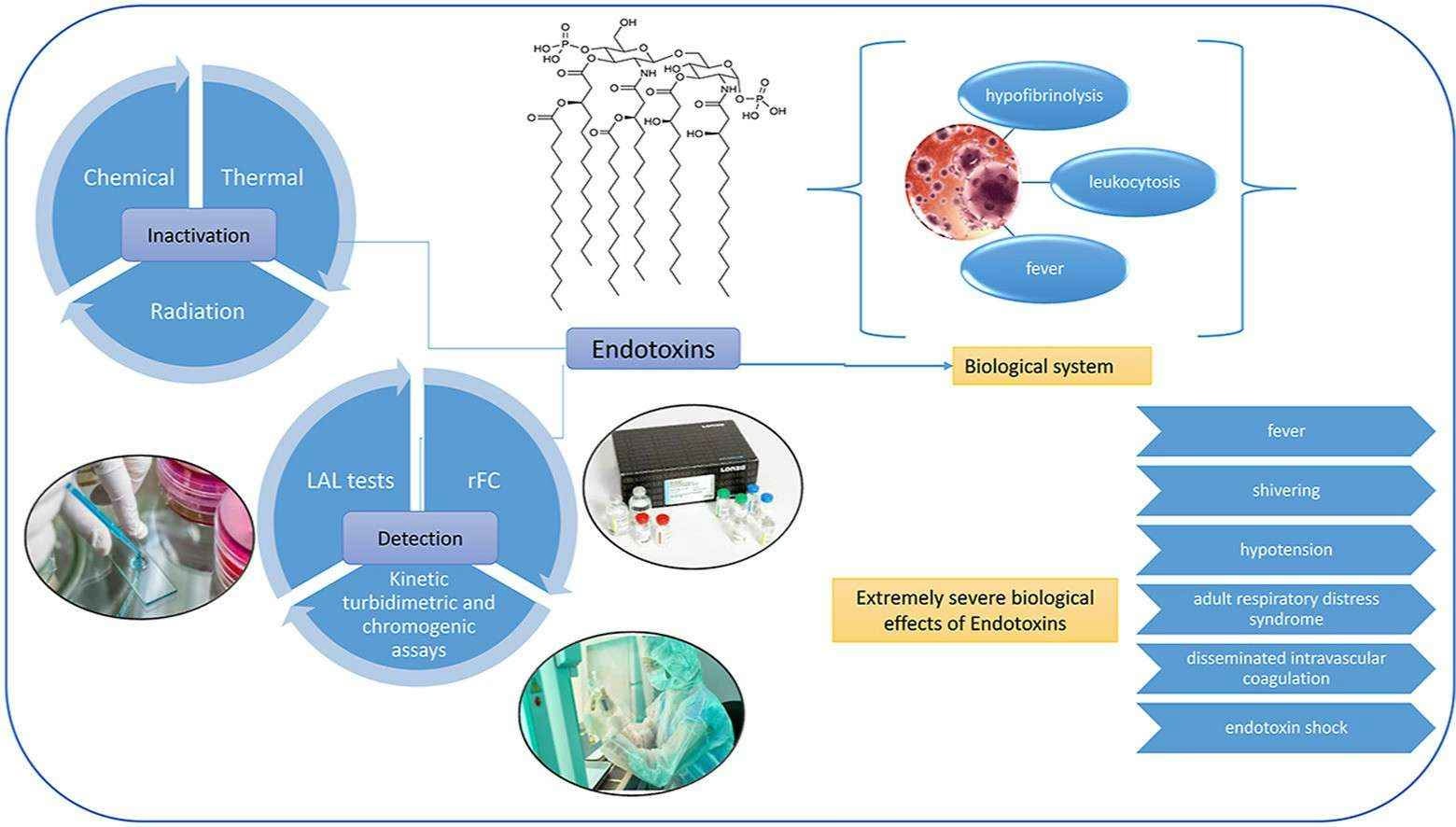
El principal problema con estas moléculas es su potente actividad biológica en humanos y muchos animales. Cuando ingresan al torrente sanguíneo, incluso en concentraciones mínimas, pueden desencadenar una fuerte respuesta inmunitaria. El cuerpo las reconoce como una señal de invasión bacteriana, lo que provoca la liberación de citoquinas y otros mediadores inflamatorios. Esto puede resultar en síntomas que van desde fiebre y malestar hasta condiciones graves como el shock séptico y la muerte. Por esta razón, se les considera potentes pirógenos, es decir, sustancias que inducen fiebre.
Las agencias reguladoras de todo el mundo, a través de las farmacopeas, han establecido límites muy estrictos para la contaminación por endotoxinas en productos parenterales (inyectables). El umbral aceptado es de 5 Unidades de Endotoxina (EU) por kilogramo de peso corporal por hora. Para poner esto en perspectiva, 1 EU equivale aproximadamente a 100 picogramos (una billonésima parte de un gramo) de endotoxina. Alcanzar este nivel de pureza es un desafío mayúsculo en cualquier proceso de fabricación.
Fuentes de Contaminación y el Desafío de la Estabilidad
La contaminación por endotoxinas puede ocurrir en múltiples etapas del proceso de fabricación biofarmacéutica. Las fuentes más comunes incluyen:
- El Sistema de Expresión: Si se utilizan bacterias Gram-negativas para producir una proteína recombinante, la lisis celular para liberar el producto también liberará una gran cantidad de endotoxinas.
- Materias Primas: El agua, los medios de cultivo, los excipientes y otros aditivos pueden estar contaminados con bacterias o endotoxinas.
- Equipamiento y Materiales: Reactores, tuberías, columnas de cromatografía y sistemas de cierre de contenedores pueden albergar contaminación si no se limpian y esterilizan adecuadamente.
Lo que complica enormemente su eliminación es su extraordinaria estabilidad. A diferencia de las proteínas, que son sensibles al calor, al pH y a los agentes químicos, las endotoxinas son extremadamente robustas. Los procedimientos de esterilización estándar, como el autoclave (vapor a 121°C), no son suficientes para destruirlas. Para inactivar endotoxinas en equipos de laboratorio (un proceso conocido como depirogenación), se requieren temperaturas de calor seco de 180-250°C durante varias horas o el uso de ácidos o bases fuertes. Evidentemente, estos métodos tan agresivos destruirían por completo cualquier producto proteico sensible.
Estrategias y Métodos para la Eliminación de Endotoxinas
Dado que la destrucción de las endotoxinas en la solución final no es una opción, el enfoque se centra en su eliminación física durante el proceso de purificación. Afortunadamente, existen varias técnicas que explotan las propiedades fisicoquímicas de los lipopolisacáridos para separarlos de las proteínas.
1. Cromatografía de Intercambio Aniónico (AEX)
Este es uno de los métodos más utilizados y efectivos. Se basa en la carga eléctrica de las moléculas. La porción de fosfato del LPS le confiere una fuerte carga negativa neta en un amplio rango de pH. En la cromatografía de intercambio aniónico, se utiliza una resina (fase estacionaria) con carga positiva. Cuando la solución de proteína contaminada pasa a través de la columna, las endotoxinas se unen fuertemente a la resina, mientras que la proteína de interés (si tiene una carga neta neutra o positiva bajo las condiciones de pH seleccionadas) no se une y puede ser recolectada. Si la proteína también es negativa, se pueden ajustar las condiciones (pH, fuerza iónica) para que la proteína eluya antes que las endotoxinas, que tienen una afinidad mucho mayor por la resina.
2. Cromatografía de Afinidad
Esta técnica utiliza ligandos específicos que se unen con alta afinidad a las endotoxinas. La resina de la columna se modifica químicamente para anclar estos ligandos. Cuando la solución pasa a través, las endotoxinas son capturadas selectivamente. Algunos ligandos comunes son:
- Polimixina B: Un antibiótico que se une específicamente a la porción Lípido A de la endotoxina, que es la responsable de su actividad biológica.
- Histidina Inmovilizada: El aminoácido histidina, cuando está inmovilizado en un soporte, también ha demostrado tener una alta afinidad para unirse a los lipopolisacáridos.
Estos métodos son muy específicos pero pueden ser más costosos y la posible lixiviación (desprendimiento) del ligando en el producto final debe ser rigurosamente controlada.
3. Ultrafiltración y Diafiltración
Este método se basa en la separación por tamaño. Las endotoxinas en solución acuosa tienden a formar grandes agregados o micelas, con un peso molecular que puede superar los 1,000 kDa. Las proteínas suelen ser mucho más pequeñas. La ultrafiltración utiliza membranas con un tamaño de poro definido (conocido como Molecular Weight Cut-Off o MWCO) que retiene las grandes micelas de endotoxinas mientras permite que las proteínas más pequeñas pasen a través. Sin embargo, la efectividad de este método puede verse comprometida si ciertos detergentes o condiciones de la solución rompen estas micelas en monómeros más pequeños, que podrían pasar a través de la membrana junto con la proteína.
4. Separación en Sistemas Acuosos de Dos Fases
Esta técnica, aunque menos común, es ingeniosa. Implica la creación de dos fases líquidas inmiscibles (como agua y aceite, pero usando polímeros o surfactantes). Las endotoxinas, debido a su naturaleza anfifílica (una parte hidrofóbica y otra hidrofílica), tienden a migrar preferentemente a una de las fases, mientras que la proteína se queda en la otra. Luego, las dos fases se separan físicamente, logrando la purificación.
Tabla Comparativa de Métodos de Eliminación
| Método | Principio de Funcionamiento | Ventajas | Desventajas |
|---|---|---|---|
| Intercambio Aniónico (AEX) | Separación por carga eléctrica. Endotoxinas (negativas) se unen a resina positiva. | Alta capacidad, muy efectivo, escalable industrialmente. | La proteína puede unirse si también es negativa. Requiere optimización de pH y sal. |
| Cromatografía de Afinidad | Unión específica de endotoxinas a un ligando inmovilizado (ej. Polimixina B). | Muy alta especificidad y eficiencia de remoción. | Mayor costo, posible lixiviación del ligando, vida útil limitada de la resina. |
| Ultrafiltración | Separación por tamaño. Retiene grandes agregados de endotoxinas. | Simple, puede ser económico, no requiere aditivos. | Ineficaz si las endotoxinas no están agregadas. Riesgo de obstrucción de la membrana. |
| Sistemas de Dos Fases | Partición diferencial entre dos fases líquidas inmiscibles. | Proceso continuo, puede manejar altas cargas de contaminantes. | Complejo de implementar, requiere la eliminación posterior de los agentes de fase. |
Preguntas Frecuentes (FAQ)
¿La eliminación de endotoxinas funciona para proteínas con etiqueta de histidina (6xHis-tag)?
Sí, pero con una consideración importante. Si se utiliza cromatografía de afinidad con histidina inmovilizada para eliminar endotoxinas, esta resina también podría unirse a la proteína con etiqueta de histidina, lo que haría ineficaz la separación. En estos casos, es preferible utilizar otros métodos como la cromatografía de intercambio aniónico o la ultrafiltración, que no dependen de la interacción con la histidina. La elección del método debe ser compatible con las propiedades de la proteína de interés.
¿Es posible eliminar el 100% de las endotoxinas?
En la práctica, el objetivo no es alcanzar una eliminación del 100%, lo cual es técnicamente casi imposible de lograr y verificar. El objetivo es reducir el nivel de endotoxinas por debajo del umbral de seguridad establecido por las agencias reguladoras (como las 5 EU/kg/h). Un proceso de purificación validado garantiza que el producto final sea consistentemente seguro para su uso en humanos.
¿Por qué no simplemente se evita usar bacterias Gram-negativas?
Aunque existen otros sistemas de expresión (levaduras, células de mamífero, bacterias Gram-positivas) que no producen endotoxinas, E. coli sigue siendo extremadamente popular por su rápido crecimiento, su bajo costo y su alta productividad. En muchos casos, los beneficios de usar E. coli superan la complejidad añadida de tener que eliminar las endotoxinas, especialmente con las robustas tecnologías de purificación disponibles hoy en día.
Conclusión
La eliminación de endotoxinas de soluciones proteicas es un paso no negociable en la producción de biofármacos seguros y eficaces. Representa un perfecto ejemplo de la intersección entre la biología, la química y la ingeniería. Aunque las endotoxinas son adversarios formidables por su estabilidad y potencia biológica, una combinación estratégica de métodos de purificación, un control riguroso de las materias primas y un diseño de proceso inteligente permiten a la industria biofarmacéutica superar este desafío. La clave del éxito reside en entender las propiedades tanto de la proteína deseada como del contaminante a eliminar, para así diseñar un proceso de purificación que sea, a la vez, implacable con las endotoxinas y gentil con el producto final.
Si quieres conocer otros artículos parecidos a El Reto de Eliminar Endotoxinas en Proteínas puedes visitar la categoría Ecología.