29/06/2003
En el corazón de la tecnología que impulsa nuestro mundo, desde la batería de nuestro teléfono móvil hasta los avanzados sistemas de purificación de agua, se encuentra un dispositivo fascinante: la celda electroquímica. Desarrolladas a finales del siglo XVIII por los visionarios científicos Luigi Galvani y Alessandro Volta, estas celdas, también conocidas como galvánicas o voltaicas en su honor, representan la unión perfecta entre la química y la electricidad. Son el escenario donde las reacciones químicas se convierten en energía útil o, a la inversa, donde la energía eléctrica se utiliza para provocar transformaciones químicas con fines ecológicos y productivos. Este proceso de transferencia de electrones, conocido como reacción de redox (oxidación-reducción), es la clave de su poder y versatilidad.
- El Mecanismo Interno: ¿Cómo Funciona una Celda Electroquímica?
- Los Dos Lados de la Moneda: Celdas Galvánicas vs. Electrolíticas
- El Potencial de la Celda: La Fuerza que Impulsa los Electrones
- Un Ejemplo Clásico: La Pila de Daniell
- Aplicaciones Ambientales: Más Allá de las Baterías
- Preguntas Frecuentes (FAQ)
El Mecanismo Interno: ¿Cómo Funciona una Celda Electroquímica?
Para entender una celda electroquímica, debemos imaginarla como un pequeño ecosistema donde cada componente tiene un rol vital. El sistema se basa en la separación de una reacción redox en dos semi-reacciones, cada una ocurriendo en un compartimento diferente. Estos compartimentos están conectados para permitir el flujo de energía y mantener el equilibrio.
Sus componentes característicos son:
- Ánodo: Es el electrodo donde tiene lugar la oxidación. Aquí, una sustancia (el agente reductor) pierde electrones. Por convención, en las celdas que generan energía, se considera el polo negativo, ya que es la fuente de donde emanan los electrones hacia el circuito externo.
- Cátodo: Es el electrodo donde ocurre la reducción. En este polo, una sustancia (el agente oxidante) gana los electrones que viajaron desde el ánodo. Se considera el polo positivo, pues atrae a los electrones.
- Puente Salino: A menudo un tubo de vidrio en forma de 'U' relleno con un electrolito inerte (como cloruro de potasio, KCl) en un gel. Su función es crucial: conecta las dos disoluciones de los electrodos, permitiendo el paso de iones para mantener la neutralidad eléctrica de cada semicelda. Sin él, la acumulación de carga detendría la reacción casi instantáneamente.
- Circuito Externo y Voltímetro: Un cable conductor que conecta el ánodo y el cátodo, permitiendo que los electrones fluyan de uno a otro. El voltímetro se intercala en este circuito para medir la diferencia de potencial (voltaje) generada por la celda.
Los Dos Lados de la Moneda: Celdas Galvánicas vs. Electrolíticas
Aunque todas las celdas se basan en el mismo principio redox, su propósito final las divide en dos grandes categorías. Comprender esta diferencia es fundamental para apreciar su amplio rango de aplicaciones.
Celda Galvánica (o Voltaica)
La celda galvánica es la que todos conocemos en forma de pilas y baterías. Su característica principal es que la reacción redox ocurre de forma espontánea. Es decir, la reacción química tiene una tendencia natural a suceder, y al hacerlo, libera energía en forma de electricidad. Convierte la energía química almacenada en sus componentes directamente en energía eléctrica que podemos usar para alimentar dispositivos.
Celda Electrolítica
Por el contrario, la celda electrolítica alberga una reacción redox no espontánea. Esta reacción no ocurriría por sí sola. Para forzarla a suceder, es necesario aplicar una fuente de energía eléctrica externa (como una fuente de alimentación). En este caso, la celda consume energía eléctrica para producir una transformación química deseada. Sus aplicaciones son industriales y medioambientales, como la producción de cloro, la purificación de metales o la descomposición del agua en hidrógeno y oxígeno (electrólisis).
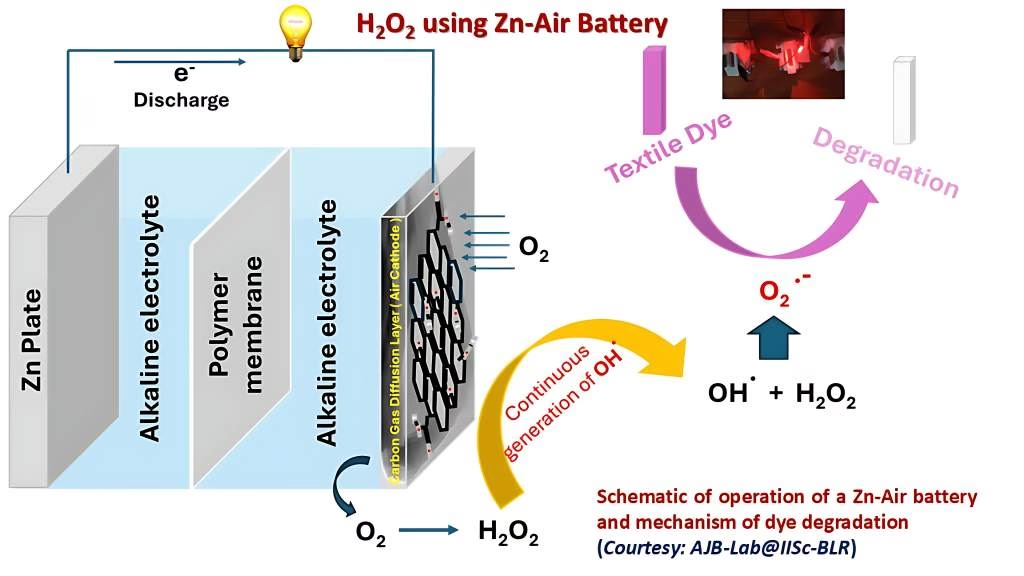
Tabla Comparativa
| Característica | Celda Galvánica (Voltaica) | Celda Electrolítica |
|---|---|---|
| Proceso | Espontáneo (produce energía) | No espontáneo (consume energía) |
| Flujo de Energía | Energía Química → Energía Eléctrica | Energía Eléctrica → Energía Química |
| Ánodo (Oxidación) | Polo Negativo (-) | Polo Positivo (+) |
| Cátodo (Reducción) | Polo Positivo (+) | Polo Negativo (-) |
| Ejemplo de Uso | Pilas, baterías de coche, celdas de combustible | Electrólisis del agua, recubrimiento de metales (galvanoplastia) |
El Potencial de la Celda: La Fuerza que Impulsa los Electrones
La razón por la cual los electrones fluyen del ánodo al cátodo es una diferencia de energía potencial eléctrica entre ambos, similar a cómo el agua fluye de un punto más alto a uno más bajo. Esta diferencia de potencial se conoce como fuerza electromotriz (fem) o potencial de la celda, y se mide en voltios (V). Se calcula con la fórmula:
Ecelda = Ecátodo - Eánodo
Dado que no podemos medir el potencial absoluto de un solo electrodo, se estableció un punto de referencia universal: el Electrodo Estándar de Hidrógeno (EEH), al cual se le asigna por convención un potencial de 0,00 V. Todos los demás potenciales de electrodo se miden en relación con este estándar, creando una tabla de potenciales estándar de reducción. Un valor positivo en Ecelda indica una reacción espontánea (celda galvánica), mientras que un valor negativo indica una no espontánea (celda electrolítica).
Un Ejemplo Clásico: La Pila de Daniell
Para ilustrar el funcionamiento de una celda galvánica, el ejemplo de la Pila de Daniell es perfecto. Consiste en:
- Ánodo: Una barra de zinc (Zn) sumergida en una disolución de sulfato de zinc (ZnSO₄).
- Cátodo: Una barra de cobre (Cu) sumergida en una disolución de sulfato de cobre (CuSO₄).
Las reacciones que ocurren son:
- En el ánodo (oxidación): Zn(s) → Zn²⁺(aq) + 2e⁻
- En el cátodo (reducción): Cu²⁺(aq) + 2e⁻ → Cu(s)
El zinc metálico se disuelve, liberando electrones que viajan por el cable externo hasta el electrodo de cobre. Allí, los iones de cobre de la disolución los aceptan y se depositan como cobre metálico. El potencial estándar de esta pila es de +1,103 V, lo que confirma que la reacción es espontánea y capaz de generar electricidad.
Aplicaciones Ambientales: Más Allá de las Baterías
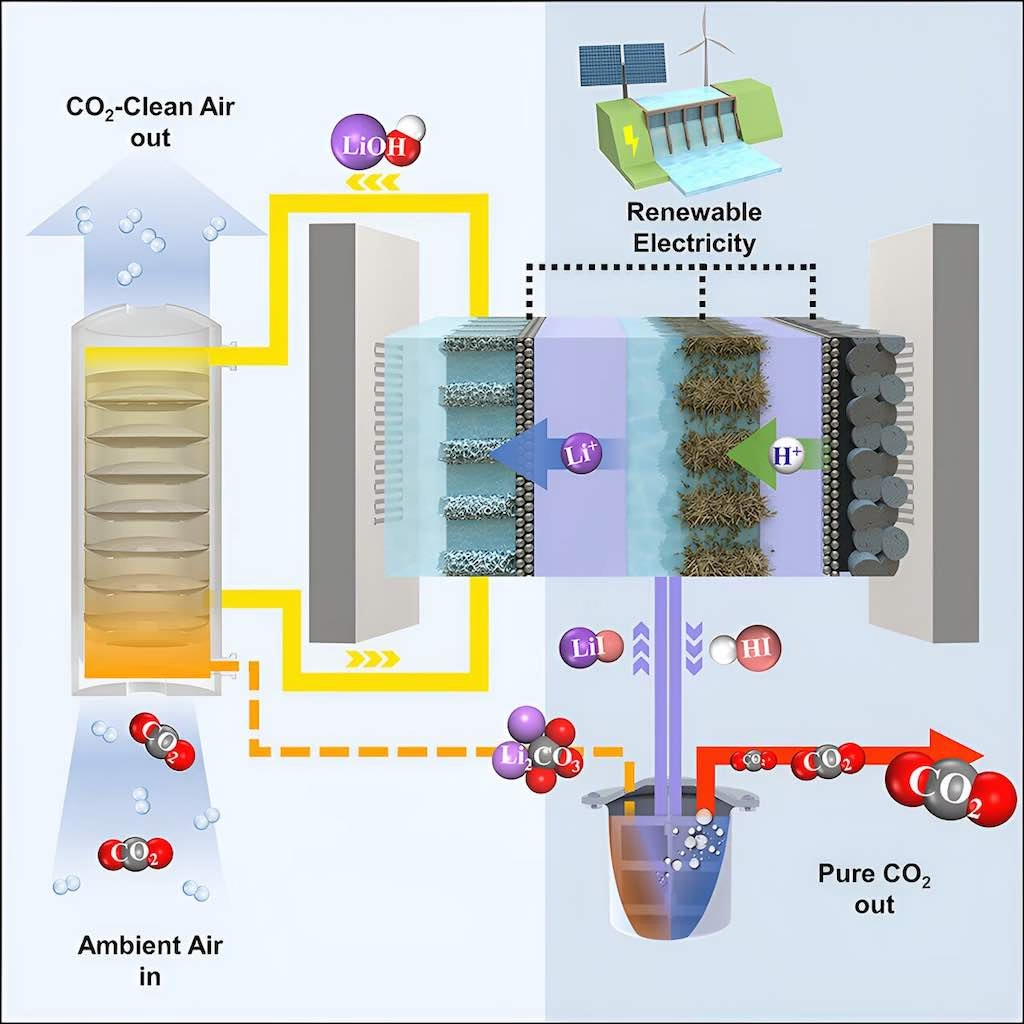
Si bien su uso en baterías es el más conocido, el verdadero potencial revolucionario de las celdas electroquímicas reside en sus aplicaciones para el cuidado del medio ambiente, principalmente a través de las celdas electrolíticas.
- Tratamiento de Aguas Residuales: Procesos como la electrocoagulación y la electrooxidación utilizan la electricidad para eliminar contaminantes persistentes. Pueden degradar pesticidas, colorantes industriales y otros compuestos orgánicos tóxicos, convirtiéndolos en sustancias más simples e inocuas como CO₂, agua y sales.
- Recuperación de Recursos: La electrodeposición permite recuperar metales valiosos (como cobre, plata o cadmio) de efluentes industriales. Esto no solo evita la contaminación de los ecosistemas acuáticos, sino que también promueve una economía circular al reintroducir estos metales en la cadena de producción.
- Producción de Desinfectantes Sostenibles: Las celdas electroquímicas pueden generar potentes agentes desinfectantes como ozono (O₃), cloro (Cl₂) o peróxido de hidrógeno (H₂O₂) in situ, es decir, en el mismo lugar donde se van a utilizar. Esto elimina los riesgos y la huella de carbono asociados al transporte de productos químicos peligrosos. El ozono, en particular, es un desinfectante "verde" ideal, ya que se descompone rápidamente en oxígeno sin dejar residuos tóxicos.
- Remediación de Suelos Contaminados: La técnica de remediación electrocinética aplica un campo eléctrico de baja intensidad a suelos contaminados para movilizar y extraer metales pesados y contaminantes orgánicos, limpiando eficazmente el terreno.
Estas aplicaciones demuestran que las celdas electroquímicas son herramientas versátiles y de bajo mantenimiento, capaces de ofrecer soluciones robustas a algunos de los desafíos ambientales más complejos de nuestro tiempo.
Preguntas Frecuentes (FAQ)
- ¿Toda batería es una celda electroquímica?
- Sí. Una batería es, en esencia, una o más celdas electroquímicas de tipo galvánico conectadas en serie o paralelo para proporcionar un voltaje y una corriente específicos. Su función es almacenar energía química y liberarla como energía eléctrica.
- ¿Cuál es la diferencia clave entre una celda galvánica y una electrolítica?
- La principal diferencia es la espontaneidad y el flujo de energía. Una celda galvánica utiliza una reacción química espontánea para generar electricidad. Una celda electrolítica utiliza electricidad externa para forzar una reacción química no espontánea.
- ¿Son las celdas electroquímicas una solución completamente sostenible?
- Tienen un enorme potencial de sostenibilidad, especialmente en la remediación ambiental. Sin embargo, la sostenibilidad global de las baterías (celdas galvánicas) depende críticamente de los materiales utilizados (como el litio o el cobalto), su método de extracción y, fundamentalmente, de la existencia de un sistema de reciclaje eficiente para evitar que se conviertan en residuos peligrosos.
- ¿Por qué es tan importante el puente salino?
- El puente salino es el guardián del equilibrio. A medida que los electrones fluyen, se crea un exceso de carga positiva en la semicelda del ánodo y un exceso de carga negativa en la del cátodo. El puente salino libera iones negativos (aniones) en la semicelda del ánodo y iones positivos (cationes) en la del cátodo para neutralizar estas cargas. Sin este equilibrio iónico, el flujo de electrones se detendría y la celda dejaría de funcionar.
Si quieres conocer otros artículos parecidos a Celdas Electroquímicas: Energía y Sostenibilidad puedes visitar la categoría Ecología.
