01/11/2013
Las aminas alifáticas son compuestos orgánicos que juegan un papel fundamental tanto en los procesos biológicos como en una vasta gama de aplicaciones industriales. Derivadas del amoníaco, su estructura se caracteriza por la sustitución de uno o más átomos de hidrógeno por grupos de carbono, conocidos como grupos alquilo. Esta simple modificación estructural da lugar a una familia de compuestos con propiedades fascinantes y, a menudo, contradictorias: son esenciales para la vida, formando parte de proteínas, vitaminas y hormonas, pero también pueden ser componentes de sustancias tóxicas e irritantes. Comprender qué indica su presencia, cómo se clasifican y cuáles son sus riesgos es crucial para la química, la biología y el cuidado del medio ambiente.
Propiedades Clave para su Identificación
Aunque existen diferentes tipos de aminas, todas comparten ciertas características que permiten su identificación. Estas propiedades no solo son útiles en el laboratorio, sino que también explican su comportamiento en la naturaleza y en la industria. El átomo de nitrógeno central, con su par de electrones libres, es el responsable de muchas de estas características compartidas.
Olor Característico y Penetrante
Una de las formas más directas de detectar la presencia de aminas es a través de su olor. Generalmente, es un olor acre, nocivo e irritante. Las aminas más simples y de bajo peso molecular, como la metilamina y la etilamina, tienen un olor muy similar al del amoníaco. Sin embargo, a medida que su peso molecular aumenta, el olor se transforma, volviéndose distintivamente a pescado. Este olor es, de hecho, el responsable del aroma característico del pescado en descomposición. La trimetilamina es la principal culpable. En otros procesos de descomposición de tejidos, como la carne, la degradación de aminoácidos da lugar a aminas como la putrescina y la cadaverina, cuyos nombres describen elocuentemente su desagradable aroma.
Basicidad: Las Bases de Lewis
Al igual que el amoníaco, las aminas son bases débiles. Se las clasifica como bases de Lewis porque el átomo de nitrógeno posee un par de electrones no compartido que puede donar en una reacción química. La fuerza de esta basicidad varía dependiendo de los grupos alquilo unidos al nitrógeno y otros factores estéricos y de solvatación. Esta propiedad es fundamental para muchas de sus reacciones químicas y aplicaciones, como catalizadores o reguladores de acidez.
Solubilidad y Punto de Ebullición
La solubilidad de las aminas en agua es variable. Las aminas más pequeñas son solubles, pero esta solubilidad disminuye a medida que la cadena de carbono se alarga. Sin embargo, una propiedad interesante es que son mucho más solubles en ácidos diluidos. Esto se debe a que reaccionan con el ácido para formar sales de amonio, que son iónicas y, por lo tanto, se disuelven fácilmente en agua. Por ejemplo, la octilamina es insoluble en agua, pero al reaccionar con ácido nítrico forma nitrato de octilamonio, que sí es soluble.
En cuanto a su punto de ebullición, las aminas se encuentran en un punto intermedio: más alto que el de los hidrocarburos de peso molecular similar, pero más bajo que el de los alcoholes correspondientes. Esto se debe a la capacidad de las aminas primarias y secundarias de formar puentes de hidrógeno, aunque estos son más débiles que los que se forman en los alcoholes.
Clasificación de las Aminas: Una Familia Diversa
Las aminas se clasifican en tres grupos principales (primarias, secundarias y terciarias) según el número de grupos alquilo que han sustituido a los hidrógenos del amoníaco. Existe también un cuarto grupo, las sales de amonio cuaternario.

Aminas Primarias (RNH₂)
En una amina primaria, solo un átomo de hidrógeno del amoníaco ha sido reemplazado por un grupo alquilo (R). Su fórmula general es RNH₂. Un ejemplo común es la metilamina (CH₃NH₂). Se caracterizan por tener dos átomos de hidrógeno unidos al nitrógeno, lo que les permite formar puentes de hidrógeno intermoleculares, haciéndolas menos volátiles que los hidrocarburos equivalentes.
Aminas Secundarias (R₂NH)
Aquí, dos grupos alquilo sustituyen a dos hidrógenos del amoníaco. Estos grupos pueden ser iguales o diferentes. Su fórmula general es R₂NH. La dimetilamina ((CH₃)₂NH) es un ejemplo. Aún conservan un átomo de hidrógeno en el nitrógeno, por lo que también pueden formar puentes de hidrógeno, pero en menor medida que las primarias. Como resultado, sus puntos de ebullición suelen ser ligeramente más bajos que los de las aminas primarias con el mismo número de carbonos.
Aminas Terciarias (R₃N)
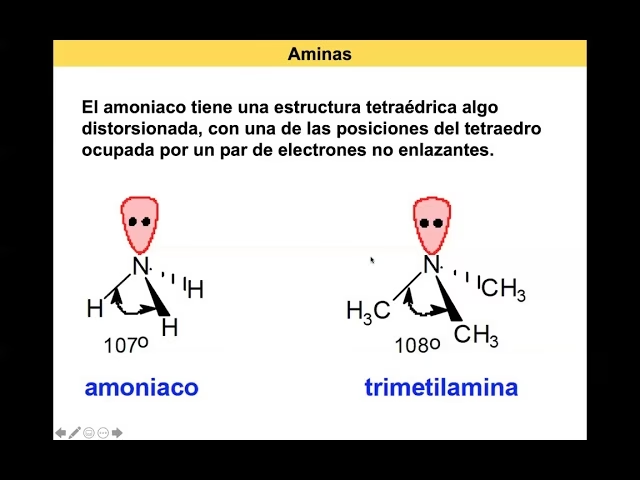
En las aminas terciarias, los tres hidrógenos del amoníaco han sido sustituidos por grupos alquilo. Su fórmula es R₃N, como en la trimetilamina ((CH₃)₃N). Al no tener hidrógenos unidos directamente al nitrógeno, no pueden formar puentes de hidrógeno entre sí. Esta ausencia de enlaces intermoleculares fuertes hace que tengan puntos de ebullición significativamente más bajos que las aminas primarias y secundarias de peso molecular comparable.
Tabla Comparativa de Aminas Alifáticas
| Tipo de Amina | Estructura General | Hidrógenos en el Nitrógeno | Puentes de Hidrógeno | Punto de Ebullición Relativo |
|---|---|---|---|---|
| Primaria | R-NH₂ | 2 | Sí (fuertes) | Alto |
| Secundaria | R₂-NH | 1 | Sí (más débiles) | Intermedio |
| Terciaria | R₃-N | 0 | No (entre sí) | Bajo |
Aplicaciones Industriales: De la Farmacia al Campo
La versatilidad química de las aminas alifáticas las convierte en compuestos intermedios indispensables en innumerables procesos industriales.
- Industria Química: Actúan como catalizadores, disolventes, emulsionantes e inhibidores de la corrosión. La trietanolamina, por ejemplo, se usa para purificar gases al eliminar dióxido de carbono y sulfuro de hidrógeno.
- Industria del Caucho y Plásticos: Se emplean como aceleradores en el proceso de vulcanización del caucho y en la síntesis de polímeros.
- Agricultura: Son precursores en la fabricación de herbicidas, pesticidas y fungicidas. La butilamina es un ejemplo de amina utilizada como pesticida.
- Farmacéutica y Cosmética: Forman parte de la estructura de muchos fármacos y se utilizan en la formulación de jabones, ceras y otros productos de cuidado personal. La dietanolamina es un emulsionante común en cosméticos.
- Otros usos: La metilamina se usa como acelerador en reveladores fotográficos, y la etanolamina como agente reblandecedor de cueros.
Riesgos para la Salud y el Medio Ambiente
A pesar de su utilidad, muchas aminas alifáticas presentan riesgos significativos. Su carácter irritante y su toxicidad requieren un manejo cuidadoso para proteger tanto la salud humana como los ecosistemas.
La exposición a sus vapores puede ser muy dañina. Son extremadamente irritantes para los ojos, la piel y el tracto respiratorio. Dependiendo del compuesto específico, los efectos pueden ser más graves:
- Alilamina: Se ha demostrado que en animales afecta gravemente el corazón y el sistema circulatorio.
- Butilamina: Sus vapores pueden tener efectos severos en el sistema nervioso central, causando depresión e incluso inconsciencia.
- Etilendiamina: Es un potente sensibilizante; la exposición a sus vapores puede provocar reacciones alérgicas en el tracto respiratorio.
- Metilamina: Puede causar fatiga olfatoria, lo que significa que una persona deja de percibir su olor de advertencia, aumentando el riesgo de sobreexposición.
Una de las mayores preocupaciones ambientales y de salud pública es la capacidad de las aminas secundarias y terciarias de reaccionar con nitritos (presentes en alimentos procesados y en el medio ambiente) para formar compuestos N-nitrosos, comúnmente conocidos como nitrosaminas. Muchas de estas nitrosaminas son carcinógenos potentes en animales de laboratorio, lo que plantea una seria preocupación sobre su impacto potencial en la salud humana.
Pruebas de Laboratorio para su Diferenciación
Para distinguir entre los diferentes tipos de aminas en un entorno de laboratorio, los químicos utilizan varias pruebas colorimétricas y de reacción.

La prueba más conocida es la Prueba de Hinsberg. En esta prueba, la amina se hace reaccionar con cloruro de bencenosulfonilo en presencia de una base. El resultado varía drásticamente según el tipo de amina:
- Amina primaria: Forma un producto soluble en la base, resultando en una sola capa clara.
- Amina secundaria: Forma un precipitado insoluble, creando dos capas distintas en la solución.
- Amina terciaria: Generalmente no reacciona, pero el producto puede disolverse en ácido para formar una solución clara.
Otras pruebas como la de Ramini (para aminas alifáticas primarias), la de Simon (para aminas secundarias) y la prueba del ácido nitroso también se utilizan para una identificación más específica.
Preguntas Frecuentes sobre Aminas Alifáticas
¿Por qué algunas aminas huelen a pescado?
El olor a pescado en descomposición se debe principalmente a la presencia de aminas como la trimetilamina. Esta se produce por la descomposición bacteriana de los aminoácidos presentes en los tejidos del pescado.
¿Todas las aminas son peligrosas?
No necesariamente. Las aminas alifáticas inferiores son constituyentes normales de los tejidos corporales y se encuentran en muchos alimentos. Sin embargo, muchas aminas sintéticas utilizadas en la industria son irritantes, tóxicas o corrosivas. El principal riesgo a largo plazo asociado con ciertas aminas es su potencial para formar nitrosaminas cancerígenas.
¿Cuál es la principal diferencia estructural entre una amina primaria y una terciaria?
La diferencia fundamental es el número de átomos de hidrógeno unidos directamente al átomo de nitrógeno. Una amina primaria (RNH₂) tiene dos hidrógenos, mientras que una amina terciaria (R₃N) no tiene ninguno. Esta diferencia afecta drásticamente sus propiedades físicas, como la capacidad de formar puentes de hidrógeno y, por lo tanto, su punto de ebullición.
¿Qué son las nitrosaminas y por qué son una preocupación?
Las nitrosaminas son compuestos que se pueden formar cuando las aminas (especialmente las secundarias) reaccionan con nitritos en condiciones ácidas, como las del estómago humano. La preocupación radica en que muchos de estos compuestos han demostrado ser potentes agentes cancerígenos en estudios con animales.
En conclusión, la presencia de aminas alifáticas indica una química compleja y dual. Son los bloques de construcción de la vida y herramientas indispensables para la industria moderna. Sin embargo, su olor penetrante a menudo sirve como una advertencia de su potencial toxicidad. Conocer sus propiedades, aplicaciones y, sobre todo, sus riesgos es esencial para aprovechar sus beneficios de manera segura y proteger nuestra salud y el medio ambiente.
Si quieres conocer otros artículos parecidos a Aminas Alifáticas: Usos, Riesgos y Detección puedes visitar la categoría Ecología.
