26/09/2007
Cuando pensamos en agua purificada para uso en laboratorio, a menudo imaginamos la molécula de H₂O en su estado más prístino, libre de cualquier contaminante. Sin embargo, la realidad es más compleja. El agua, incluso después de los procesos de purificación inicial, está en constante interacción con su entorno, especialmente con el aire. Esta interacción conduce a la disolución de gases atmosféricos, y uno de ellos, el dióxido de carbono (CO₂), representa un desafío particular y a menudo subestimado para obtener y mantener la calidad del agua ultrapura necesaria en aplicaciones científicas sensibles.
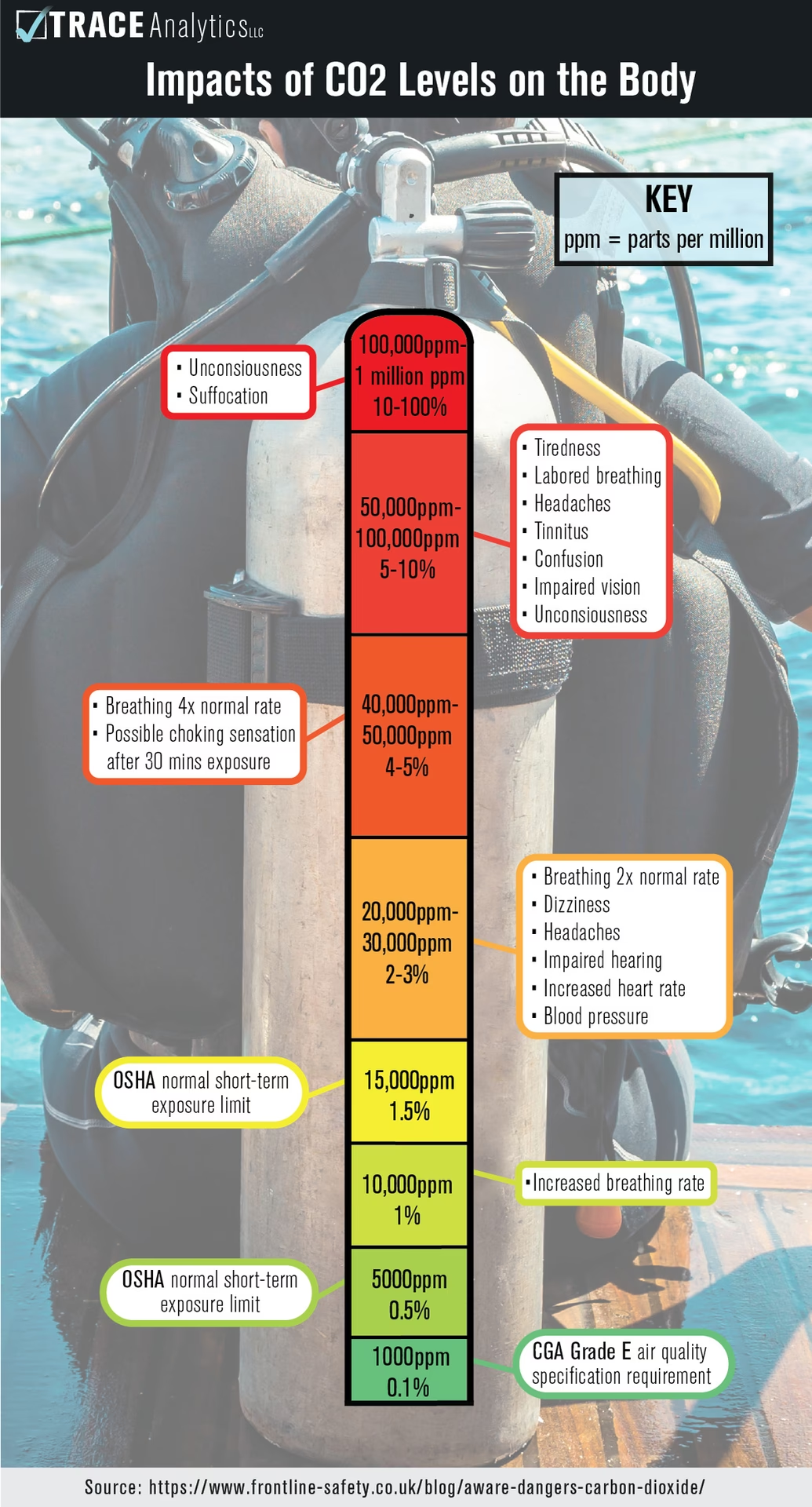
A diferencia de otros gases como el nitrógeno o el oxígeno, el CO₂ no permanece inerte en el agua. Reacciona químicamente para formar un ácido débil que altera propiedades fundamentales del agua, como su pH y su resistividad. Este artículo profundiza en la naturaleza del problema del CO₂ disuelto, su impacto en los sistemas de purificación y en los resultados analíticos, y explora las tecnologías más avanzadas para su eliminación eficaz.
¿Por qué el Dióxido de Carbono es un Problema en el Agua de Laboratorio?
El agua que llega a nuestros laboratorios, ya sea del grifo o pretratada, ha estado en equilibrio con la atmósfera. Por ello, contiene gases disueltos. El dióxido de carbono, al disolverse, inicia una reacción química en cadena que lo convierte en un contaminante iónico activo:
CO₂ + H₂O ⇔ H₂CO₃ (Ácido Carbónico) ⇔ H⁺ + HCO₃⁻ (Ion Hidrógeno + Ion Bicarbonato)
Esta simple ecuación es la raíz de múltiples problemas en el entorno del laboratorio. Los iones resultantes, aunque débiles, tienen efectos significativos y perjudiciales:
- Disminución de la Resistividad: La resistividad eléctrica es la medida estándar de la pureza iónica del agua. Se mide en Megaohmios-centímetro (MΩ·cm). El agua teóricamente pura tiene una resistividad de 18.2 MΩ·cm a 25°C. La presencia de iones como el H⁺ y el HCO₃⁻ aumenta la conductividad del agua y, por lo tanto, reduce drásticamente su resistividad. Una caída en este valor es una señal inequívoca de contaminación iónica, y el CO₂ es un culpable frecuente.
- Reducción del pH: La liberación de iones de hidrógeno (H⁺) acidifica el agua, disminuyendo su pH. Muchas aplicaciones de laboratorio, como la biología celular, la cromatografía líquida de alto rendimiento (HPLC) o la preparación de tampones, son extremadamente sensibles al pH. Un pH incorrecto puede alterar reacciones químicas, afectar la estabilidad de las muestras o dañar equipos como las columnas de cromatografía.
- Agotamiento Prematuro de las Resinas de Purificación: Los sistemas de purificación de agua de laboratorio utilizan cartuchos de resinas de intercambio iónico para eliminar los contaminantes iónicos residuales. El ion bicarbonato (HCO₃⁻) se comporta como un anión débil y es capturado por las resinas de intercambio aniónico. Si el agua de alimentación tiene una alta concentración de CO₂, estas resinas se saturarán mucho más rápido, lo que obligará a sustituir los consumibles con mayor frecuencia, aumentando los costos operativos y el tiempo de inactividad del equipo.
- Interferencia en Técnicas Analíticas: Los gases disueltos, incluido el CO₂, pueden salir de la solución y formar microburbujas cuando cambia la presión o la temperatura. Estas burbujas son un problema grave en técnicas como la espectrofotometría (donde dispersan la luz y causan lecturas erróneas), el recuento de partículas o en los sistemas de dispensación de líquidos de precisión, donde pueden causar imprecisiones en los volúmenes.
El Desafío de la Ósmosis Inversa con el CO₂
La ósmosis inversa (RO) es una tecnología fundamental en la mayoría de los sistemas de purificación de agua. Utiliza una membrana semipermeable para eliminar entre el 95% y el 99% de la mayoría de los contaminantes, incluyendo iones, partículas y materia orgánica. Sin embargo, su eficacia para eliminar gases disueltos como el CO₂ es muy limitada.
Las moléculas de CO₂ son pequeñas y no tienen carga, lo que les permite atravesar la membrana de RO junto con las moléculas de agua. Esto lleva a una situación que a menudo confunde a los usuarios: el agua permeada por la ósmosis inversa (el agua producto) tiene un pH más bajo que el agua de alimentación. ¡No es que se haya añadido un ácido! Lo que ocurre es que la RO elimina eficazmente los iones de bicarbonato y carbonato (alcalinidad) que actúan como un tampón de pH en el agua de alimentación. Al eliminar estos agentes amortiguadores, el efecto acidificante del CO₂ que sí ha atravesado la membrana se vuelve mucho más pronunciado, resultando en una caída del pH.
Métodos Efectivos para la Eliminación de Dióxido de Carbono
Afortunadamente, existen varias tecnologías diseñadas específicamente para abordar el problema del CO₂. La elección del método adecuado dependerá de la escala del sistema, la calidad del agua de alimentación y los requisitos de pureza final.
1. Desgasificación por Membrana
Este es el método más moderno y eficiente para los sistemas de purificación de agua a escala de laboratorio. Utiliza una membrana microporosa hidrofóbica que permite el paso de los gases pero no del agua. El proceso se puede realizar de dos maneras:
- Barrido con Aire: Se hace pasar un flujo de aire a baja presión por un lado de la membrana. Esto crea un gradiente de presión parcial que "empuja" al CO₂ fuera del agua y a través de la membrana.
- Aplicación de Vacío: Un enfoque más avanzado consiste en aplicar un vacío en el lado seco de la membrana. Esto "succiona" eficazmente el CO₂ y otros gases disueltos fuera del agua. Esta técnica, utilizada por sistemas como los de ELGA LabWater, es muy eficiente y simplifica el diseño del sistema al no requerir una fuente de aire comprimido.
La desgasificación por membrana es altamente efectiva, pudiendo reducir la concentración de CO₂ a menos de 1 mg/l antes de las etapas finales de pulido.
2. Conversión Química y Filtración
Este método aborda el problema convirtiendo el CO₂ en una forma que la membrana de ósmosis inversa sí puede eliminar. Consiste en dosificar una base, como hidróxido de sodio (NaOH), en el agua de alimentación antes de la RO. Esto eleva el pH por encima de 8.5, lo que convierte todo el CO₂ disuelto en iones de bicarbonato (HCO₃⁻). Estos iones, al tener carga, son rechazados eficazmente por la membrana de RO. Si bien es un método efectivo, especialmente en sistemas industriales de gran tamaño, su implementación a escala de laboratorio es más compleja y requiere el manejo de productos químicos.
3. Purificación por Intercambio Iónico
Como se mencionó anteriormente, las resinas de lecho mixto en los cartuchos de pulido final son extremadamente eficaces para eliminar los iones de bicarbonato. Sin embargo, depender únicamente de este método para eliminar altas cargas de CO₂ es económicamente inviable. Las resinas se agotarán rápidamente, lo que resultará en altos costos de consumibles. Por lo tanto, el intercambio iónico debe considerarse como una etapa de pulido final, no como el método principal para la eliminación de CO₂.
Tabla Comparativa de Métodos de Eliminación de CO₂
| Método | Eficiencia | Costo Operativo | Complejidad | Aplicación Ideal |
|---|---|---|---|---|
| Desgasificación por Membrana | Muy Alta | Bajo | Baja (integrada en el sistema) | Sistemas de laboratorio y a gran escala. |
| Conversión Química + RO | Muy Alta | Medio (costo de químicos) | Alta (dosificación y control) | Sistemas industriales a gran escala. |
| Intercambio Iónico | Excelente (hasta agotamiento) | Alto (reemplazo frecuente) | Muy Baja (cartucho) | Etapa de pulido final, no para eliminación masiva. |
¿Cuándo es Crucial Implementar un Sistema de Desgasificación?
Si bien la eliminación de CO₂ es siempre beneficiosa para la calidad del agua y la longevidad del sistema, se vuelve absolutamente crítica en situaciones donde el agua de alimentación presenta ciertas características:
- Agua con pH bajo (inferior a 6.0): Un pH bajo indica que una mayor proporción del carbono inorgánico total ya está en forma de CO₂ disuelto, lo que representa una carga mayor para el sistema de purificación.
- Agua con alta alcalinidad de bicarbonato (superior a 200 mg/l): Una alta alcalinidad significa que hay una gran cantidad de bicarbonato en el agua. Este bicarbonato se convertirá en CO₂ a medida que el agua atraviesa las diferentes etapas del sistema, especialmente después de la RO.
En estos casos, invertir en un sistema con una unidad de desgasificación integrada no es un lujo, sino una necesidad para garantizar un rendimiento constante, una calidad de agua óptima y unos costos operativos controlados.
Preguntas Frecuentes (FAQ) sobre el CO₂ en Agua Pura
¿Por qué el agua purificada con ósmosis inversa tiene un pH más bajo que el agua de la red?
Esto se debe a que la membrana de ósmosis inversa elimina los iones (como el bicarbonato) que actúan como amortiguadores del pH, pero no elimina el CO₂ disuelto. Sin los amortiguadores, el efecto acidificante del CO₂ (que forma ácido carbónico) se hace mucho más evidente, provocando una caída del pH.

¿El CO₂ disuelto en el agua es peligroso para la salud?
En el agua potable, el CO₂ disuelto no representa un riesgo directo para la salud humana. De hecho, es lo que le da el sabor característico y la efervescencia al agua con gas. En el contexto del laboratorio, el peligro no es para el usuario, sino para la integridad del experimento, la precisión de los análisis y la vida útil de los equipos de purificación.
¿Cómo puedo saber si mi agua de alimentación tiene altos niveles de CO₂?
Una analítica completa del agua de alimentación es la mejor manera. Los parámetros clave a observar son el pH y la alcalinidad total (o alcalinidad de bicarbonato). Un pH bajo y/o una alcalinidad alta son indicadores claros de que la eliminación de CO₂ será un factor importante a considerar al elegir un sistema de purificación de agua.
¿La ebullición del agua elimina el CO₂?
Sí, la ebullición reduce la solubilidad de todos los gases en el agua, incluido el CO₂. Sin embargo, este no es un método práctico ni eficiente para la purificación de agua a escala de laboratorio. Además, tan pronto como el agua se enfría y entra en contacto con el aire, comenzará a reabsorber CO₂ de nuevo.
En conclusión, el dióxido de carbono es un componente invisible pero influyente en la química del agua de laboratorio. Su capacidad para afectar el pH, la resistividad y la eficiencia de los consumibles lo convierte en un factor crítico que debe ser gestionado. La implementación de tecnologías de desgasificación avanzadas es la estrategia más efectiva para neutralizar su impacto, asegurando que el agua utilizada en los procedimientos científicos sea de la más alta pureza y no se convierta en una variable oculta que pueda comprometer la validez y reproducibilidad de los resultados.
Si quieres conocer otros artículos parecidos a CO2 en Agua de Laboratorio: Cómo Eliminarlo puedes visitar la categoría Ecología.

