08/10/2007
En el vasto y complejo lenguaje de la química que describe nuestro mundo, pocas familias de compuestos tienen un papel tan dual y omnipresente como los óxidos no metálicos. A menudo invisibles, presentes en el aire que respiramos y formados por la unión de elementos como el carbono, el azufre o el nitrógeno con el oxígeno, estos compuestos son tanto arquitectos de la vida y la industria como agentes de profundo desequilibrio ecológico. Desde el dióxido de carbono que nutre a las plantas hasta los gases que envenenan nuestros cielos, entender su naturaleza es fundamental para abordar algunos de los mayores desafíos ambientales de nuestra era. Este artículo se adentra en el mundo de los óxidos no metálicos para desentrañar su química, sus usos y, sobre todo, su crucial impacto en la salud de nuestro planeta.
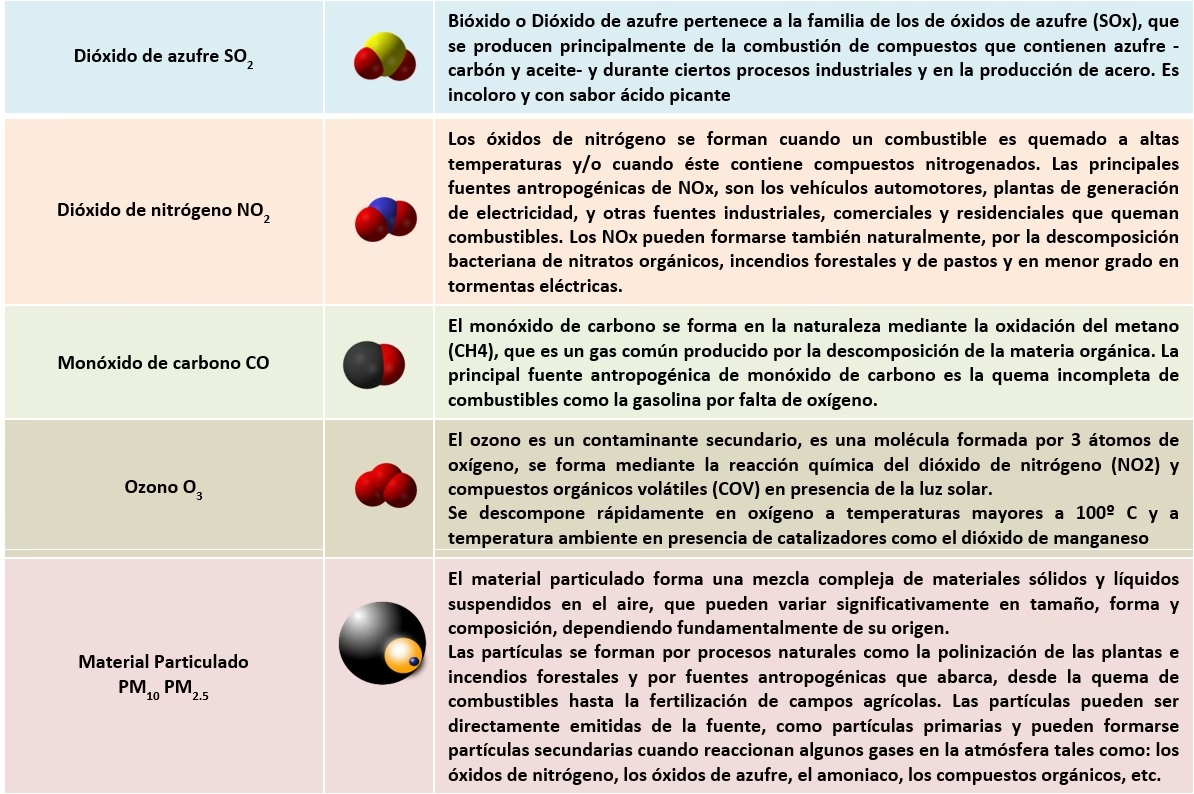
¿Qué son los Óxidos No Metálicos y por qué son tan Relevantes?
Un óxido no metálico, también conocido históricamente como anhídrido, es un compuesto químico que resulta de la combinación de un elemento no metálico con el oxígeno. Su naturaleza química les confiere propiedades muy particulares. Debido a que sus átomos se unen mediante enlaces covalentes, a menudo son moléculas pequeñas y poco polares. Esta característica explica por qué, en condiciones normales de presión y temperatura, la mayoría de ellos se encuentran en estado gaseoso. Pensemos en el dióxido de carbono (CO₂), el dióxido de azufre (SO₂) o los diversos óxidos de nitrógeno (NOx); todos ellos son gases que juegan un papel crucial en la dinámica atmosférica.
Cuando se presentan en estado sólido, como el dióxido de silicio (SiO₂), que es el componente principal de la arena y el vidrio, carecen de brillo metálico y suelen ser quebradizos. A diferencia de los metales, no son buenos conductores del calor ni de la electricidad. Esta diversidad de estados y propiedades es lo que les permite tener aplicaciones tan variadas y, al mismo tiempo, ser protagonistas de fenómenos de contaminación a gran escala.
La Formación: Procesos Naturales vs. Impacto Humano
La mayoría de estos óxidos se forman por reacción directa del elemento no metálico con el oxígeno, un proceso que vemos a diario en la combustión. Sin embargo, el resultado de esta reacción depende enormemente de las condiciones. Por ejemplo, cuando el carbono se quema con abundante oxígeno, se forma dióxido de carbono (CO₂), el gas que exhalamos y que es fundamental para la fotosíntesis. Pero si la combustión ocurre con déficit de oxígeno, como en un motor de coche mal ajustado, se produce monóxido de carbono (CO), un gas altamente tóxico.
Esta dualidad se repite con otros elementos:
- Azufre: La quema de combustibles fósiles como el carbón o el petróleo, que contienen impurezas de azufre, libera directamente dióxido de azufre (SO₂). Una vez en la atmósfera, este gas puede oxidarse aún más para formar trióxido de azufre (SO₃).
- Nitrógeno: Aunque el nitrógeno es el gas más abundante en nuestra atmósfera, no reacciona fácilmente con el oxígeno. Sin embargo, a las altas temperaturas que se alcanzan en los motores de combustión interna o en las centrales eléctricas, el nitrógeno y el oxígeno atmosféricos sí reaccionan, formando óxidos de nitrógeno como el monóxido de nitrógeno (NO) y el dióxido de nitrógeno (NO₂).
Si bien existen fuentes naturales de estos gases, como las erupciones volcánicas que liberan SO₂ o los procesos bacterianos del suelo que emiten óxido nitroso (N₂O), la actividad industrial y el transporte han multiplicado exponencialmente su concentración en la atmósfera, alterando equilibrios químicos que han permanecido estables durante milenios.
El Lado Oscuro: Protagonistas de la Crisis Ambiental
La verdadera preocupación ambiental con muchos óxidos no metálicos radica en su comportamiento al entrar en contacto con el agua. Reaccionan para formar ácidos, de ahí su nombre clásico de anhídridos (que significa "sin agua"). Este simple proceso químico es la raíz de graves problemas ecológicos.
La Lluvia Ácida: Cuando el Cielo Llora Ácido
El dióxido de azufre (SO₂) y los óxidos de nitrógeno (NOx) son los principales precursores de la lluvia ácida. Al ser liberados a la atmósfera, viajan con el viento y reaccionan con el vapor de agua, el oxígeno y otros químicos para formar ácido sulfúrico (H₂SO₄) y ácido nítrico (HNO₃). Estas sustancias caen a la tierra en forma de lluvia, nieve o niebla, acidificando suelos, lagos y ríos. Las consecuencias son devastadoras: muerte de peces, daños a los bosques, corrosión de edificios y monumentos históricos. Es un claro ejemplo de cómo la contaminación local puede convertirse en un problema regional e incluso transfronterizo.
El Efecto Invernadero y el Calentamiento Global
Dos óxidos no metálicos son actores principales en el drama del cambio climático: el dióxido de carbono (CO₂) y el óxido nitroso (N₂O). Aunque el CO₂ es el más famoso, el N₂O es un gas de efecto invernadero aproximadamente 300 veces más potente que el CO₂ a lo largo de un siglo. El CO₂, proveniente principalmente de la quema de combustibles fósiles, y el N₂O, emitido en gran parte por prácticas agrícolas y el uso de fertilizantes nitrogenados, actúan como una manta que atrapa el calor del sol en la atmósfera, elevando la temperatura media del planeta y provocando alteraciones climáticas extremas.

Contaminación del Aire y Salud Pública
El dióxido de nitrógeno (NO₂) es un gas pardo-rojizo que, además de contribuir a la lluvia ácida, es un irritante respiratorio directo. Es un componente clave del smog fotoquímico que tiñe de una bruma marrón las grandes ciudades, causando problemas de asma, bronquitis y otras enfermedades pulmonares, especialmente en niños y ancianos.
Usos Beneficiosos: No Todos son Villanos
A pesar de su reputación ambiental, es crucial reconocer que los óxidos no metálicos también son indispensables para nuestra sociedad y tecnología. El equilibrio está en gestionar sus riesgos mientras se aprovechan sus beneficios.
| Óxido No Metálico | Fórmula | Uso Principal | Impacto Ambiental Principal |
|---|---|---|---|
| Dióxido de Silicio | SiO₂ | Fabricación de vidrio, cemento, cerámica. Componente de la arena. | Generalmente inerte y no contaminante en su forma sólida. |
| Óxido Nitroso | N₂O | Anestésico y analgésico ("gas de la risa"), aditivo en combustibles. | Potente gas de efecto invernadero. |
| Dióxido de Carbono | CO₂ | Bebidas carbonatadas, extintores de incendios, esencial para la fotosíntesis. | Principal gas de efecto invernadero causante del cambio climático. |
| Trióxido de Azufre | SO₃ | Producción a gran escala de ácido sulfúrico para la industria. | Principal precursor de la lluvia ácida al reaccionar con el agua. |
| Dióxido de Nitrógeno | NO₂ | Intermediario en la síntesis de ácido nítrico. | Contaminante del aire, causa problemas respiratorios y lluvia ácida. |
Preguntas Frecuentes (FAQ)
¿Todos los óxidos no metálicos son gaseosos y contaminantes?
No. El ejemplo más claro es el dióxido de silicio (SiO₂), que constituye la arena y el cuarzo. Es un sólido extremadamente estable e inerte, y no representa una amenaza ambiental directa. La peligrosidad suele estar asociada a los óxidos gaseosos de carbono, azufre y nitrógeno debido a su capacidad de dispersarse en la atmósfera y reaccionar para formar compuestos dañinos.
¿Cuál es la diferencia entre el monóxido de carbono (CO) y el dióxido de carbono (CO₂)?
Ambos son óxidos de carbono, pero difieren en su composición y efectos. El CO se forma en una combustión incompleta y es un gas tóxico que puede ser letal para los seres vivos al interferir con el transporte de oxígeno en la sangre. El CO₂, resultado de la combustión completa, no es directamente tóxico en bajas concentraciones (de hecho, es vital para las plantas), pero su acumulación en la atmósfera es la principal causa del calentamiento global.
¿Es posible eliminar la contaminación por estos óxidos?
Eliminarla por completo es muy difícil, pero reducirla drásticamente es posible y necesario. Esto implica una transición energética hacia fuentes renovables que no emitan CO₂, SO₂ o NOx; la implementación de tecnologías como los convertidores catalíticos en los vehículos para transformar los gases nocivos en otros más inocuos; y el uso de "lavadores" o "scrubbers" en las chimeneas industriales para capturar el dióxido de azufre antes de que llegue a la atmósfera.
Conclusión: Un Llamado al Equilibrio y la Responsabilidad
Los óxidos no metálicos son un testimonio perfecto de la dualidad de la química: herramientas poderosas para el progreso humano, pero también fuentes potenciales de un daño ambiental inmenso. Su historia está intrínsecamente ligada a la nuestra, desde la primera fogata que liberó CO₂ hasta la revolución industrial que llenó los cielos de los precursores de la lluvia ácida. Comprender su comportamiento no es solo un ejercicio académico; es una necesidad urgente. La solución a los problemas que plantean no reside en demonizarlos, sino en gestionar su producción y liberación con inteligencia, innovación y un profundo sentido de la responsabilidad hacia el único planeta que tenemos.
Si quieres conocer otros artículos parecidos a Óxidos No Metálicos: El Doble Filo Ambiental puedes visitar la categoría Medioambiente.

