10/06/2002
El amoníaco, cuya fórmula química es NH3, es uno de los compuestos más producidos y utilizados a nivel mundial. Este gas incoloro, de olor penetrante y característico, juega un papel dual en nuestro mundo: por un lado, es un pilar fundamental para la agricultura moderna y numerosos procesos industriales; por otro, representa un compuesto que, si no se maneja con la debida precaución, puede acarrear significativos riesgos para la salud humana y el medio ambiente. Desde su formación natural en la descomposición de la materia orgánica hasta su síntesis a gran escala mediante el proceso Haber-Bosch, el amoníaco es una molécula omnipresente cuya comprensión es vital para avanzar hacia un futuro más sostenible.

- ¿Qué es el Amoníaco (NH3)? Un Vistazo Químico Profundo
- Nomenclatura del Amoníaco: Los Diferentes Nombres del NH3
- Propiedades Físicas y Químicas Clave
- El Proceso Haber-Bosch: La Revolución Industrial del Amoníaco
- Usos del Amoníaco: De la Agricultura a la Industria
- El Doble Filo: Impacto Ambiental y Riesgos para la Salud
- Manejo Seguro y Precauciones Esenciales
- Preguntas Frecuentes (FAQ) sobre el Amoníaco
¿Qué es el Amoníaco (NH3)? Un Vistazo Químico Profundo
En su nivel más básico, el amoníaco es una molécula compuesta por un átomo de nitrógeno (N) unido covalentemente a tres átomos de hidrógeno (H). Esta configuración le confiere una geometría molecular piramidal trigonal, con el átomo de nitrógeno en el vértice y los tres hidrógenos formando la base. El ángulo entre los enlaces H-N-H es de aproximadamente 107 grados.
Esta estructura no es trivial; es la responsable de muchas de sus propiedades más importantes. El nitrógeno, al ser más electronegativo que el hidrógeno, atrae los electrones de los enlaces, generando una polaridad en la molécula. Además, el nitrógeno posee un par de electrones no enlazantes, lo que le permite actuar como una base de Lewis, aceptando protones. Cuando el amoníaco se disuelve en agua, reacciona para formar el ion amonio (NH4+), comportándose como una base débil y aumentando el pH de la solución. Esta capacidad para formar puentes de hidrógeno entre sus moléculas explica por qué es tan soluble en agua y tiene puntos de ebullición y fusión más altos de lo que se esperaría para una molécula de su tamaño.
Nomenclatura del Amoníaco: Los Diferentes Nombres del NH3
Aunque comúnmente lo conocemos como amoníaco, este compuesto tiene diferentes nombres según el sistema de nomenclatura química que se utilice. Conocerlos es importante para evitar confusiones en contextos técnicos o académicos.
| Tipo de Nomenclatura | Nombre del Compuesto |
|---|---|
| Nomenclatura Tradicional | Amoníaco |
| Nomenclatura Sistemática (IUPAC) | Trihidruro de nitrógeno |
El nombre "amoníaco" es el más extendido y aceptado en el lenguaje común e industrial, mientras que "trihidruro de nitrógeno" describe de forma precisa su composición atómica, siguiendo las reglas de la Unión Internacional de Química Pura y Aplicada (IUPAC).

Propiedades Físicas y Químicas Clave
Las propiedades del amoníaco determinan su comportamiento y sus aplicaciones. A continuación, se detallan las más relevantes:
Propiedades Físicas
- Estado: A temperatura y presión ambiente, es un gas incoloro.
- Olor: Presenta un olor muy fuerte, irritante y sofocante.
- Punto de Ebullición: -33.34 °C. Esta temperatura relativamente alta para su masa molar se debe a los fuertes puentes de hidrógeno.
- Punto de Fusión: -77.73 °C.
- Densidad: Es más ligero que el aire, con una densidad de 0.73 kg/m³.
- Solubilidad: Es extremadamente soluble en agua, pudiendo disolverse hasta 89 gramos en 100 mL de agua a 20°C.
- Masa Molar: 17.031 g/mol.
Propiedades Químicas
- Basicidad: Como se mencionó, actúa como una base débil en soluciones acuosas.
- Reactividad con Ácidos: Reacciona vigorosamente con ácidos para formar sales de amonio. Por ejemplo, con ácido clorhídrico (HCl) forma cloruro de amonio (NH4Cl).
- Formación de Complejos: Su par de electrones libres le permite actuar como ligando, formando complejos con iones de metales de transición, como el cobre y la plata.
- Reacciones Redox: Puede participar en reacciones de oxidación-reducción. Puede ser oxidado para formar nitrógeno gaseoso (N2) u óxidos de nitrógeno.
El Proceso Haber-Bosch: La Revolución Industrial del Amoníaco
La producción de amoníaco a escala industrial fue uno de los mayores hitos científicos del siglo XX. El proceso Haber-Bosch, desarrollado por los químicos alemanes Fritz Haber y Carl Bosch, permitió sintetizar amoníaco directamente a partir de nitrógeno atmosférico (N2) e hidrógeno (H2). La reacción es la siguiente: N₂(g) + 3H₂(g) ↔ 2NH₃(g).
Este proceso requiere condiciones extremas: altas presiones (150-250 atmósferas) y altas temperaturas (400-500 °C), además del uso de un catalizador, generalmente a base de hierro. A pesar de su alto consumo energético, el proceso Haber-Bosch transformó la agricultura al hacer posible la producción masiva de fertilizantes nitrogenados, lo que permitió alimentar a una población mundial en rápido crecimiento. Hoy en día, sigue siendo el principal método de producción de amoníaco en todo el mundo.
Usos del Amoníaco: De la Agricultura a la Industria
La versatilidad del amoníaco lo convierte en un compuesto indispensable en múltiples sectores:
Agricultura: El Pilar de la Alimentación
Más del 80% de la producción mundial de amoníaco se destina a la fabricación de fertilizante. El nitrógeno es un macronutriente esencial para el crecimiento de las plantas, ya que forma parte de las proteínas, los ácidos nucleicos (ADN y ARN) y la clorofila. El amoníaco, ya sea aplicado directamente como amoníaco anhidro o convertido en urea y nitrato de amonio, proporciona a los cultivos el nitrógeno necesario para maximizar su rendimiento.
Industria Química
Es una materia prima clave para la síntesis de una vasta gama de productos químicos, incluyendo:
- Ácido nítrico: Fundamental para la producción de explosivos como el TNT y fertilizantes como el nitrato de amonio.
- Urea: Además de su uso como fertilizante, se emplea en la fabricación de plásticos y resinas.
- Fibras sintéticas: Como el nailon y el rayón.
- Productos farmacéuticos: Es un precursor en la síntesis de muchos medicamentos.
Refrigeración Industrial
El amoníaco (conocido en este sector como R-717) es un refrigerante altamente eficiente. Posee excelentes propiedades termodinámicas, lo que se traduce en un menor consumo de energía en los sistemas de refrigeración. Además, tiene un Potencial de Calentamiento Global (PCG) y un Potencial de Agotamiento de Ozono (PAO) nulos, lo que lo convierte en una alternativa mucho más ecológica que los clorofluorocarbonos (CFC) y los hidrofluorocarbonos (HFC).
Limpieza y Otros Usos
Las soluciones acuosas de amoníaco son excelentes desengrasantes y se utilizan en numerosos productos de limpieza para el hogar y la industria. También se emplea en la producción de pulpa y papel y en el tratamiento de aguas residuales para eliminar contaminantes nitrogenados.
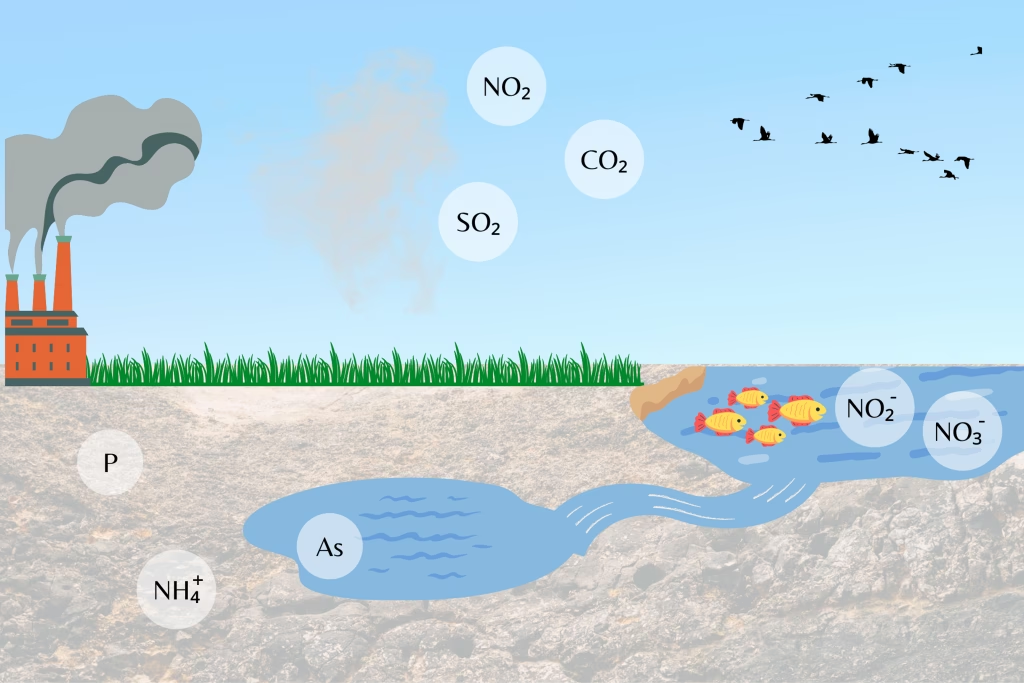
El Doble Filo: Impacto Ambiental y Riesgos para la Salud
A pesar de sus inmensos beneficios, el uso extensivo del amoníaco conlleva importantes desafíos ambientales y de seguridad.
Impacto Ambiental
La gestión inadecuada del amoníaco puede tener graves consecuencias ecológicas. La principal preocupación proviene de su uso en la agricultura. El exceso de fertilizantes nitrogenados no absorbido por los cultivos puede ser arrastrado por la lluvia hacia ríos y lagos. Este aporte masivo de nutrientes provoca un fenómeno conocido como eutrofización, que consiste en el crecimiento descontrolado de algas. Estas algas consumen el oxígeno del agua al descomponerse, creando "zonas muertas" donde la vida acuática no puede sobrevivir.
Además, las emisiones de amoníaco a la atmósfera contribuyen a la formación de partículas finas (PM2.5), que afectan la calidad del aire y pueden causar problemas respiratorios. También puede reaccionar en la atmósfera para formar óxidos de nitrógeno, precursores de la lluvia ácida.
Riesgos para la Salud
El amoníaco es un compuesto tóxico y corrosivo. La exposición a altas concentraciones de gas puede causar quemaduras graves en la piel, los ojos, la garganta y los pulmones. La inhalación puede provocar desde una irritación leve hasta un edema pulmonar potencialmente mortal. Por ello, su manejo requiere seguir protocolos de seguridad muy estrictos.
Manejo Seguro y Precauciones Esenciales
Para mitigar los riesgos asociados al amoníaco, es fundamental adoptar medidas de seguridad rigurosas:
- Almacenamiento: Debe guardarse en tanques presurizados, en áreas bien ventiladas y lejos de fuentes de calor o ignición.
- Equipo de Protección Personal (EPP): Es obligatorio el uso de guantes, gafas de seguridad o protectores faciales, y ropa de protección especializada al manipular amoníaco. En caso de riesgo de inhalación, se deben usar respiradores adecuados.
- Capacitación: Todo el personal que trabaje con amoníaco debe recibir una formación completa sobre sus propiedades, riesgos y procedimientos de emergencia.
- Planes de Emergencia: Se deben tener establecidos planes de acción claros y simulacros periódicos para actuar de forma rápida y eficaz en caso de fugas o derrames.
Preguntas Frecuentes (FAQ) sobre el Amoníaco
- ¿Qué es el amoníaco y para qué se utiliza principalmente?
- El amoníaco (NH3) es un compuesto químico gaseoso formado por nitrógeno e hidrógeno. Su uso principal, abarcando más del 80% de su producción, es la fabricación de fertilizantes para la agricultura. También se usa en refrigeración, limpieza y como materia prima en la industria química.
- ¿Cuáles son las propiedades más destacadas del amoníaco?
- Es un gas incoloro con un olor muy penetrante, altamente soluble en agua y con un punto de ebullición de -33.34°C. Químicamente, actúa como una base débil y es muy reactivo, especialmente con los ácidos.
- ¿Qué precauciones se deben tomar al manipular amoníaco?
- Debido a su toxicidad y naturaleza corrosiva, es crucial manipularlo con cuidado. Se debe utilizar equipo de protección personal completo (guantes, gafas, ropa protectora), asegurar una buena ventilación y tener planes de emergencia para fugas. La inhalación de sus vapores puede ser muy peligrosa.
- ¿Cuál es el principal impacto ambiental del amoníaco?
- Su principal impacto ambiental está ligado a su uso como fertilizante. El exceso aplicado a los campos puede contaminar cuerpos de agua, causando eutrofización y dañando los ecosistemas acuáticos. Sus emisiones a la atmósfera también contribuyen a la contaminación del aire.
- ¿Cómo se mide la toxicidad del amoníaco en el agua?
- La toxicidad del amoníaco en el agua depende en gran medida del pH y la temperatura. Para medirla con precisión, se utilizan métodos como el del salicilato, pero los resultados deben interpretarse siempre junto con los valores de pH y temperatura del agua, ya que estos factores determinan qué proporción del amoníaco total está en su forma tóxica no ionizada (NH3).
Si quieres conocer otros artículos parecidos a Amoníaco (NH3): Usos, Riesgos y Rol Ambiental puedes visitar la categoría Ecología.
