16/05/2002
En el mundo de la ciencia y la investigación, especialmente en campos como la genómica y la epidemiología, la precisión no es solo un objetivo, es la base sobre la que se construyen todos los descubrimientos. Cuando estudiamos organismos microscópicos como los virus, nos enfrentamos a un desafío monumental: trabajar con cantidades de material genético increíblemente pequeñas. Para poder 'ver' y analizar este material, necesitamos un proceso llamado amplificación, que actúa como una fotocopiadora molecular, creando millones de copias a partir de una sola hebra de ADN o ARN. Sin embargo, este poderoso proceso tiene un talón de Aquiles: el riesgo de contaminación cruzada. Una minúscula partícula de una muestra puede viajar por el aire y aterrizar en otra, un pequeño error de pipeteo puede transferir material no deseado, o residuos en el equipo pueden falsear los resultados. Cuando esto ocurre, la fotocopiadora molecular no distingue entre lo correcto y lo incorrecto, y amplifica todo por igual. El resultado es un caos de datos que puede llevar a diagnósticos erróneos, a trazar rutas de transmisión falsas de una enfermedad o, en el contexto ambiental, a identificar incorrectamente la presencia de un microorganismo en un ecosistema. Es una amenaza silenciosa que pone en jaque la integridad de la investigación. Afortunadamente, la innovación científica ha desarrollado un ingenioso sistema de vigilancia para combatir a este enemigo invisible.
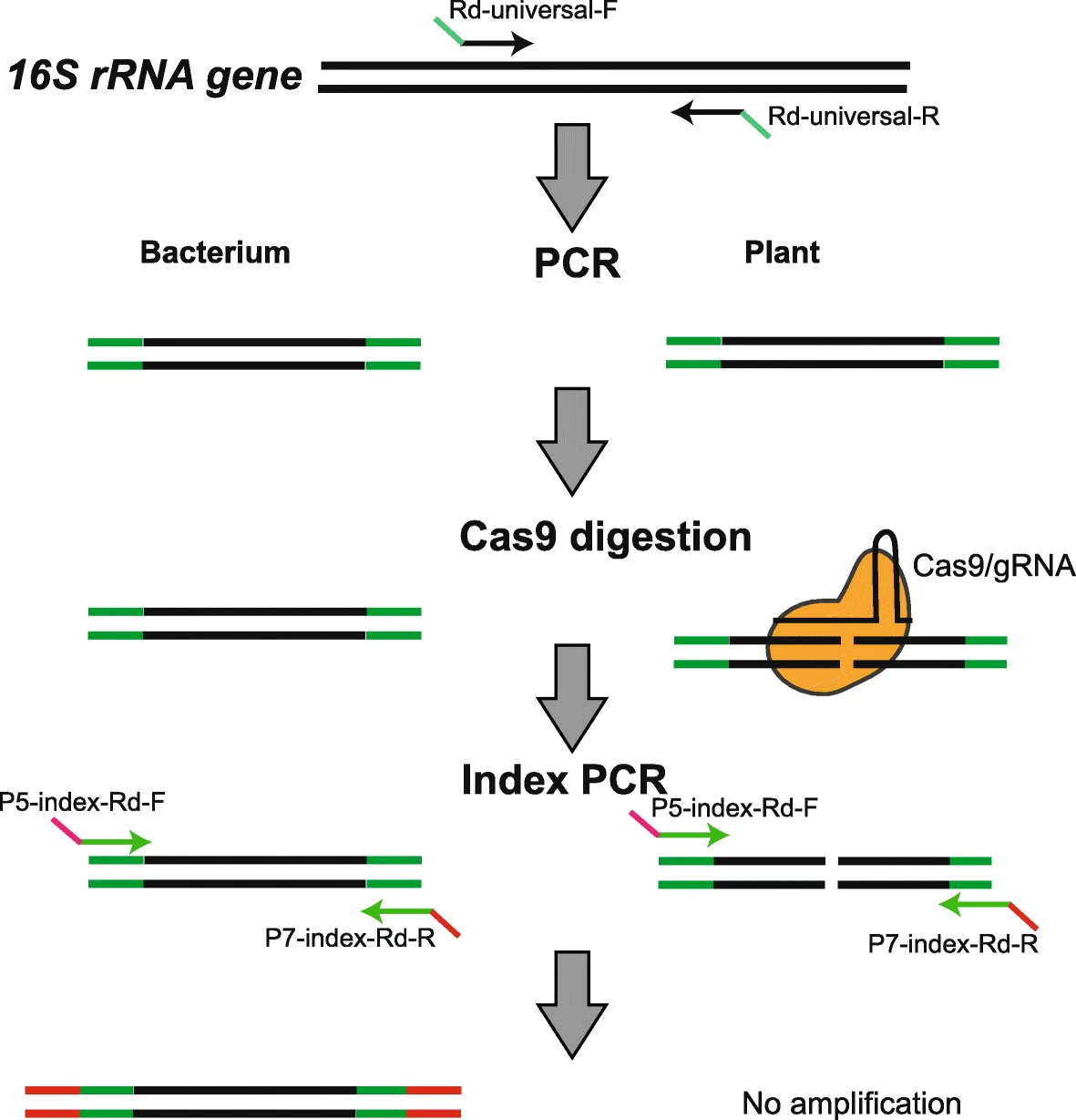
- El Campo Minado de la Amplificación por PCR
- Un Guardián Sintético: La Solución de los SDSI
- Validación Exhaustiva: Asegurando que el Guardián no Interfiere
- Tabla Comparativa: Secuenciación con y sin Trazadores Sintéticos
- Aplicación en el Mundo Real: Rastreo de un Brote Nosocomial
- Preguntas Frecuentes (FAQ)
El Campo Minado de la Amplificación por PCR
La técnica más común para la amplificación es la Reacción en Cadena de la Polimerasa (PCR, por sus siglas en inglés). Imagina que tienes un libro con una sola palabra escrita en una página y necesitas leerla, pero es demasiado pequeña. La PCR toma esa palabra y la reescribe millones de veces hasta que llena un capítulo entero, haciéndola fácil de leer. Este proceso es fundamental para detectar la presencia de un virus en una muestra de un paciente, incluso si la carga viral es muy baja.
El problema surge porque la PCR es extraordinariamente sensible. Esta sensibilidad es su mayor fortaleza y, a la vez, su mayor debilidad. Si una mota de polvo que lleva ADN de una muestra anterior cae en tu nuevo experimento, la PCR la amplificará con la misma eficiencia que a tu muestra de interés. Esto es la contaminación cruzada. En los laboratorios de alto rendimiento, donde se procesan cientos o miles de muestras al día, el riesgo se multiplica. Los aerosoles generados al abrir un tubo, las puntas de las pipetas reutilizadas por error o incluso la circulación del aire pueden actuar como vehículos para estos contaminantes invisibles. El resultado es que una muestra negativa podría parecer positiva, o peor aún, la secuencia genética de un virus de un paciente podría asignarse erróneamente a otro, creando un mapa epidemiológico completamente falso.
Un Guardián Sintético: La Solución de los SDSI
Para resolver este problema crítico, los científicos han desarrollado una solución elegante y robusta: los Trazadores Sintéticos de ADN o 'Spike-ins' (SDSI, por sus siglas en inglés). La idea es simple pero brillante: antes de comenzar cualquier proceso de amplificación, se añade a cada muestra una pequeña cantidad de una secuencia de ADN única y artificial. Esta secuencia actúa como un código de barras genético.
Estos SDSI están diseñados meticulosamente para ser completamente ajenos a cualquier organismo conocido. Los investigadores utilizan herramientas bioinformáticas para asegurarse de que estas secuencias sintéticas no se parezcan en nada al genoma humano, a los genomas virales que se están estudiando, ni a bacterias comunes. Son, en esencia, una firma genética que no existe en la naturaleza. A cada muestra de un lote (por ejemplo, en una placa de 96 pocillos) se le asigna un SDSI único. La muestra del paciente A recibe el código de barras 001, la del paciente B el 002, y así sucesivamente.
Una vez que todas las muestras han sido 'etiquetadas' con su SDSI, se someten al proceso de amplificación y secuenciación. Al final, cuando se analizan los datos, el primer paso es buscar estos códigos de barras. Si en la muestra del paciente A (que solo debería tener el SDSI 001) se detecta una pequeña cantidad del SDSI 002, se enciende una alarma. Esto es una prueba irrefutable de que ha habido una contaminación desde la muestra del paciente B. No solo eso, sino que la cantidad de SDSI 'contaminante' que se detecta permite cuantificar el nivel de la contaminación. Esto transforma la duda en certeza y permite a los investigadores descartar datos poco fiables o corregirlos, asegurando la integridad de los datos.
Validación Exhaustiva: Asegurando que el Guardián no Interfiere
Introducir un elemento extraño en un experimento delicado requiere una validación extremadamente rigurosa. Los científicos responsables de desarrollar el método SDSI realizaron una batería de pruebas para garantizar que su 'guardián' no se convirtiera en un problema en sí mismo.
- No Interferencia: La primera y más importante pregunta era si los SDSI y sus cebadores (las pequeñas moléculas que inician la amplificación) interferirían con la amplificación del virus real. Los experimentos demostraron que, en las concentraciones adecuadas, los SDSI se amplifican eficientemente sin afectar la recuperación del genoma viral. La presencia del código de barras no impide leer el mensaje principal.
- Especificidad: Se confirmó mediante simulaciones computacionales (in silico) y experimentos de laboratorio (in vitro) que los cebadores de los SDSI solo amplificaban los SDSI y no se unían accidentalmente a otras partes del material genético de la muestra.
- Rendimiento Consistente: Se optimizaron todos los aspectos del proceso, desde las enzimas de PCR utilizadas hasta los ciclos de temperatura y la concentración de los cebadores, para asegurar que tanto el virus como el SDSI se amplificaran de manera fiable y consistente en una amplia gama de condiciones y tipos de muestras.
Este nivel de detalle garantiza que el sistema de trazabilidad no solo funciona, sino que es robusto y fiable para su uso a gran escala.

Tabla Comparativa: Secuenciación con y sin Trazadores Sintéticos
| Característica | Secuenciación Tradicional | Secuenciación con SDSI |
|---|---|---|
| Detección de Contaminación Cruzada | Indirecta y difícil. Se basa en controles negativos y patrones sospechosos. | Directa e inequívoca. La presencia de un SDSI incorrecto confirma la contaminación. |
| Cuantificación del Error | Prácticamente imposible. No se puede saber qué porcentaje de la señal es contaminante. | Posible y precisa. La proporción de lecturas del SDSI contaminante indica la magnitud del problema. |
| Confianza en los Resultados | Moderada a baja, especialmente en resultados de bajo nivel o inesperados. | Muy alta. Los resultados limpios de SDSI contaminantes están validados internamente. |
| Toma de Decisiones Clínicas/Epidemiológicas | Basada en datos con un nivel de incertidumbre inherente. | Basada en datos de alta fiabilidad, reduciendo el riesgo de conclusiones erróneas. |
Aplicación en el Mundo Real: Rastreo de un Brote Nosocomial
La utilidad de esta tecnología no es teórica. Se ha aplicado en situaciones críticas, como la investigación de un presunto brote nosocomial, es decir, una transmisión de una enfermedad dentro de un hospital. En estos escenarios, es vital determinar si varios pacientes se contagiaron a partir de una fuente común dentro del centro (lo que indicaría un fallo en los protocolos de control de infecciones) o si cada uno se infectó de forma independiente fuera del hospital.
La secuenciación genómica del virus puede responder a esta pregunta. Si los virus de diferentes pacientes son genéticamente idénticos o muy similares, sugiere una cadena de transmisión. Pero, ¿y si esa similitud es un espejismo creado por la contaminación cruzada en el laboratorio? Aquí es donde los SDSI son cruciales. Al asignar un SDSI único a cada paciente, los investigadores pueden secuenciar las muestras con la certeza de que si encuentran genomas virales idénticos, es porque realmente lo son en los pacientes, y no porque las muestras se mezclaron en el laboratorio. Esto proporciona a los responsables de salud pública la información fiable que necesitan para actuar, proteger a otros pacientes y detener la propagación de la enfermedad.
Preguntas Frecuentes (FAQ)
¿Qué es exactamente la contaminación cruzada en un laboratorio?
Es la transferencia no intencionada de material genético (ADN o ARN) de una muestra a otra. Puede ocurrir a través de microgotas en el aire (aerosoles), equipo mal limpiado, o errores humanos durante la manipulación de las muestras. Dado que técnicas como la PCR amplifican exponencialmente cualquier material genético presente, incluso una contaminación minúscula puede generar una señal fuerte y llevar a un resultado falso positivo o a una identificación incorrecta.
¿Estos "códigos de barras" de ADN sintético (SDSI) no alteran el resultado del virus que se está estudiando?
No. Han sido diseñados específicamente para no interferir. Se utilizan en concentraciones muy bajas y sus secuencias son únicas y no tienen homología con el genoma del virus ni con el del huésped (humano). Los cebadores que los amplifican son específicos para ellos, por lo que el proceso de amplificación del SDSI ocurre en paralelo al del virus, pero sin competir ni interactuar con él. Es como tener dos conversaciones separadas en la misma habitación, cada una con su propio idioma.
¿Es este método muy costoso o difícil de implementar?
Inicialmente, requiere una inversión en el diseño y síntesis de los SDSI y sus cebadores. Sin embargo, una vez implementado en un flujo de trabajo de laboratorio, el coste por muestra es relativamente bajo. Los beneficios en términos de calidad de los datos, ahorro de tiempo en la repetición de experimentos fallidos y la prevención de decisiones erróneas basadas en datos falsos, superan con creces el coste adicional. La implementación requiere una planificación cuidadosa, pero los protocolos son claros y transferibles.
¿Por qué no se usaba algo así desde siempre?
La idea de usar 'spike-ins' no es nueva, pero el desarrollo de sistemas tan sofisticados y bien validados como los SDSI es relativamente reciente. Ha sido impulsado por el auge de la secuenciación de alto rendimiento (Next-Generation Sequencing), donde se procesan miles de muestras simultáneamente, aumentando exponencialmente el riesgo y las consecuencias de la contaminación. La capacidad de sintetizar ADN a medida de forma barata y las herramientas bioinformáticas para diseñar secuencias únicas también han sido factores clave para hacer esta tecnología accesible y práctica.
Si quieres conocer otros artículos parecidos a Contaminación en Laboratorio: El Guardián Invisible puedes visitar la categoría Ecología.
