14/07/2014
En el vasto universo de la química analítica, existen técnicas que nos permiten "ver" lo invisible, cuantificando sustancias con una precisión asombrosa. Una de estas poderosas herramientas es la potenciometría, un método electroquímico que, en lugar de alterar la muestra, simplemente la "escucha". Mide la diferencia de potencial eléctrico en una solución para determinar la concentración de un componente específico. Es una técnica elegante, precisa y, fundamentalmente, no destructiva, lo que la convierte en una aliada indispensable en campos tan diversos como el monitoreo ambiental, el diagnóstico clínico y la investigación fisicoquímica.
Imagina poder medir la cantidad de flúor en el agua potable o los niveles de potasio en la sangre de un paciente sin consumir ni alterar la muestra. Eso es precisamente lo que la potenciometría nos permite hacer. Se basa en la relación directa que existe entre el potencial eléctrico de una celda electroquímica y la actividad (una medida efectiva de la concentración) de los iones disueltos. Acompáñanos en este recorrido para desentrañar los secretos de esta fascinante técnica.
- ¿Qué es la Potenciometría Exactamente?
- Los Pilares de la Medición: El Montaje Potenciométrico
- El Corazón de la Técnica: Fundamentos y Ecuaciones
- Los Sensores Químicos: Tipos de Electrodos
- Aplicaciones Prácticas de la Potenciometría: Más Allá del Laboratorio
- Preguntas Frecuentes (FAQ) sobre Potenciometría
¿Qué es la Potenciometría Exactamente?
La potenciometría es una técnica analítica que mide la diferencia de potencial (voltaje) entre dos electrodos sumergidos en una solución. El valor de este potencial está directamente relacionado con la concentración de una especie iónica de interés, conocida como analito. El instrumento clave en este proceso es el potenciómetro, que en esencia es un voltímetro de muy alta impedancia interna, diseñado para medir el voltaje sin permitir que fluya una corriente eléctrica significativa a través de la solución. Este último punto es crucial, ya que evita que ocurran reacciones químicas que podrían cambiar la composición de la muestra que se está analizando.
Los Pilares de la Medición: El Montaje Potenciométrico
Para llevar a cabo un análisis potenciométrico, se requiere un montaje específico que funciona como una celda electroquímica. Esta celda se compone de varios elementos esenciales, cada uno con una función vital:
- Electrodo Indicador (o de Trabajo): Es la estrella del sistema. Se trata de una semicelda cuyo potencial eléctrico es sensible y responde selectivamente a la concentración del analito en la solución. Su voltaje varía a medida que cambia la concentración de la especie que nos interesa medir.
- Electrodo de Referencia: Es el punto de anclaje, la referencia estable. Esta semicelda está diseñada para mantener un potencial constante y conocido, sin importar la composición de la muestra en la que se sumerge. Permite tener una base fija contra la cual medir el potencial variable del electrodo indicador.
- Puente Salino: Conecta las dos semiceldas (la del electrodo indicador y la del de referencia), permitiendo el flujo de iones entre ellas para mantener la neutralidad eléctrica y completar el circuito, pero evitando que las soluciones se mezclen.
- Potenciómetro (Voltímetro de alta impedancia): El cerebro del montaje. Mide la diferencia de potencial total de la celda, que es la diferencia entre el potencial del electrodo indicador y el del electrodo de referencia.
Tabla Comparativa de Componentes
| Componente | Función Principal | Característica Clave |
|---|---|---|
| Electrodo Indicador | Detectar el analito | Su potencial es variable y depende de la concentración del analito. |
| Electrodo de Referencia | Proporcionar una base estable de medición | Su potencial es constante e independiente de la muestra. |
| Potenciómetro | Medir la diferencia de potencial | Debe tener una alta impedancia para no drenar corriente. |
El Corazón de la Técnica: Fundamentos y Ecuaciones
El voltaje medido por el potenciómetro, conocido como potencial de celda (E_celda), es la suma de los potenciales de cada componente. Por convención, se expresa como:
E_celda = E_indicador – E_referencia + E_j
Donde E_j es el potencial de unión líquida, una pequeña diferencia de potencial que se genera en la interfaz del puente salino y que se intenta minimizar en la práctica. Dado que E_referencia es constante y E_j es idealmente insignificante, cualquier cambio en E_celda se debe directamente a un cambio en E_indicador, que a su vez es causado por una variación en la concentración del analito.
La Ecuación de Nernst: Traduciendo Voltaje a Concentración
La relación cuantitativa entre el potencial del electrodo indicador y la concentración del analito viene dada por la famosa ecuación de Nernst. Para una reacción general de un catión metálico Mn+ que se reduce a su forma metálica M, la ecuación se simplifica a:
E_indicador = Eº – (RT/nF) ln (1/aMn+)
Donde:
- Eº: Es el potencial estándar de reducción del par redox.
- R: Es la constante de los gases ideales.
- T: Es la temperatura absoluta (en Kelvin).
- n: Es el número de electrones transferidos en la reacción.
- F: Es la constante de Faraday.
- aMn+: Es la actividad del ion de interés. En soluciones diluidas, la actividad es muy similar a la concentración molar.
Esta ecuación es la clave de todo. Al medir E_celda, podemos calcular E_indicador y, a partir de ahí, despejar la actividad (o concentración) del analito que buscamos. Es la matemática que convierte un simple voltaje en información química valiosa.

Los Sensores Químicos: Tipos de Electrodos
El electrodo indicador es la pieza más especializada del sistema, ya que su diseño determina a qué ion será sensible la medición. Existen varios tipos, cada uno adaptado para diferentes analitos.
Electrodos de Primera Especie
Son los más simples. Consisten en un metal puro sumergido en una solución que contiene sus propios iones (por ejemplo, una barra de plata en una solución de nitrato de plata). El potencial de este electrodo responde directamente a la concentración de los cationes del metal (Ag+ en el ejemplo). Metales como la plata, el cobre, el zinc y el mercurio se utilizan comúnmente para este propósito.
Electrodos de Segunda Especie
Estos electrodos también son metálicos, pero están recubiertos con una de sus sales poco solubles. Su potencial no responde al catión del metal, sino al anión de la sal. Los ejemplos más comunes son el electrodo de plata-cloruro de plata (Ag/AgCl) y el electrodo de calomelanos (Hg/Hg2Cl2). Son tan estables que a menudo se utilizan como electrodos de referencia.
Electrodos Selectivos de Iones (ISE)
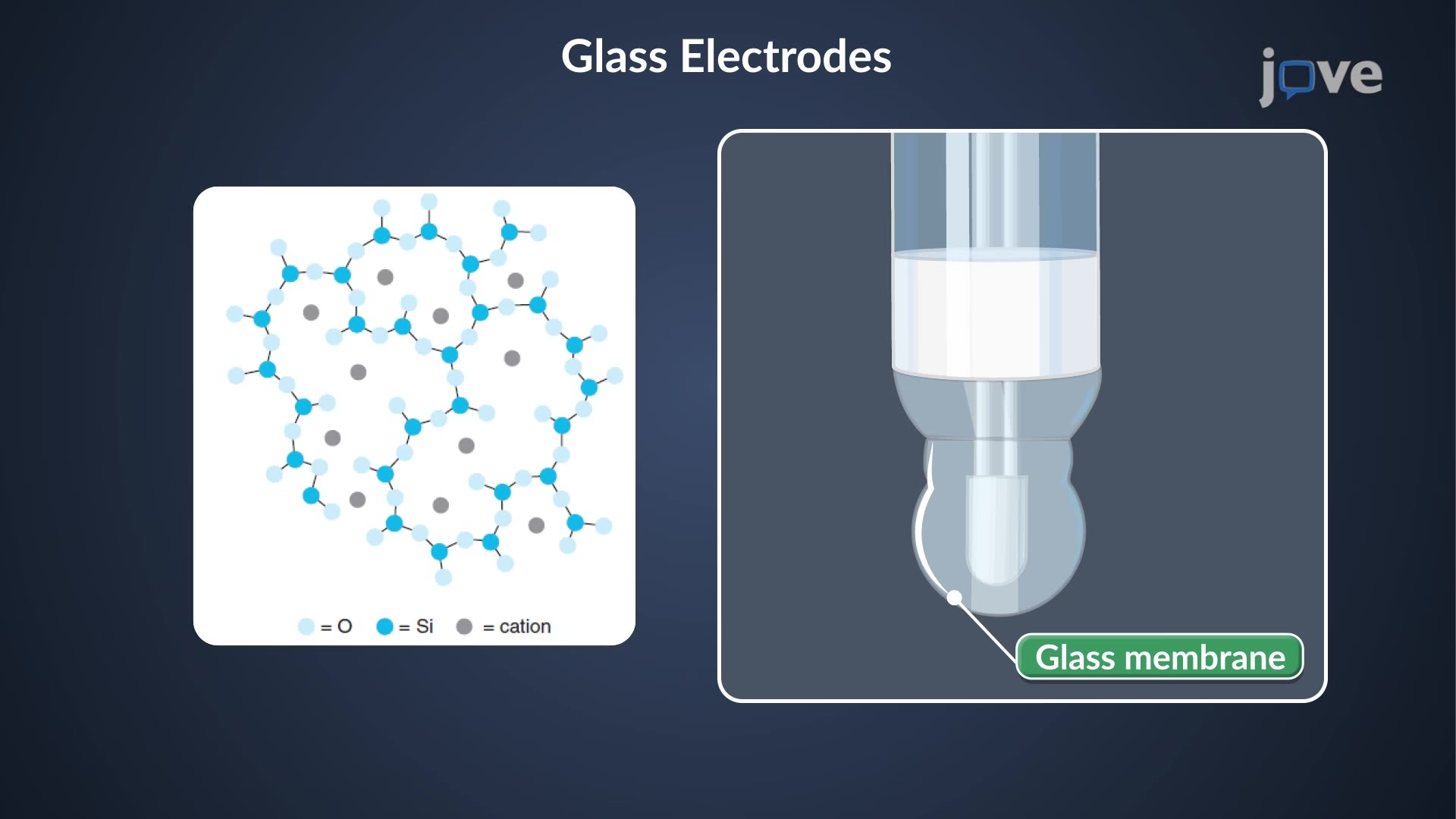
Estos son los electrodos más avanzados y versátiles. Cuentan con una membrana especial que es permeable selectivamente a un único tipo de ion. La interacción del ion con la membrana genera un potencial que es proporcional a la concentración de dicho ion en la solución, ignorando en gran medida la presencia de otros iones. El ejemplo más conocido es el electrodo de vidrio, utilizado universalmente para medir el pH (la concentración de iones H+), pero existen ISEs para una gran variedad de iones como Na+, K+, Ca2+, F-, y NO3-.

Aplicaciones Prácticas de la Potenciometría: Más Allá del Laboratorio
La versatilidad, rapidez y bajo costo de la potenciometría la han convertido en una técnica indispensable en múltiples sectores.
Vigilancia Ambiental
En ecología y ciencias ambientales, es crucial monitorear la calidad del agua y del suelo. La potenciometría se utiliza para la determinación rápida de contaminantes iónicos en ríos, lagos y aguas residuales. Se pueden medir concentraciones de iones tóxicos como el cianuro (CN-), o nutrientes en exceso como el nitrato (NO3-) y el amoníaco (NH3), que pueden causar eutrofización en cuerpos de agua.
Diagnóstico en Química Clínica
Los electrodos selectivos de iones son fundamentales en la medicina moderna. Los analizadores de electrolitos en sangre, presentes en cualquier hospital, utilizan ISEs para medir en segundos los niveles de iones vitales como K+, Na+, Cl- y Ca2+. Un desequilibrio en estos iones puede indicar problemas graves de salud. Incluso se han desarrollado microelectrodos tan pequeños que pueden insertarse en células individuales para estudiar procesos biológicos a nivel iónico.
Titulaciones Potenciométricas
Una de las aplicaciones más precisas es el seguimiento de una titulación. En lugar de usar un indicador de color visual, se sumerge un electrodo indicador en la solución y se mide el potencial de la celda a medida que se añade el titulante. Al graficar el potencial (E_celda) contra el volumen de titulante añadido, se obtiene una curva con un cambio brusco en el punto de equivalencia. Este método es mucho más objetivo y preciso que el ojo humano y puede automatizarse fácilmente.
Preguntas Frecuentes (FAQ) sobre Potenciometría
- ¿Cuál es la principal diferencia entre potenciometría y voltamperometría?
- La principal diferencia radica en lo que se mide y en las condiciones. La potenciometría mide el potencial (voltaje) en condiciones de corriente casi nula (equilibrio). En cambio, la voltamperometría aplica un potencial variable a la celda y mide la corriente eléctrica resultante, estudiando procesos dinámicos de transferencia de electrones.
- ¿Por qué el voltímetro debe tener una alta impedancia?
- Para ser una técnica no destructiva, es fundamental que la medición no altere la muestra. Un voltímetro de alta impedancia (o alta resistencia interna) evita que fluya una corriente eléctrica significativa entre los electrodos. Si fluyera corriente, se producirían reacciones de oxidación y reducción que consumirían el analito, cambiando su concentración y falseando la medida.
- ¿Se puede medir la concentración de moléculas neutras con potenciometría?
- Directamente, no. La potenciometría se basa en la respuesta de un electrodo a especies cargadas (iones). Sin embargo, existen métodos indirectos. Por ejemplo, algunos electrodos selectivos para gases (como el de amoníaco) utilizan una membrana permeable al gas que, al entrar en una solución interna, reacciona para formar un ion (NH4+) que sí es detectado potenciométricamente.
Si quieres conocer otros artículos parecidos a Potenciometría: El Análisis Electroquímico Esencial puedes visitar la categoría Ecología.
