03/11/2001
La Reacción en Cadena de la Polimerasa, comúnmente conocida como PCR, es una de las técnicas más revolucionarias y fundamentales en la biología molecular. Permite amplificar exponencialmente un fragmento específico de ADN, generando millones de copias a partir de una muestra mínima. Sin embargo, a pesar de su poder, la PCR es un proceso delicado y sensible a una multitud de variables. Un pequeño error en la configuración o en las condiciones del ciclo puede llevar a resultados frustrantes: desde la ausencia total de producto hasta la aparición de bandas inespecíficas que enturbian el análisis. La clave para el éxito no reside en seguir una receta única, sino en comprender la función de cada componente y saber cómo ajustar las condiciones para lograr una optimización precisa. Esta guía exhaustiva desglosa cada aspecto del proceso de PCR, desde los reactivos esenciales hasta las estrategias de solución de problemas, para ayudarte a obtener resultados nítidos y reproducibles en cada experimento.
Componentes Esenciales de la Reacción de PCR
El éxito de una PCR comienza con la correcta preparación de la mezcla de reacción. Cada componente tiene un rol crítico y su concentración debe ser la adecuada para garantizar la especificidad y eficiencia de la amplificación.
1. ADN Polimerasa Termoestable
Es la enzima estrella de la reacción. Su función es sintetizar nuevas hebras de ADN utilizando el molde y los cebadores. Debe ser termoestable para soportar las altas temperaturas del paso de desnaturalización (típicamente 94-98 °C) sin perder su actividad. La Taq polimerasa es la más común, conocida por su alta procesividad, aunque carece de actividad de corrección de pruebas, lo que puede introducir errores. Para aplicaciones que requieren alta fidelidad, se prefieren enzimas como la Pfu polimerasa, que sí poseen esta capacidad de corrección.
2. Cebadores (Primers)
Son secuencias cortas de ADN de cadena simple (oligonucleótidos) que se unen a regiones específicas del ADN molde, flanqueando el segmento que se desea amplificar. El diseño de los cebadores es quizás el factor más crítico para la especificidad de la PCR. Un mal diseño puede resultar en la amplificación de secuencias incorrectas, la formación de dímeros de cebador o la ausencia total de producto.
3. Desoxinucleótidos Trifosfato (dNTPs)
Son los ladrillos con los que la polimerasa construye las nuevas hebras de ADN. La mezcla de dNTPs debe contener concentraciones equimolares de dATP, dCTP, dGTP y dTTP. La concentración final típica es de 200 µM (50 µM de cada uno). Concentraciones más bajas pueden aumentar la fidelidad, mientras que concentraciones excesivas pueden inhibir la reacción.
4. Buffer de Reacción y Magnesio (Mg²⁺)
El buffer mantiene el pH óptimo para la actividad de la polimerasa. Sin embargo, el componente más influyente dentro de esta solución es el ion magnesio (Mg²⁺). El magnesio actúa como un cofactor esencial para la ADN polimerasa. Su concentración afecta drásticamente la rigurosidad (stringency) de la reacción:
- Poco Mg²⁺: La polimerasa tendrá baja actividad, resultando en poco o ningún producto de PCR.
- Exceso de Mg²⁺: Estabiliza el dúplex de ADN y la unión inespecífica de los cebadores, lo que disminuye la especificidad y puede generar múltiples bandas no deseadas.
La titulación de la concentración de MgCl₂ (generalmente entre 1.5 mM y 4.0 mM) es uno de los primeros pasos en la optimización de una nueva PCR.

5. ADN Molde (Template)
La calidad y cantidad del ADN molde son cruciales. El ADN debe estar libre de inhibidores de la PCR, como proteínas, solventes orgánicos o detergentes remanentes de la extracción. La pureza se estima midiendo la relación de absorbancia OD₂₆₀/₂₈₀, que idealmente debe estar entre 1.8 y 2.0. La cantidad óptima de molde suele estar entre 10⁴ y 10⁷ copias de la secuencia diana por reacción.
Diseño de Cebadores: La Piedra Angular de la Especificidad
Un diseño cuidadoso de los cebadores previene la mayoría de los problemas comunes en la PCR.
- Temperatura de Fusión (Tm): Es la temperatura a la cual la mitad de los cebadores están unidos a su secuencia complementaria. La Tm óptima se sitúa entre 52-58 °C. Ambos cebadores de un par deben tener una Tm similar (una diferencia no mayor a 5 °C) para asegurar que ambos se unan eficientemente a la misma temperatura de anillamiento (Ta).
- Evitar Estructuras Secundarias: Los cebadores no deben tener secuencias internas complementarias que puedan formar horquillas (hairpin loops). Tampoco deben ser complementarios entre sí, especialmente en sus extremos 3', para evitar la formación de dímeros de cebador (primer-dimers), que compiten con la amplificación del producto deseado.
- Pinza GC (GC Clamp): Es recomendable que el extremo 3' de los cebadores termine en una G o una C. Los tres puentes de hidrógeno de los pares G-C proporcionan una unión más estable al molde, evitando el "deshilachado" del extremo y mejorando la eficiencia de la extensión por parte de la polimerasa.
- Longitud y Contenido GC: Generalmente, los cebadores tienen entre 18 y 25 nucleótidos de longitud con un contenido de GC entre el 40% y el 60%.
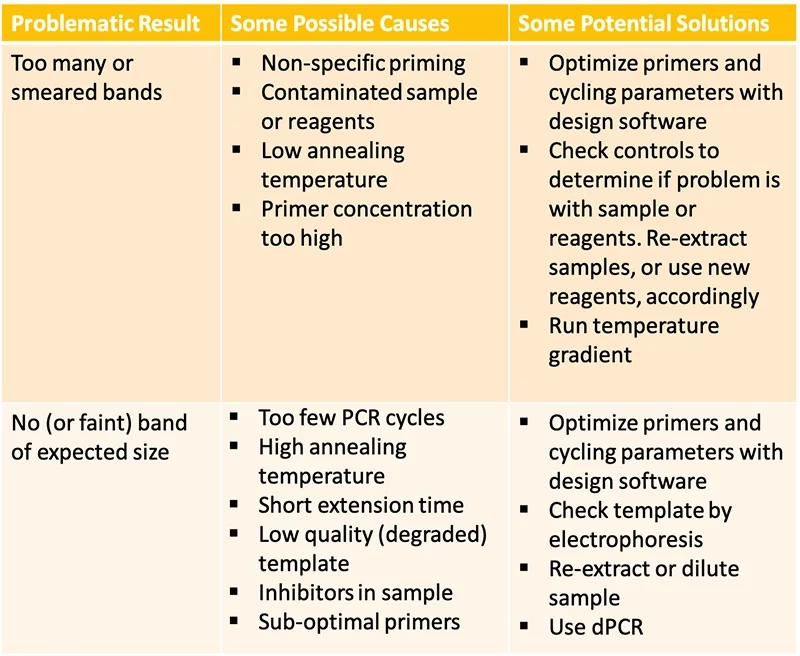
Solución de Problemas Comunes (Troubleshooting)
Incluso con una preparación cuidadosa, los resultados pueden no ser los esperados. Analizar el patrón de bandas en un gel de agarosa es el primer paso para diagnosticar el problema.
Problema 1: Ausencia de Producto
Si no se observa ninguna banda en el gel, las causas pueden ser múltiples. Puede deberse a condiciones demasiado estrictas (temperatura de anillamiento muy alta), una concentración de Mg²⁺ insuficiente, la presencia de inhibidores en la muestra de ADN, o simplemente un error en la adición de algún reactivo. Para solucionarlo, se puede probar a disminuir la temperatura de anillamiento, titular la concentración de Mg²⁺, diluir el ADN molde para reducir la concentración de inhibidores, o preparar una nueva mezcla de reacción asegurándose de que todos los componentes estén presentes.
Problema 2: Productos Inespecíficos o "Smear"
La aparición de múltiples bandas de tamaños inesperados o un barrido continuo (smear) indica que las condiciones de la reacción son poco estrictas. Esto permite que los cebadores se unan a sitios no deseados del genoma. Las soluciones incluyen:
- Aumentar la temperatura de anillamiento.
- Disminuir la concentración de MgCl₂.
- Reducir la concentración de los cebadores.
- Disminuir el número de ciclos de la PCR.
- Utilizar protocolos como la PCR "Hot Start" o "Touchdown".
Problema 3: Dímeros de Cebador
Se manifiestan como una banda muy intensa y de bajo peso molecular (<100 pb) en el gel. Ocurren cuando los cebadores se anillan entre sí y son extendidos por la polimerasa, consumiendo reactivos y compitiendo con la amplificación del producto de interés. La mejor solución es rediseñar los cebadores para evitar la complementariedad en sus extremos 3'. Alternativamente, se puede intentar reducir la concentración de cebadores o utilizar una PCR "Hot Start" para minimizar su interacción a bajas temperaturas.

Técnicas Avanzadas y Aditivos para PCR Difíciles
Cuando se trabaja con moldes complejos, como aquellos con alto contenido de GC, pueden ser necesarios aditivos o protocolos especiales para lograr la amplificación.
Aditivos Comunes
- DMSO (Dimetilsulfóxido) y Formamida: Ayudan a desestabilizar las estructuras secundarias en moldes ricos en GC, facilitando la desnaturalización y el anillamiento de los cebadores.
- Betaína: Reduce la dependencia de la temperatura de fusión de la composición de nucleótidos, igualando la estabilidad de los pares AT y GC y mejorando la amplificación de secuencias difíciles.
- BSA (Albúmina de Suero Bovino): Se añade cuando se sospecha la presencia de inhibidores en la muestra de ADN (ej. extractos de suelo, sangre), ya que puede secuestrarlos y prevenir su interferencia con la polimerasa.
Protocolos de PCR Modificados
A continuación, se presenta una tabla comparativa de algunos protocolos avanzados de PCR:
| Protocolo | Principio de Funcionamiento | Principal Ventaja | Ideal Para |
|---|---|---|---|
| Hot Start PCR | La ADN polimerasa se mantiene inactiva hasta que la reacción alcanza la temperatura de desnaturalización inicial. | Aumenta drásticamente la especificidad al prevenir la unión inespecífica de cebadores y la formación de dímeros a bajas temperaturas. | Casi todas las aplicaciones, especialmente con bajo número de copias del molde o cebadores propensos a formar dímeros. |
| Touchdown PCR (TD-PCR) | Se inicia con una temperatura de anillamiento muy alta (por encima de la Tm teórica) y se disminuye gradualmente en cada ciclo o cada par de ciclos. | Favorece la amplificación del producto perfectamente complementario, aumentando la especificidad sin necesidad de una optimización exhaustiva de la temperatura. | Amplificar un gen sin conocer la temperatura de anillamiento óptima o para evitar productos inespecíficos. |
| Nested PCR | Se realizan dos rondas de PCR consecutivas. La segunda ronda utiliza un par de cebadores que anillan dentro del producto generado en la primera ronda. | Ofrece una especificidad y sensibilidad extremadamente altas. | Detectar secuencias presentes en muy baja cantidad (ej. patógenos) o para amplificar un gen específico de una familia de genes muy similares. |
Preguntas Frecuentes (FAQ)
¿Por qué mi PCR no produce ningún resultado?
Las causas más comunes son: un componente esencial olvidado en la mezcla, inhibidores en el ADN molde, temperatura de anillamiento demasiado alta, concentración de Mg²⁺ inadecuada o cebadores mal diseñados. Revisa tu protocolo, prepara reactivos frescos y considera realizar una titulación de Mg²⁺ y un gradiente de temperatura de anillamiento.
¿Qué son los dímeros de cebador y cómo puedo evitarlos?
Son artefactos de la PCR formados por la unión de los cebadores entre sí. La mejor prevención es un buen diseño que evite la complementariedad entre ellos, especialmente en los extremos 3'. Utilizar una PCR "Hot Start" también es muy efectivo para minimizar su formación.
Mi gel muestra un "barrido" en lugar de una banda nítida, ¿qué significa?
Un "smear" o barrido suele indicar condiciones de reacción poco estrictas, lo que provoca una amplificación inespecífica en múltiples sitios del genoma. También puede ser causado por una cantidad excesiva de ADN molde o demasiados ciclos de PCR. Intenta aumentar la temperatura de anillamiento o disminuir la concentración de Mg²⁺.
¿Cuándo debería usar aditivos como el DMSO o la betaína?
Estos aditivos son particularmente útiles cuando se intenta amplificar secuencias de ADN con un alto contenido de Guanina y Citosina (GC > 60%). Estas regiones son difíciles de desnaturalizar y tienden a formar estructuras secundarias que bloquean el avance de la polimerasa. El DMSO y la betaína ayudan a relajar estas estructuras, facilitando la amplificación.
Si quieres conocer otros artículos parecidos a Guía Definitiva para una Reacción en Cadena de la Polimerasa (PCR) Exitosa puedes visitar la categoría Ecología.