30/07/2010
En nuestra búsqueda de un planeta más sostenible, a menudo nos centramos en soluciones a gran escala: paneles solares, turbinas eólicas, políticas de reciclaje. Sin embargo, muchas de las respuestas a nuestros mayores desafíos ambientales se encuentran en lo invisible, en el comportamiento de las partículas que componen el mundo que nos rodea. Uno de estos conceptos fundamentales, extraído directamente de la termodinámica, es la energía interna de un gas. Aunque pueda sonar como un tema exclusivo para laboratorios de física, comprender cómo los gases almacenan y liberan energía es crucial para optimizar la eficiencia energética, modelar el cambio climático y diseñar tecnologías más limpias. Este viaje al corazón de la materia nos revelará por qué el movimiento de átomos individuales tiene un impacto directo en la salud de nuestro planeta.
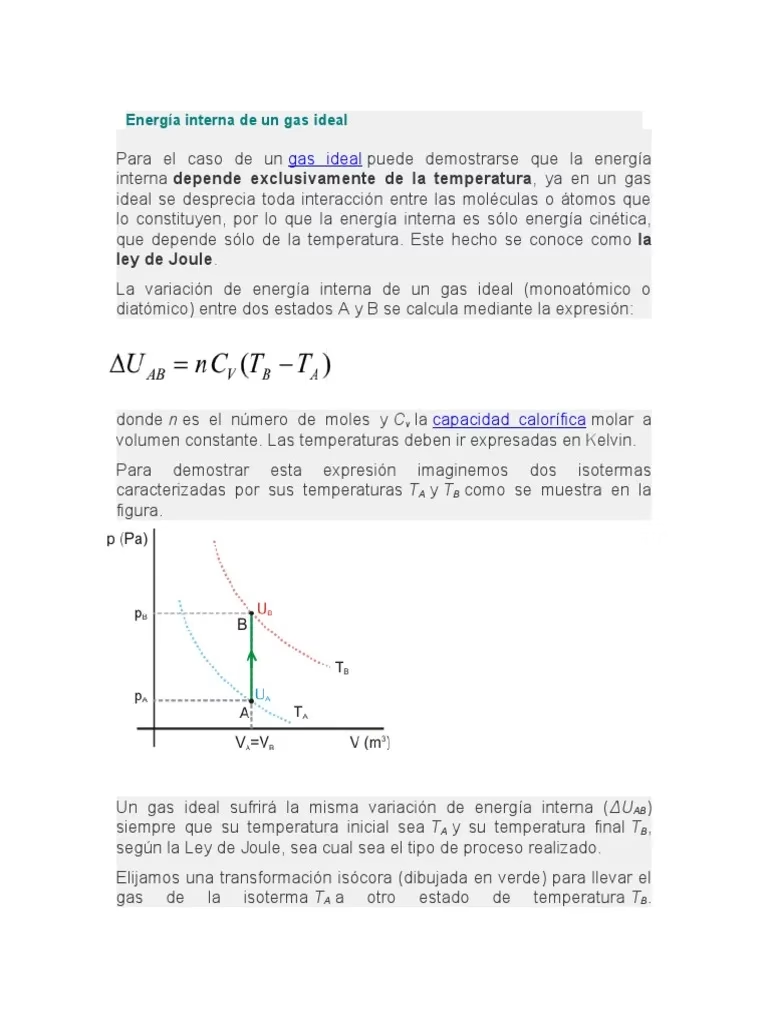
¿Qué es la Energía Interna y por qué nos importa?
La energía interna de un sistema, como una masa de gas, es la suma de todas las energías microscópicas de sus partículas constituyentes. Esto incluye la energía cinética (debido a su movimiento) y la energía potencial (debido a las fuerzas entre ellas). Para un 'gas ideal', un modelo simplificado que nos ayuda a entender los principios básicos, la situación es más sencilla: asumimos que las partículas no interactúan entre sí, por lo que su energía interna es puramente la suma de sus energías cinéticas. ¿Y por qué es esto relevante para el ecologismo? Porque la energía es el motor de casi todos los procesos industriales y naturales. Entender cómo un gas la almacena a nivel molecular nos permite:
- Diseñar motores de combustión más eficientes que quemen menos combustible y emitan menos CO2.
- Optimizar los ciclos de refrigeración y calefacción, reduciendo el consumo eléctrico.
- Crear modelos climáticos más precisos al comprender cómo la atmósfera (una mezcla de gases) absorbe y retiene el calor del sol.
En esencia, la gestión de la energía a gran escala comienza con la comprensión de la energía a escala atómica.
El Modelo del Gas Ideal: Simplificando la Complejidad
Para analizar la energía interna, los científicos utilizan el modelo del 'gas ideal'. Este es un gas teórico compuesto por partículas que se mueven al azar y que no interactúan entre sí. Aunque ningún gas es perfectamente 'ideal', este modelo es una aproximación excelente para muchos gases (como el nitrógeno o el oxígeno de nuestro aire) en condiciones de baja presión y alta temperatura. La principal característica de un gas ideal es que su energía interna depende exclusivamente de su temperatura. A mayor temperatura, las partículas se mueven más rápido, y por lo tanto, la energía interna total del sistema aumenta.
El Caso Base: Gas Ideal Monoatómico
Imaginemos un gas compuesto por átomos individuales, como el Helio (He), el Neón (Ne) o el Argón (Ar). Estos son gases monoatómicos. Cada átomo puede moverse en tres dimensiones espaciales: arriba-abajo (eje Y), izquierda-derecha (eje X), y adelante-atrás (eje Z). A estos tres tipos de movimiento se les llama 'grados de libertad de traslación'. Para un gas ideal monoatómico, la energía interna (E_int) se calcula como la suma de la energía cinética de todos estos movimientos y viene dada por la fórmula:
E_int = (3/2) nRT
Donde 'n' es el número de moles del gas, 'R' es la constante de los gases ideales y 'T' es la temperatura absoluta en Kelvin. El factor '3/2' proviene directamente de esos tres grados de libertad.
Moléculas Diatómicas: El Aire que Respiramos
Aquí es donde la cosa se pone más interesante y directamente aplicable a nuestro entorno. La mayor parte del aire que respiramos está compuesta por nitrógeno (N₂) y oxígeno (O₂), que son moléculas diatómicas (formadas por dos átomos unidos). Estas moléculas no solo pueden trasladarse en las tres dimensiones como los átomos individuales, sino que también pueden girar.
Piense en una molécula diatómica como una pequeña mancuerna. Puede girar sobre dos ejes perpendiculares a la línea que une los dos átomos. La rotación a lo largo del eje que une los átomos es insignificante a nivel cuántico. Por lo tanto, una molécula diatómica tiene los 3 grados de libertad de traslación más 2 grados de libertad de energía cinética rotacional. Esto suma un total de 5 grados de libertad.
Debido a estas formas adicionales de almacenar energía, la energía interna de un gas ideal diatómico es mayor que la de un gas monoatómico a la misma temperatura. Su fórmula es:
E_int = (5/2) nRT
Este '5/2' refleja los cinco grados de libertad activos a temperaturas intermedias. Es importante notar que esto es una aproximación. A temperaturas muy bajas, la energía rotacional se 'congela' y la molécula se comporta casi como una monoatómica. A temperaturas extremadamente altas (como en la combustión de un motor), los átomos dentro de la molécula comienzan a vibrar, añadiendo dos grados de libertad más (uno cinético y otro potencial por la vibración), lo que complica aún más el cálculo. Esta dependencia de la temperatura es clave para entender procesos de alta energía y su eficiencia.
Tabla Comparativa: Gases Ideales Monoatómicos vs. Diatómicos
| Característica | Gas Monoatómico | Gas Diatómico (a temp. intermedia) |
|---|---|---|
| Ejemplos | Helio (He), Argón (Ar) | Oxígeno (O₂), Nitrógeno (N₂) |
| Grados de Libertad | 3 (solo traslación) | 5 (3 de traslación + 2 de rotación) |
| Fórmula de Energía Interna | E_int = (3/2) nRT | E_int = (5/2) nRT |
| Capacidad de Almacenar Energía | Menor | Mayor (a la misma temperatura) |
Más Allá del Ideal: Gases Reales y su Impacto Ambiental
El mundo real es más complejo que el modelo ideal. Los gases reales, especialmente a alta presión y baja temperatura, se desvían del comportamiento ideal. Sus moléculas sí ocupan un volumen y sí existen fuerzas de atracción y repulsión entre ellas. Esto significa que la energía interna de un gas real no solo depende de la temperatura, sino también del volumen y la presión.
Esta distinción es vital para aplicaciones ambientales críticas:
- Refrigerantes: Los gases utilizados en aires acondicionados y refrigeradores (como los HFC) experimentan cambios de fase de gas a líquido. Su comportamiento como gases reales es lo que permite el ciclo de enfriamiento. Entender su termodinámica es clave para encontrar sustitutos con menor potencial de calentamiento global.
- Captura y Almacenamiento de Carbono (CAC): Una estrategia para mitigar el cambio climático es capturar el CO₂ de las centrales eléctricas y almacenarlo bajo tierra. Este proceso implica comprimir el CO₂ a presiones muy altas, donde se comporta como un gas muy real (o incluso un fluido supercrítico). El cálculo preciso de la energía necesaria para este proceso depende de un conocimiento profundo de su energía interna en condiciones no ideales.
- Transporte de Gas Natural: El gas natural (principalmente metano, CH₄) se transporta a menudo en forma licuada (GNL) o comprimida (GNC). Su comportamiento como gas real determina la eficiencia y seguridad de su transporte y almacenamiento.
Conclusión: La Conexión Invisible con la Sostenibilidad
Lo que comienza como una simple ecuación sobre el movimiento de átomos se convierte en una herramienta poderosa para forjar un futuro más sostenible. La energía interna de los gases es un pilar de la termodinámica que informa directamente sobre la eficiencia de nuestros sistemas energéticos. Cada mejora en la eficiencia de un motor, cada optimización en un proceso químico, cada avance en la tecnología de refrigeración, se basa en estos principios fundamentales. Al mirar el mundo a través de la lente de la energía molecular, nos damos cuenta de que la lucha por la sostenibilidad no solo se libra en los bosques y los océanos, sino también en el espacio invisible entre los átomos que componen nuestro aire. Comprenderlo es el primer paso para protegerlo.
Preguntas Frecuentes (FAQ)
¿Por qué la energía interna de un gas ideal solo depende de la temperatura?
En el modelo del gas ideal, se asume que no existen fuerzas intermoleculares. Por lo tanto, no hay energía potencial asociada a la distancia entre las partículas. La única energía que poseen es la cinética, que está directamente relacionada con su velocidad de movimiento, y la velocidad promedio de las partículas es, por definición, una medida de la temperatura del sistema.
¿El aire que respiramos se comporta como un gas ideal?
En condiciones atmosféricas normales (presión y temperatura ambiente), el aire se comporta de manera muy similar a un gas ideal. Las moléculas de nitrógeno y oxígeno están lo suficientemente separadas y se mueven lo suficientemente rápido como para que las interacciones entre ellas sean mínimas. Por eso, las leyes de los gases ideales son muy útiles para la meteorología y la ciencia atmosférica.
¿Cómo se relaciona este concepto con el efecto invernadero?
Gases de efecto invernadero como el dióxido de carbono (CO₂) o el metano (CH₄) son poliatómicos. Tienen más grados de libertad (traslacionales, rotacionales y vibracionales) que el O₂ o N₂. Esto les permite absorber radiación infrarroja (calor) emitida por la Tierra en una gama más amplia de frecuencias, excitando sus modos vibracionales y rotacionales. Al re-emitir esta energía en todas direcciones, parte de ella regresa a la superficie, calentando el planeta. Su compleja estructura molecular es la clave de su capacidad para atrapar calor.
Si quieres conocer otros artículos parecidos a Energía Interna de Gases: Una Clave Ambiental puedes visitar la categoría Ecología.
