08/05/2017
La migración celular es uno de los procesos más fascinantes y fundamentales de la vida. Es el motor que impulsa el desarrollo embrionario, permite que nuestro sistema inmune nos defienda de patógenos y es crucial para la cicatrización de heridas. Sin embargo, cuando este mecanismo se descontrola, puede tener consecuencias devastadoras, como la metástasis en el cáncer. Para comprender y combatir estas enfermedades, los científicos necesitan herramientas precisas que les permitan estudiar este proceso en el laboratorio. Aquí es donde entra en juego el ensayo de la Cámara de Boyden, una técnica estándar de oro que, a pesar de sus décadas de existencia, sigue evolucionando para ofrecer resultados cada vez más fiables.
¿Qué es y Cómo Funciona el Ensayo de la Cámara de Boyden?
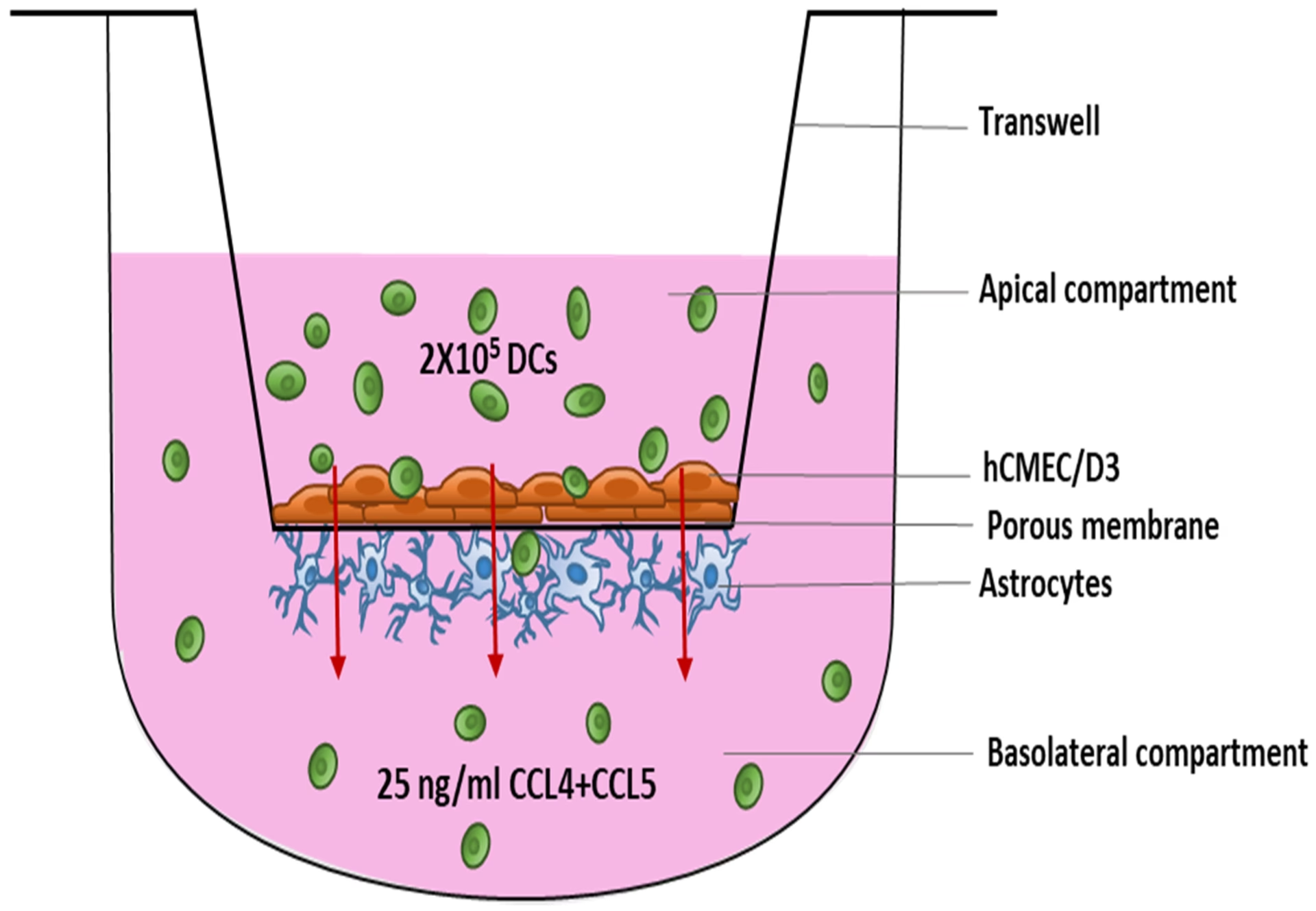
Desarrollado en 1962 por el Dr. Stephen Boyden, este ensayo, también conocido como ensayo transwell, es el método más utilizado para estudiar la migración e invasión celular in vitro. Su diseño es elegantemente simple pero increíblemente poderoso. Consiste en un inserto especial (transwell) que se coloca dentro de un pozo de una placa de cultivo celular, dividiéndolo en dos compartimentos: uno superior y otro inferior, separados por una membrana microporosa.
El procedimiento básico es el siguiente:
- Compartimento Superior: Aquí se siembran las células que se desean estudiar.
- Compartimento Inferior: Se coloca un medio que contiene un agente quimioatrayente, es decir, una sustancia que atrae a las células (como un factor de crecimiento).
- La Migración: Las células en el compartimento superior detectan el gradiente del quimioatrayente y comienzan a moverse activamente, atravesando los pequeños poros de la membrana para llegar al compartimento inferior. Este movimiento dirigido se conoce como quimiotaxis.
Tras un período de incubación determinado, el investigador cuantifica el número de células que lograron cruzar la membrana. Este número es un indicador directo de la capacidad migratoria de ese tipo celular en respuesta a un estímulo específico.
Migración vs. Invasión: Una Distinción Crucial
Aunque a menudo se usan indistintamente, los ensayos de migración e invasión miden dos habilidades celulares diferentes, y la Cámara de Boyden puede adaptarse para estudiar ambas. La diferencia clave radica en la membrana que separa los dos compartimentos.
- Ensayo de Migración: Utiliza una membrana porosa sin recubrimiento. Mide la motilidad inherente de una célula, su capacidad para moverse a través de un espacio confinado. Es relevante para procesos como la respuesta inmune, donde los leucocitos deben moverse a través de los tejidos.
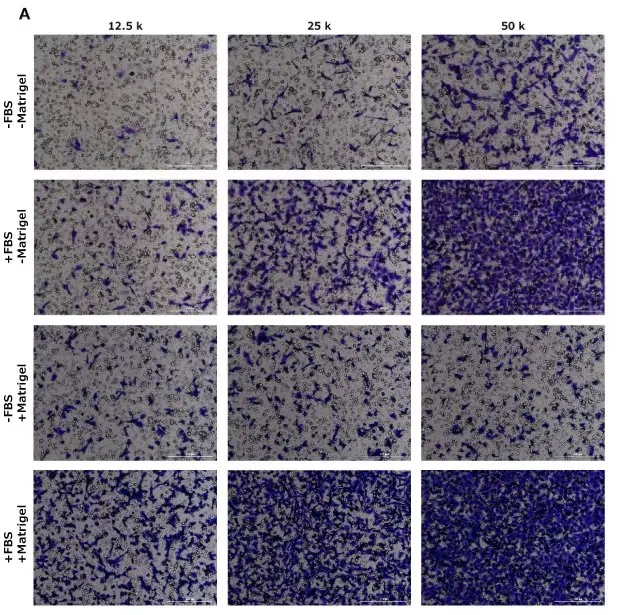
- Ensayo de Invasión: Utiliza una membrana recubierta con una capa de matriz extracelular (MEC), como Matrigel. Este gel simula la barrera física (membrana basal) que las células deben atravesar en el cuerpo. Para cruzar, las células no solo deben moverse, sino también secretar enzimas para degradar activamente esta barrera. Este ensayo es fundamental para estudiar la metástasis del cáncer, ya que las células tumorales deben invadir los tejidos circundantes para propagarse.
Tabla Comparativa: Migración vs. Invasión
| Característica | Ensayo de Migración | Ensayo de Invasión |
|---|---|---|
| Objetivo Principal | Medir la motilidad celular (quimiotaxis) | Medir la capacidad de atravesar barreras tisulares |
| Tipo de Membrana | Porosa, sin recubrimiento | Porosa, recubierta con Matrigel u otra MEC |
| Proceso Celular Medido | Movimiento activo a través de poros | Movimiento + Degradación de la matriz |
| Relevancia Biológica | Respuesta inmune, desarrollo embrionario | Metástasis del cáncer, angiogénesis |
El Talón de Aquiles del Ensayo Tradicional: ¿Qué Pasa Arriba?
El protocolo clásico del ensayo transwell con membranas transparentes tiene un paso crítico: después de la incubación, las células que no migraron y permanecieron en la superficie superior de la membrana deben ser eliminadas, generalmente frotando con un hisopo de algodón. Luego, las células en la parte inferior se tiñen y se cuentan. Aquí reside una omisión fundamental que ha afectado la precisión de innumerables estudios: se ignora por completo lo que ocurrió con la población celular inicial en el compartimento superior.
Considerar solo las células que llegaron abajo cuenta una historia incompleta. ¿Por qué? Porque el resultado final debería ser un porcentaje de migración, y para calcularlo, necesitamos saber cuántas células había en total. Durante el ensayo, especialmente en los de invasión que pueden durar hasta 72 horas, pueden ocurrir varios fenómenos en el compartimento superior:
- Adhesión diferencial: No todas las células sembradas se adhieren correctamente a la membrana.
- Viabilidad celular: Algunas células pueden morir debido a las condiciones del cultivo.
- Proliferación: ¡Este es el factor más crítico! Las células pueden dividirse durante el experimento. Si un tratamiento experimental reduce la migración pero también inhibe la proliferación, el resultado puede malinterpretarse. Podríamos pensar que el fármaco es un potente anti-migratorio, cuando en realidad simplemente había menos células en total para migrar.
No tener en cuenta estos factores puede conducir a conclusiones erróneas, sobrestimando o subestimando drásticamente la capacidad migratoria real de las células.
Mejorando la Precisión: Un Enfoque Modernizado
La conciencia de estas limitaciones ha impulsado modificaciones metodológicas para hacer el ensayo más robusto y preciso. La solución más efectiva combina técnicas de imagen avanzadas con una elección inteligente de materiales.

El enfoque mejorado propone lo siguiente:
- Utilizar membranas transparentes: A diferencia de las membranas opacas que impiden la visualización de la parte superior, las transparentes permiten analizar ambos lados.
- Emplear tinción fluorescente nuclear: En lugar de los tintes histoquímicos tradicionales que colorean todo el citoplasma, se utilizan colorantes fluorescentes que se unen específicamente al ADN, como el DAPI. Esto tiñe únicamente el núcleo de las células, creando puntos brillantes y bien definidos que son fáciles de contar, ya sea manualmente o con software de análisis de imágenes.
- Contar ambos lados de la membrana: Este es el paso clave. Se toman imágenes tanto de la superficie superior (células no migradas) como de la inferior (células migradas). Esto proporciona el número total de células viables al final del experimento.
- Superponer imágenes: Para una precisión aún mayor, se puede superponer la imagen de fluorescencia (núcleos teñidos con DAPI) con una imagen de campo claro del microscopio. Esto permite ver los poros de la membrana y asegurar que lo que se está contando es realmente una célula y no un artefacto o tinte acumulado en un poro.
Al implementar estas modificaciones, el cálculo del porcentaje de migración (% Migración = [Células en la parte inferior] / [Células en la parte superior + Células en la parte inferior] x 100) se vuelve infinitamente más preciso y fiable, eliminando los sesgos introducidos por la proliferación o la muerte celular.
Preguntas Frecuentes (FAQ)
¿Cuál es la diferencia entre quimiotaxis y haptotaxis?
La quimiotaxis es la migración celular dirigida por un gradiente de concentración de una sustancia química soluble (como un factor de crecimiento). La haptotaxis, por otro lado, es la migración dirigida por gradientes de moléculas de adhesión fijadas a una superficie, como las proteínas de la matriz extracelular. El ensayo de invasión con Matrigel involucra ambos procesos.
¿Se puede usar este ensayo para cualquier tipo de célula?
Prácticamente sí, siempre que las células sean móviles. Es ampliamente utilizado para células cancerosas, fibroblastos, células inmunes (linfocitos, macrófagos), células endoteliales y células madre. El factor clave es seleccionar el tamaño de poro de la membrana adecuado para el tamaño de la célula. Por ejemplo, poros de 8 µm son estándar para la mayoría de las células tumorales, mientras que los linfocitos, más pequeños y deformables, pueden usar poros de 3 a 5 µm.
¿Por qué es tan importante eliminar las células de la parte superior en el método tradicional?
En el método clásico que utiliza membranas transparentes y tintes como el cristal violeta, el colorante tiñe tanto las células de arriba como las de abajo. Si no se eliminaran las de arriba, al mirar la membrana desde abajo para contar, sería imposible distinguir qué células cruzaron y cuáles no, haciendo la cuantificación inviable.
¿Qué es mejor, el ensayo de herida (scratch) o la Cámara de Boyden?
Depende de la pregunta de investigación. El ensayo de herida es más simple y económico, ideal para observar la migración colectiva en 2D, como en la cicatrización. Sin embargo, carece de un gradiente quimiotáctico y es menos reproducible. La Cámara de Boyden es más compleja pero ofrece un modelo 3D, cuantifica la quimiotaxis y puede adaptarse para estudios de invasión, lo que la hace mucho más relevante para estudiar procesos como la metástasis.
En conclusión, el ensayo de la Cámara de Boyden sigue siendo una herramienta indispensable en la biología celular y la investigación biomédica. Aunque su concepto original tiene más de medio siglo, la comprensión de sus limitaciones ha llevado a refinamientos cruciales. Al adoptar un enfoque más completo que cuantifica tanto las células que migran como las que no, los científicos pueden obtener datos mucho más precisos y fiables, acelerando el descubrimiento de nuevas terapias para enfermedades donde la migración celular juega un papel protagonista.
Si quieres conocer otros artículos parecidos a Cámara de Boyden: Clave en Migración Celular puedes visitar la categoría Ecología.