24/07/2002
El azufre es uno de los elementos más fascinantes y paradójicos de nuestro planeta. Presente en la corteza terrestre, en los océanos y en la atmósfera, su ciclo y sus compuestos tienen un impacto profundo tanto en los ecosistemas naturales como en las actividades humanas. Durante décadas, el azufre fue etiquetado como un villano ambiental, el principal culpable de la lluvia ácida y un contaminante a erradicar. Sin embargo, la historia es mucho más compleja. Este mismo elemento es un pilar para la vida, un nutriente esencial para el crecimiento de las plantas y un componente clave en innumerables procesos industriales. Este artículo explora la increíble dualidad del azufre, desde su química versátil hasta su rol como contaminante, su importancia en la agricultura y los métodos que hemos desarrollado para controlar su presencia donde no es deseado.

- La Química Versátil del Azufre: Más Allá del Olor Característico
- El Azufre como Contaminante Ambiental
- La Paradoja: Deficiencia de Azufre en la Agricultura
- El Azufre como Nutriente: Fertilizantes y Manejo Agrícola
- Eliminación y Filtración de Azufre: Controlando su Presencia
- Preguntas Frecuentes (FAQ) sobre el Azufre
La Química Versátil del Azufre: Más Allá del Olor Característico
Perteneciente al grupo 16 de la tabla periódica, justo debajo del oxígeno, el azufre comparte algunas similitudes con su vecino más ligero, pero posee una química mucho más rica y variada. A diferencia del oxígeno, que forma moléculas diatómicas (O₂) y triatómicas (O₃), el azufre en su estado elemental más común forma moléculas cíclicas con ocho átomos (S₈), lo que le confiere propiedades únicas. Su capacidad para formar una amplia gama de compuestos lo convierte en un actor central en la biología y la industria.
Compuestos Clave del Azufre
- Ácido Sulfúrico (H₂SO₄): Conocido como el "rey de los productos químicos", el ácido sulfúrico es el compuesto fabricado en mayor cantidad a nivel mundial. Su producción masiva y bajo costo lo hacen indispensable en una multitud de aplicaciones, desde la fabricación de fertilizantes fosfatados, que son cruciales para la seguridad alimentaria, hasta la limpieza de metales, la producción de explosivos, detergentes, papel y celofán.
- Dióxido de Azufre (SO₂): Este gas es un subproducto inevitable de la quema de combustibles fósiles (carbón y petróleo) que contienen azufre. Durante mucho tiempo, el dióxido de azufre fue el principal precursor de la lluvia ácida, un grave problema ambiental que causó estragos en bosques y ecosistemas acuáticos en todo el mundo. También es una etapa intermedia en la producción de ácido sulfúrico.
- Sulfuro de Hidrógeno (H₂S): Famoso por su penetrante olor a "huevo podrido", el sulfuro de hidrógeno es un gas altamente tóxico. Se genera de forma natural en pantanos y procesos de descomposición, y también emana de extracciones petrolíferas. Paradójicamente, a pesar de su toxicidad, es una fuente primaria para la obtención de azufre elemental puro mediante procesos de oxidación catalítica. Su efecto anestesiante sobre el sentido del olfato lo hace particularmente peligroso, ya que las personas pueden dejar de percibirlo a concentraciones letales.
El Azufre como Contaminante Ambiental
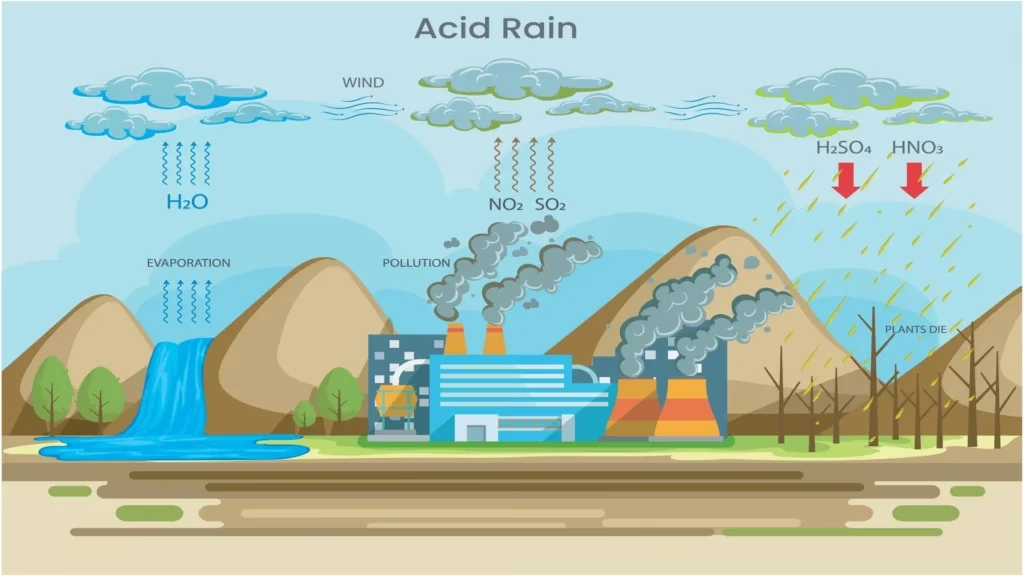
La reputación del azufre como contaminante se forjó principalmente en el siglo XX. La quema masiva de carbón y petróleo para generar energía y alimentar la industria liberó a la atmósfera cantidades ingentes de dióxido de azufre. Una vez en el aire, el SO₂ reacciona con el agua, el oxígeno y otros químicos para formar ácido sulfúrico y sulfatos, que luego caen a la tierra en forma de lluvia, nieve o niebla ácida. Este fenómeno tuvo consecuencias devastadoras: acidificó lagos y ríos hasta el punto de hacerlos inhabitables para los peces, dañó severamente los bosques al lixiviar nutrientes del suelo y erosionó edificios y monumentos históricos. La creciente preocupación pública y científica llevó a la creación de legislaciones ambientales estrictas en muchos países para reducir drásticamente las emisiones de azufre, obligando a las industrias a instalar filtros o a utilizar combustibles con bajo contenido de este elemento.
La Paradoja: Deficiencia de Azufre en la Agricultura
Las exitosas políticas para reducir la contaminación por azufre tuvieron una consecuencia inesperada y sorprendente: crearon un desequilibrio en el ciclo global del azufre. La deposición atmosférica, que antes era una fuente constante y gratuita de azufre para los suelos agrícolas, se redujo drásticamente. Esto, combinado con prácticas de agricultura intensiva que extraen grandes cantidades de nutrientes del suelo, llevó a una creciente deficiencia de azufre en los cultivos de todo el mundo. El azufre es un macronutriente secundario, tan vital como el nitrógeno o el fósforo. Es un componente esencial de los aminoácidos cisteína y metionina, y por lo tanto, fundamental para la síntesis de proteínas y enzimas en las plantas. Una deficiencia de azufre puede limitar severamente el rendimiento y la calidad de los cultivos, manifestándose a menudo como un amarillamiento de las hojas más jóvenes.

El Azufre como Nutriente: Fertilizantes y Manejo Agrícola
Para corregir esta deficiencia, los agricultores ahora deben aplicar azufre deliberadamente a través de fertilizantes. La fuente de azufre elegida depende de las necesidades del cultivo, las condiciones del suelo y el costo. La forma en que las plantas pueden absorberlo es principalmente como sulfato (SO₄²⁻), una forma soluble en agua.
El azufre elemental (S) es una fuente popular, pero no es directamente asimilable. Debe ser oxidado a sulfato por bacterias del suelo, principalmente del género Thiobacillus. Este proceso biológico depende de factores como la temperatura, la humedad y, crucialmente, el tamaño de las partículas de azufre. Partículas más finas tienen una mayor superficie de contacto, lo que acelera la oxidación. Las partículas grandes pueden tardar meses o incluso años en convertirse en una forma útil para las plantas.
Tabla Comparativa de Fertilizantes con Azufre
| Fuente de Azufre | Contenido de S (%) | Solubilidad | Disponibilidad para la planta |
|---|---|---|---|
| Azufre elemental | ~90-99% | No soluble | Lenta (requiere oxidación microbiana) |
| Yeso (Sulfato de calcio) | 15-17% | Semi-soluble | Moderada |
| Sulfato de amonio | 24% | Soluble | Inmediata |
| Sulfato de potasio | 18% | Soluble | Inmediata |
| Tiosulfatos | 10-26% | Soluble | Inmediata a moderada |
Eliminación y Filtración de Azufre: Controlando su Presencia
Así como necesitamos añadir azufre a los campos, también necesitamos eliminarlo de otros lugares donde su presencia es perjudicial. Este control es fundamental tanto en la industria como en el tratamiento del agua potable.
En la Industria: Desulfuración de Combustibles
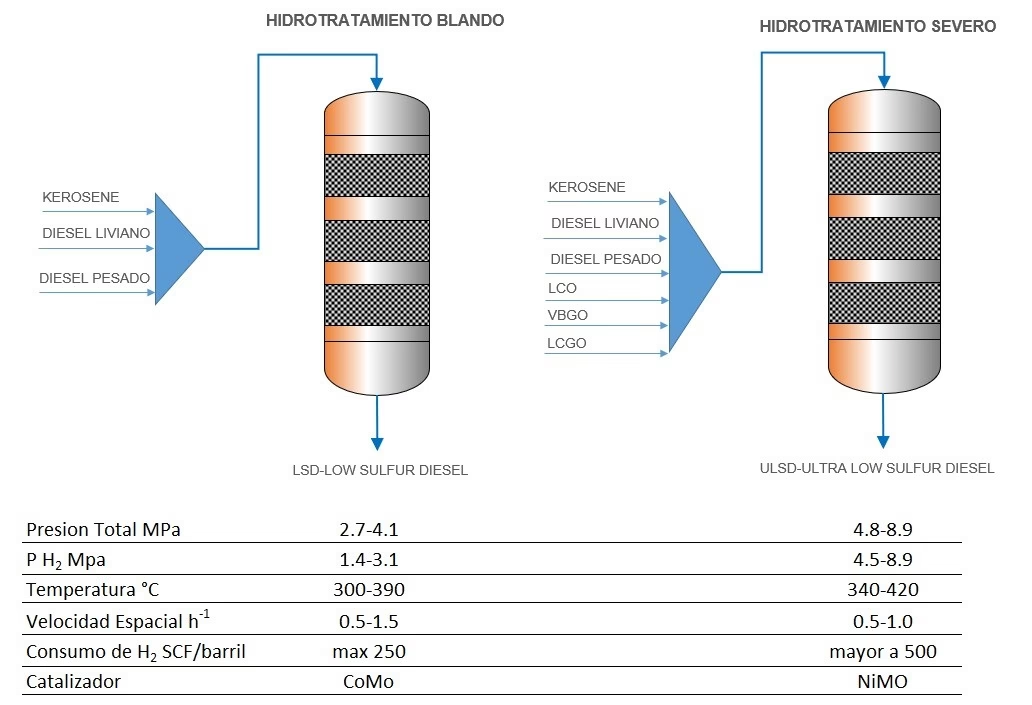
Para cumplir con las regulaciones ambientales, las refinerías de petróleo y gas deben eliminar el azufre de sus productos. El proceso más común se conoce como hidrodesulfuración. En este proceso, los compuestos de azufre presentes en el combustible crudo reaccionan con hidrógeno (H₂) a altas temperaturas y presiones en presencia de un catalizador, típicamente de Cobalto-Molibdeno (CoMo). Esta reacción convierte los compuestos orgánicos de azufre en sulfuro de hidrógeno gaseoso (H₂S). Posteriormente, este H₂S es capturado, a menudo por adsorción en óxido de zinc (ZnO), que se convierte en sulfuro de zinc (ZnS), dejando un combustible mucho más limpio y listo para su uso en reformadores o para la venta.
En el Agua Potable
La presencia de azufre en el agua subterránea es un problema común que afecta la calidad del suministro para consumo humano. Puede presentarse en dos formas principales:
- Sulfuros: Principalmente como gas sulfuro de hidrógeno (H₂S), que, aunque no suele ser peligroso para la salud a las concentraciones encontradas en el agua de pozo, le confiere un desagradable olor y sabor a huevo podrido. Además, es corrosivo para las tuberías de metal.
- Sulfatos: En altas concentraciones, los sulfatos pueden tener un efecto laxante y dar al agua un sabor amargo.
Existen diversos métodos para tratar estos problemas, dependiendo de la forma y concentración del azufre:
- Aireación: Exponer el agua al aire puede ayudar a que el gas H₂S se libere a la atmósfera.
- Oxidación: La adición de agentes oxidantes como cloro, ozono o peróxido de hidrógeno convierte el H₂S en azufre elemental, que luego puede ser eliminado por filtración.
- Ósmosis Inversa y Nanofiltración: Estos sistemas de membranas son muy eficaces para eliminar los sulfatos disueltos del agua.
- Intercambio Iónico: Similar a un ablandador de agua, un sistema de intercambio de aniones puede eliminar los sulfatos.
Preguntas Frecuentes (FAQ) sobre el Azufre
¿Por qué mi agua de pozo huele a huevo podrido?
Ese olor característico es causado por la presencia de gas sulfuro de hidrógeno (H₂S). Generalmente es producido por bacterias reductoras de azufre que pueden vivir en el pozo o en el sistema de plomería, especialmente en ausencia de oxígeno.
¿El azufre es siempre un contaminante?
No, es un elemento de doble cara. Mientras que el dióxido de azufre (SO₂) liberado por la quema de combustibles fósiles es un importante contaminante atmosférico causante de la lluvia ácida, el azufre en forma de sulfato (SO₄²⁻) es un nutriente esencial para el crecimiento de todas las plantas y animales.
¿Cómo llega el azufre a los fertilizantes que usamos?
El azufre para fertilizantes se obtiene de varias fuentes. Históricamente se extraía de depósitos volcánicos. Hoy en día, la mayor parte se obtiene como un coproducto del procesamiento de combustibles fósiles, como el petróleo y el gas natural. Al eliminar el azufre de estos combustibles para reducir la contaminación, se recupera y se procesa para usos agrícolas e industriales.
¿Qué es el ácido sulfúrico y por qué es tan importante?
El ácido sulfúrico (H₂SO₄) es el compuesto químico más producido a nivel mundial. Es un ácido fuerte y corrosivo con una inmensa importancia industrial. Su principal uso es en la fabricación de fertilizantes, pero también es crucial para procesar metales, producir detergentes, plásticos, explosivos y muchos otros productos de uso diario.
En conclusión, el azufre es un claro ejemplo de cómo la percepción de un elemento puede cambiar con el conocimiento científico y las necesidades de la sociedad. Pasó de ser el enemigo público número uno en la lucha contra la contaminación a ser un recurso valioso que debemos gestionar con inteligencia. El desafío actual radica en mantener su ciclo en equilibrio: continuar eliminándolo de nuestras emisiones y de nuestra agua para proteger la salud y el medio ambiente, al tiempo que aseguramos su disponibilidad para la agricultura, garantizando así la producción de alimentos para una población mundial en crecimiento. La gestión sostenible del azufre es, en esencia, un microcosmos del desafío ecológico global que enfrentamos.
Si quieres conocer otros artículos parecidos a Azufre: Del Contaminante al Nutriente Esencial puedes visitar la categoría Ecología.