24/08/2009
En el corazón de la ecología moderna y la biotecnología ambiental se encuentra una molécula fundamental: el ADN. Gracias a ella, podemos identificar especies en peligro, monitorear la biodiversidad en un ecosistema, detectar patógenos en el agua o incluso diseñar microorganismos capaces de limpiar derrames de petróleo. Sin embargo, el poder de estas técnicas depende de un factor a menudo subestimado y que ocurre tras bambalinas, en el laboratorio: la pureza de la muestra de ADN. Una contaminación, por mínima que parezca, puede invalidar por completo un estudio. Hoy nos adentraremos en un tipo de contaminación muy común y perjudicial, la del ADN genómico, y exploraremos las mejores prácticas para evitarla y asegurar que la ciencia ambiental avance sobre cimientos sólidos.
¿Qué es la Contaminación por ADN Genómico y Por Qué es un Problema?
Para entender el problema, primero debemos diferenciar dos tipos de ADN con los que los científicos trabajan habitualmente, sobre todo en el campo de la microbiología. Por un lado, tenemos el ADN genómico, que es el "libro de instrucciones" principal y completo de un organismo. En las bacterias, es una molécula cromosómica muy grande y compleja. Por otro lado, están los plásmidos, que son pequeñas moléculas de ADN circulares e independientes del cromosoma. Los plásmidos son herramientas biotecnológicas de un valor incalculable, ya que se pueden modificar e introducir en bacterias para que produzcan una proteína de interés o realicen una función específica, como degradar un contaminante.
El proceso de laboratorio llamado "miniprep" o minipreparación tiene como objetivo aislar estos valiosos plásmidos de un cultivo bacteriano. El problema surge cuando, durante este proceso, el enorme ADN genómico se rompe y se mezcla con los plásmidos. Esto es la contaminación por ADN genómico. Las consecuencias son nefastas:
- Resultados Falsos en PCR: Si se intenta amplificar un gen del plásmido, el ADN genómico contaminante puede interferir, dando lugar a resultados erróneos o no concluyentes.
- Secuenciación Incorrecta: Al intentar leer la secuencia de un plásmido, la presencia de fragmentos genómicos puede arruinar la lectura, generando datos confusos e inútiles.
- Fracaso en Experimentos Clave: En biotecnología ambiental, si se intenta usar un plásmido contaminado para modificar una bacteria, es muy probable que el experimento falle, perdiendo tiempo, recursos y retrasando posibles soluciones ecológicas.
La Lisis Celular: El Momento Crítico para Evitar la Contaminación
La mayoría de los problemas de contaminación genómica se originan en un paso crucial de la miniprep: la lisis celular. Durante este paso, se utilizan soluciones químicas para romper la pared y la membrana de las bacterias y liberar su contenido, incluidos los plásmidos.
El Error Fatal: La Agitación Excesiva
El error más común y dañino es agitar la muestra de forma demasiado violenta después de añadir la solución de lisis. Muchos protocolos indican que se debe resuspender el pellet celular y luego añadir las soluciones de lisis. Si en este punto se utiliza un vórtex o se agita bruscamente, se genera una fuerza mecánica muy intensa conocida como cizallamiento. Esta fuerza actúa como una tijera molecular, fragmentando el frágil y larguísimo ADN genómico en trozos mucho más pequeños. Estos fragmentos se comportan de manera similar a los plásmidos y son arrastrados junto a ellos durante el resto del proceso de purificación, resultando en una muestra contaminada.
La técnica correcta es la inversión suave. Una vez añadida la solución de lisis, el tubo debe cerrarse e invertirse suavemente de 4 a 6 veces, sin agitar. Este movimiento es suficiente para mezclar los reactivos y lisar las células de forma controlada, liberando los plásmidos pero manteniendo el ADN genómico intacto y en una masa gelatinosa que será fácilmente separable en el siguiente paso.
El Exceso de Reactivos y Tiempo
Otro error frecuente es excederse con la cantidad de solución de lisis o con el tiempo de incubación. Estas soluciones son alcalinas y muy potentes. Su objetivo es desnaturalizar tanto el ADN genómico como el plasmídico. Sin embargo, los plásmidos, al ser pequeños y circulares (superenrollados), pueden renaturalizarse rápidamente y volver a su forma original cuando se neutraliza la solución. El ADN genómico, al ser tan grande, no puede hacerlo y precipita. Si se deja la solución de lisis actuar por más de 5 minutos, puede dañar irreversiblemente también a los plásmidos, disminuyendo el rendimiento final. Es vital seguir los tiempos que indica el protocolo, que suelen ser de un mínimo de dos minutos para asegurar una lisis completa pero sin exceder los cinco minutos para evitar daños.
Tabla Comparativa: Prácticas para una Miniprep Exitosa
Para visualizar mejor la diferencia, aquí tienes una tabla comparativa de las prácticas correctas e incorrectas durante los pasos más críticos.
| Práctica Incorrecta ❌ | Práctica Correcta ✅ | Justificación |
|---|---|---|
| Usar el vórtex para mezclar tras añadir la solución de lisis. | Invertir el tubo suavemente de 4 a 6 veces. | La agitación violenta causa cizallamiento del ADN genómico, contaminando la muestra. La inversión suave lisa las células sin romper el cromosoma. |
| Incubar con la solución de lisis por más de 5 minutos. | Incubar el tiempo exacto que indica el protocolo (generalmente entre 2 y 5 minutos). | Un tiempo excesivo puede dañar de forma irreversible los plásmidos, reduciendo la cantidad y calidad del ADN obtenido. |
| Añadir más solución de lisis de la cuenta pensando que mejorará el resultado. | Utilizar los volúmenes exactos recomendados por el fabricante del kit. | Un exceso de reactivo puede hacer la lisis demasiado agresiva y dificultar la posterior neutralización y precipitación selectiva del ADN genómico. |
Plan B: ¿Qué Hacer si la Contaminación ya Ocurrió?
A veces, a pesar de seguir las mejores prácticas, puede ocurrir una ligera contaminación. En estos casos, existe una solución de rescate, aunque siempre es preferible la prevención. Se puede utilizar una enzima llamada DNasa I. Esta enzima tiene la capacidad de degradar cualquier tipo de ADN.
El truco consiste en un tratamiento controlado. La idea es añadir una pequeña cantidad de DNasa I a la muestra y dejarla incubar por un tiempo muy corto. El ADN genómico, al estar más expuesto y fragmentado, es más susceptible a la degradación por la enzima que los plásmidos superenrollados, que son más compactos y resistentes. Sin embargo, es un equilibrio muy delicado. Si la incubación es demasiado corta, no se eliminará la contaminación. Si es demasiado larga, la DNasa I también destruirá los plásmidos de interés.
Este método requiere una cuidadosa optimización de los tiempos de incubación y la concentración de la enzima, y debe ser considerado siempre como un último recurso, no como una práctica habitual.
Preguntas Frecuentes (FAQ)
¿Cómo puedo verificar si mi muestra de plásmido está contaminada con ADN genómico?
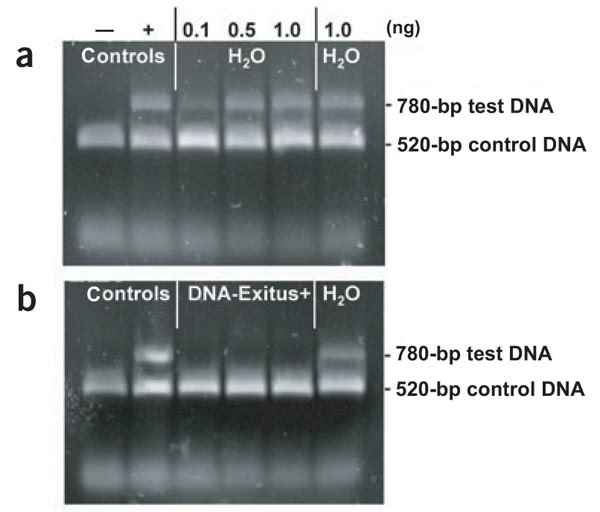
La forma más sencilla y común es mediante una electroforesis en gel de agarosa. Una muestra de plásmido pura mostrará bandas nítidas y bien definidas (generalmente una, dos o tres, correspondientes a las formas superenrollada, lineal y circular relajada del plásmido). Una muestra contaminada mostrará, además de las bandas del plásmido, una especie de "arrastre" o mancha difusa en la parte superior del carril, que corresponde a los fragmentos de alto peso molecular del ADN genómico.
¿Todos los kits de miniprep son iguales frente a este problema?
No. Aunque la mayoría de los kits modernos se basan en principios similares (lisis alcalina y purificación en columna de sílice), algunos están optimizados con soluciones tampón y protocolos que minimizan el riesgo de contaminación. Es importante leer y seguir al pie de la letra las instrucciones del fabricante específico que se esté utilizando.
¿Este problema solo afecta a la purificación de plásmidos de bacterias?
El principio de evitar el cizallamiento del ADN genómico es aplicable a casi cualquier extracción de ácidos nucleicos, ya sea de plantas, hongos o células animales. Sin embargo, los protocolos de lisis varían enormemente según el tipo de célula, siendo la lisis alcalina una técnica especialmente diseñada para la separación de plásmidos en bacterias.
Si quieres conocer otros artículos parecidos a ADN Puro: Clave para la Ecología Moderna puedes visitar la categoría Ecología.